��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
91EXAM.org
1������� (12��)��ͼ�У�A��LΪ�������ʻ�����ʵ�ˮ��Һ��B��A������ȼ�ղ�����ɫ�̣�B��GΪ��ѧ��ѧ�г����������ʣ�I����ɫ��ӦΪ��ɫ�����J��Ԫ��ԭ�Ӻ���ֻ��һ�����ӣ�FΪ��ɫ���д̼�����ζ���壬����ʹƷ����Һ��ɫ��
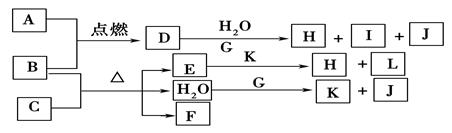
�ش��������⣺
(1)K�����Ļ�ѧ����?��
(2)D��ˮ��Һ��G��Ӧ�������ӷ���ʽΪ_______________________________________________��
(3)д����ҵ����ȡ����G�Ļ�ѧ����ʽ?��
(4)������Fͨ������װ����
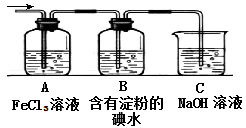
д��A��B�е����ӷ���ʽ��
?��?��
(5)����Fͨ��һ����K��ˮ��Һ�У���������Һ�и�����Ũ��һ������Ĺ�ϵʽΪ?
?��
�ο��𰸣���1�����Ӽ������ۼ���2��6Na��2Fe3����6H2O===2Fe(OH)3����6Na����3H2����3��2NaCl 2Na+Cl2����4��SO2+2Fe3++2H2O=SO42-+Fe2++4H+? SO2+I2+2H2O=4H++2I-+SO42-��5��c(Na��)��c(H��)��c(OH��)��c(HSO)��2c(SO)
2Na+Cl2����4��SO2+2Fe3++2H2O=SO42-+Fe2++4H+? SO2+I2+2H2O=4H++2I-+SO42-��5��c(Na��)��c(H��)��c(OH��)��c(HSO)��2c(SO)
��������������ͻ�ƿ�ΪB��A��ȼ��Ϊ��ɫ���̣�����ΪFe��������ȼ������I��ɫΪ��ɫ��Ϊ�ƵĻ����J��ֻ������ΪH��F��Ʒ����ɫΪSO2����Ͽ�ͼ�ۺϿ��ǿ���ȷ����AΪCl2��BΪFe��CΪH2SO4��DΪFeCl3��EΪFe2(SO4)3��FΪSO2��GΪNa��HΪFe(OH)3��IΪNaCl��JΪH2��KΪNaOH��LΪNa2SO4��
��1���������ƺ����Ӽ��ͼ��Թ��ۼ���
��2�������Ȼ�����Һ��Ӧ����Ϊ������ˮ��Ӧ�����ɵ��������������Ȼ�����Һ��Ӧ�����ӷ���ʽΪ6Na��2Fe3����6H2O===2Fe(OH)3����6Na����3H2����
��3����ҵ�ϵ�������Ȼ������ƣ�����ʽΪ2NaCl 2Na+Cl2����
2Na+Cl2����
��4����������ͨ���Ȼ�������ˮ�з���������ԭ��Ӧ�����ӷ���ʽ�ֱ�ΪSO2+2Fe3++2H2O=SO42-+Fe2++4H+? SO2+I2+2H2O=4H++2I-+SO42-��
��5����������ͨ������������Һ���������ʳɷֿ��������֣��������ƺ��������ơ��������ơ��������ƺ����������ơ����������ƣ���������������е���غ㣺c(Na��)��c(H��)��c(OH��)��c(HSO)��2c(SO)��
����������ھ����ۣ�������������������Ӧȷ�����ʡ�
�����Ѷȣ�һ��
2��ѡ���� Ԫ��X�ĵ��ʼ�X��Y�γɵĻ������ܰ�����ͼ��ʾ�Ĺ�ϵ����ת��(����m��n���Ҿ�Ϊ������)������˵����ȷ����
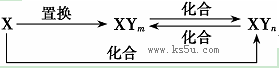
A��Xһ��Ϊ����Ԫ��
B��X��Y�����ܾ�Ϊ�ǽ���Ԫ��
C����XΪFe��Y��ΪCl��Br����������I
D����XΪFe��Yֻ��ΪCl
�ο��𰸣�C
�����������ΪCl2��Br2�������Դ���Fe3+����I2��������С��Fe3+������XΪFe��Y������Cl��Br��������I��X��Y����Ϊ�ǽ�������XΪC��YΪO��C������H2O�û�����CO��CO��O2��������CO2��CO2��C���Ͽ�������CO��
�����Ѷȣ���
3���ƶ��� �������п�ͼ��ϵ��ա���֪������XΪ��ɫҺ�壬D��E��Ϊ��ɫ���壬 G��һ����Ҫ�Ĺ�ҵ��Ʒ��C����ɫ��ӦΪ��ɫ��E��F����Է�����֮��Ĺ�ϵΪ M��F��=M��E��+16���ش���������

��1��A�л�ѧ��������Ϊ__________��д��B��һ����;__________��
��2��������A����CuSO4��Һ�е���Ҫ������____________________��
��3��д������B��ˮ��Һ��CuSO4��Һ��Ӧ�����ӷ���ʽ____________________��
��4��д����Ӧ�ڵĻ�ѧ����ʽ������������ԭ��Ӧ����������ת�Ƶķ������Ŀ��
_____________________________
��5�����ⶨ����Ӧ����ÿ����1.0gX���ų�3.2kJ�������������£�����д����Ӧ�ܵ��Ȼ�ѧ����ʽ________________________��
�ο��𰸣���1�� �Ǽ��Թ��ۼ������Ӽ�����������������
��2����ɫ���塢��ɫ����
��3��2NH3��H2O+Cu2+=Cu(OH)2��+2NH4+��4�� ��5��NaOH(aq)+HNO3(aq)=NaNO3(aq)+H2O(l) ����H= -57.6kJ/mol
��5��NaOH(aq)+HNO3(aq)=NaNO3(aq)+H2O(l) ����H= -57.6kJ/mol
���������
�����Ѷȣ�һ��
4������� A��B��C����������Ԫ����ɵ�������Ǻ͵��ʼס��ҡ���������ͼ��ʾ��ת����ϵ��ת�����̶�����Ҫʹ�ô�������
����������⣺

��1�������dz������������dz����ǽ������嵥�ʣ�A��C�ڳ����¾�Ϊ��ɫ���壬��A��B��C���ס��ҡ������ɶ�����Ԫ����ɣ���B�ĵ���ʽ��______��A���Ӧ�Ļ�ѧ����ʽ��______��
��2������ͼ��ʾ�ķ�Ӧ��ˮ��Һ�н��У����ڳ�����Ϊ��ɫ���壬���ڳ�����ΪҺ�壬���������г����Ľ�������
�ٱ���C��Ӧ�����ӷ���ʽΪ______��
����A��Һ����μ���NaOH��Һʱ���ܳ��ֵ�������______��
�ο��𰸣��ɿ�ͼ��֪������A+���ʼ�����B+������Ϊ�û���Ӧ����Ϊ������AΪ��ɫ��������ɻ�����A��һ��Ԫ��Ϊ�ɱ��̬�������ƶϼ�ΪMg��AΪCO2��������Һ�з�������Ϊ��۽����������Ƴ���������Fe����Ϊ��ɫ���壬��ΪCl2���ɲ�ȡ���뷨���飮�������ڳ�������Һ�壬������һ����Һ�壮
��1�������dz������������dz����ǽ������嵥�ʣ�A��C�ڳ����¾�Ϊ��ɫ���壬��A��B��C���ס��ҡ������ɶ�����Ԫ����ɣ��ƶϳ���ΪMg����ΪC����ΪO2��AΪCO2��BΪMgO��CΪCO��B�ĵ���ʽΪ��
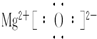
��A���Ӧ�Ļ�ѧ����ʽ��2Mg+CO2?��ȼ?.?2MgO+C��
�ʴ�Ϊ��
��2Mg+CO2?��ȼ?.?2MgO+C��
��2������ͼ��ʾ�ķ�Ӧ��ˮ��Һ�н��У����ڳ�����Ϊ��ɫ���壬���ڳ�����ΪҺ�壬���������г����Ľ��������ΪCl2��������ΪBr2����ΪFe��AΪFeBr2��BΪFeCl3��CΪFeBr3��
�ٱ�Fe��CFeBr3��Ӧ�����ӷ���ʽΪFe+2Fe3+�T3Fe2+���ʴ�Ϊ��Fe+2Fe3+�T3Fe2+��
����A��FeBr2����Һ����μ���NaOH��Һʱ���ܳ��ֵ����������ɰ�ɫ������Ѹ�ٱ�ɻ���ɫ������ɺ��ɫ���ʴ�Ϊ�����ɰ�ɫ������Ѹ�ٱ�ɻ���ɫ������ɺ��ɫ��
���������
�����Ѷȣ�һ��
5������� ��A��B��C��D��E��F��G��H�ȳ������ʣ���֪������ͼת����ϵ������B��C?Ϊ�����ǽ������ʣ�FΪ�����������ʣ�B��C��ȼ��ʱ������ʲ�ɫ��A��D����ɫ��ӦΪ��ɫ��G��D��Һ��ͣ��������ɫ������
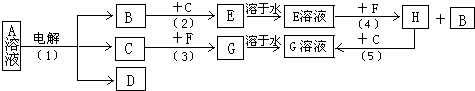
��1����Ӧ��1����������0.1mol?B����ת�Ƶĵ��ӵ����ʵ���Ϊ______��д��C��F��Ӧ�Ļ�ѧ����ʽ______����ע����Ӧ������
��2��ͼ����ʾ��5����Ӧ������������ԭ��Ӧ���У�______������д��ţ�
�ο��𰸣���1��B��C��ȼ��ʱ������ʲ�ɫ��˵��B��H2��C��Cl2����E��HCl���壬E��ҺΪ���ᣮA��D����ɫ��ӦΪ��ɫ��˵��A��D�к�Na+��G��D��Һ��ͣ��������ɫ������ΪFe��OH��3������˵��G�к�Fe3+�����FΪ�����������ʣ��Ƶ�FΪ����Fe����Ӧ��3��ΪCl2��Fe��Ӧ����FeCl3����Ӧ��4��Ϊ�����Fe��Ӧ����FeCl2��H2����Ӧ��5��ΪFeCl2��Cl2��Ӧ����FeCl3��B��H2��C��Cl2��D�к�Na+�����ݵ��ԭ���Ƶ÷�Ӧ��1���ǵ�ⱥ��ʳ��ˮ����A��ҺΪNaCl��Һ����Ӧ��1������ʽΪ��2NaCl+2H2O�T2NaOH+H2��+Cl2��������1molH2ת��2mol���ӣ�������0.1molH2��ת�Ƶĵ��ӵ����ʵ���Ϊ0.2mol��C��F��Ӧ�Ļ�ѧ����ʽΪ��2Fe+3Cl2?��ȼ?.?2FeCl3��
�ʴ�Ϊ��0.2mol��2Fe+3Cl2?��ȼ?.?2FeCl3��
��2����Ӧ��1������ʽΪ��2NaCl+2H2O?���?.?2NaOH+H2��+Cl2����
��Ӧ��2������ʽΪ��H2+Cl2?��ȼ?.?2HCl��
��Ӧ��3������ʽΪ��2Fe+3Cl2?��ȼ?.?2FeCl3��
��Ӧ��4������ʽΪ��2HCl+Fe�TFeCl2+H2����
��Ӧ��5������ʽΪ��2FeCl2+Cl2�T2FeCl3��
����5����Ӧ�ж��л��ϼ۵ı仯�����Զ�����������ԭ��Ӧ��
�ʴ�Ϊ����1������2������3������4������5����
���������
�����Ѷȣ�һ��