微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (15分)已知B为黑色粉末,用D、E、G作焰色反应,隔蓝色钴玻璃观察,焰色均呈紫色,F为深红棕色液体,H能使淀粉变蓝,它们之间的相互转化关系如图所示。

(1)请根据以上关系进行判断,指出下列物质的化学式:
A?,C?,D?,?G?.
(2)写出下列反应的化学方程式:
C+D:?;
A+B:?。
在A和B的反应中,A显示出来的性质是?(填写序号,多选倒扣)。
①只有还原性;②还原性和酸性;③只有氧化性;④氧化性和酸性
(3)C还能由以下反应制得:KClO3+6HCl=KCl+3Cl2↑+3H2 O,在该反应中,被氧化的氯元素与被还原的氯元素的物质的量之比为?。
O,在该反应中,被氧化的氯元素与被还原的氯元素的物质的量之比为?。
2、简答题 下列是中学常见的一些物质之间的转化关系(其中部分反应产物省略),其中I是一种金属单质,A是一种黄绿色的非金属单质;F、M、N均为难溶于水的白色沉淀物质,M和N不溶于稀硝酸;B是一种具有刺激性气味的气体,且具有漂白性;C和D是中学化学中两种常见的强酸.请回答下列问题:

(1)写出物质B和M的化学式:B.______,M.______;
(2)写出E→G转化反应的离子方程式:______;
(3)写出反应⑥的化学方程式:______;
(4)写出反应⑤的离子方程式:______.
3、填空题 下图中A、B、C、D、E为单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物。已知①C+G→B+H,放出大量的热,该反应曾应用于铁轨的焊接,G物质是磁铁矿的主要成分,②I是一种常见的温室气体,它和E发生反应:2E+I→2F+D,F中E元素的质量分数为60%,回答下列问题(每空2分,共12分)
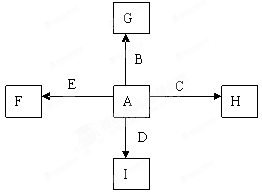
(1)反应①的化学方程式是?
(2)化合物I中所存在的化学键是?键(填“离子”或“极性”或“非极性”)
(3)称取11.9gB、C、E的混合物,用过量的NaOH溶液溶解后,过滤、称量剩余固体质量为9.2g,另取等质量的B、C、E的混合物用稀硝酸完全溶解,共收集到标况下气体6.72L,向剩余的混合液,加入过量的NaOH溶液使其中的金属离子完全沉淀,则沉淀的质量为(?)
A.27.2g? B.7.8g? C.2.7g? D.19.4g
(4)C与过量的NaOH溶液反应的离子方程式是:?
(5)将G溶于过量的稀盐酸中,欲检验其中的Fe3+的方案是?,欲检验其中的Fe2+的方案是?
A.滴加KSCN溶液,溶液变血红色?
B.加铁粉,溶液变浅绿色?
C.滴入酸性KMnO4溶液,迅速褪色?
D.滴加NaOH溶液,有白色沉淀且迅速变成灰绿色最后转化为红 褐色
褐色
4、简答题 图表示由元素周期表中1~20号且不同主族元素组成的单质及化合物之间转化关系(产物中的水已略去).其中A为单质;在实验室中,常用固体B和固体C加热制取气体F;F与G的组成元素相同,G与I分子所含电子数相同.请回答:
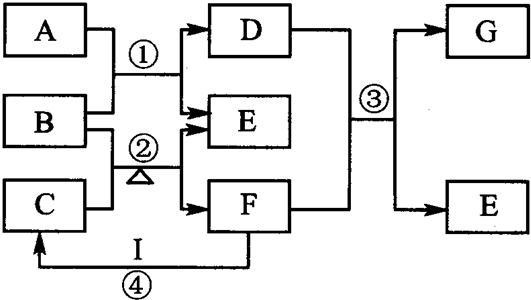
(1)写出B、G的化学式B______、G______.
(2)写出C的电子式______;反应④的实验现象为______;写出F的一种具体用途______.
(3)向具有漂白作用的D溶液加入I的稀溶液,写出反应的离子方程式:______.向D的溶液加入I的浓溶液有A生成,其反应的离子方程式为:______.
(4)写出反应③的化学方程式______.
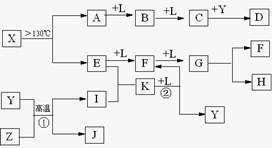
5、填空题 已知A、E、I、L是常见的非金属单质,其中A为淡黄色固体,Z是常见的金属单质,B的相对分子质量比A大32,C的相对分子质量比B大16,Y是一种常见的液体,J是磁铁矿的主要成分,D、H、K均是重要的工业产品,X分子的球棍模型如图所示,图中部分反应条件已略去。
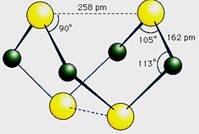 ?
?
试回答下列问题
(1)写出化学式:D?X ?。
(2)E的电子式为:?。
(3)写出化学方程式:①?;②?。