微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 依据事实,写出下列反应的热化学方程式。
(1)在25℃、101kPa下,1g液体甲醇燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为____________________________。
(2)若适量的N2和O2完全反应,每生成23g NO2需要吸收16.95kJ热量___________________________。
2、填空题 下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列问题:
周期
| ⅠA
|
| 0
|
1
| ①
| ⅡA
| ⅢA
| ⅣA
| ⅤA
| ⅥA
| ⅦA
|
|
2
|
|
|
| ②
| ③
| ④
|
|
|
3
| ⑤
|
| ⑥
|
|
| ⑦
| ⑧
|
|
(1)请画出元素⑥的离子结构示意图: 。
(2)元素⑦中质子数和中子数相等的同位素符号是: 。
(3)④、⑤、⑦的离子半径由大到小的顺序为: 。
(4)②的最高价氧化物对应水化物的电离方程式为: 。
(5)④、⑤两种元素的原子按1:1组成的常见化合物的电子式为: 。
(6)由表中两种元素形成的5核10电子分子常做燃料电池的燃料,该电池在碱性条件下的负极反应式为: 。
(7)由表中两种元素形成的氢化物A和B都含有18个电子,A是一种6原子分子,可做火箭发动机燃料;B是一种常见强氧化剂。已知16g液态A与液态B充分反应生成一种液态10电子分子和一种气态单质,并放出838kJ热量,写出A与B反应的热化学方程式: 。
3、填空题 (1)已知25℃、101kPa时,一些物质的燃烧热为

请回答下列问题:
①该条件下CH3OH(l)完全燃烧的热化学方程式为:__________________________。
②根据盖斯定律完成下列反应的热化学方程式:CO(g)+2H2(g)==CH3OH(l) ΔH=____________。
(2)①常温下,0.10mol/LNH4Cl溶液pH__________7(填>、=、<),溶液中各离子浓度由大到小的顺序是______________。
②相同物质的量浓度的Na2S溶液与NaHS溶液,pH大小关系是:Na2S________NaHS(填>、=、<),两种溶液中微粒种类:Na2S_______NaHS(填>、=、<)。
4、选择题 已知:CH3CH2CH2CH3(g)+6.5O2(g)→4CO2(g)+5H2O(l),1mol?CH3CH2CH2CH3完全燃烧放出?2878kJ热量;(CH3)2CHCH3(g)+6.5O2(g)→4CO2(g)+5H2O(l),1mol(CH3)2CHCH3燃烧放出2869kJ热量.下列说法正确的是( )
A.1molCH3CH2CH2CH3分子储存的能量大于1mol(CH3)2CHCH3分子
B.1molCH3CH2CH2CH3分子储存的能量小于1mol(CH3)2CHCH3分子
C.(CH3)2CHCH3转化为CH3CH2CH2CH3的过程是一个放热过程?
D.断开1mol物质中化学键吸收的能量CH3CH2CH2CH3大于(CH3)2CHCH3
5、选择题 已知在 25℃ ,101kPa 下,1g C8H18(辛烷)燃烧生成二氧化碳和液态水时放出48.40kJ热量。表示上述反应的热化学方程式正确的是
[? ]
A.C8H18(l)+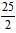 O2(g)=8CO2(g)+ 9H2O(g);ΔH = - 48.40 kJ・mol-1
O2(g)=8CO2(g)+ 9H2O(g);ΔH = - 48.40 kJ・mol-1
B.C8H18(l)+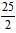 O2(g)=8CO2(g)+ 9H2O(l);ΔH = - 5518 kJ・mol-1
O2(g)=8CO2(g)+ 9H2O(l);ΔH = - 5518 kJ・mol-1
C.C8H18(l)+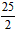 O2(g)=8CO2(g)+ 9H2O(l);ΔH = + 5518 kJ・mol-1
O2(g)=8CO2(g)+ 9H2O(l);ΔH = + 5518 kJ・mol-1
D.C8H18(l)+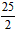 O2(g)=8CO2(g)+ 9H2O(l);ΔH = - 48.40 kJ・mol-1
O2(g)=8CO2(g)+ 9H2O(l);ΔH = - 48.40 kJ・mol-1