微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 关于浓H2SO4与Cu反应的叙述正确的是
A.在反应中,浓H2SO4只表现出氧化性
B.此反应属于复分解反应
C.在反应中,浓H2SO4既表现出氧化性,又表现出酸性
D.每1 mol铜参加反应就有2 mol浓H2SO4被还原,同时生成2 molSO2
参考答案:C
本题解析:注意原理和计量:Cu→CuO时,H2SO4为氧化剂;CuO→CuSO4时,H2SO4显示酸性.
本题难度:一般
2、选择题 对下列事实的解释正确的是
A.浓硝酸通常保存在棕色的试剂瓶中,说明浓硝酸不稳定
B.不用浓硝酸与铜屑反应来制取硝酸铜,说明浓硝酸具有挥发性
C.足量铁与稀硝酸反应后溶液呈浅绿色,说明稀硝酸不能氧化Fe2+
D.锌与稀硝酸反应得不到氢气,说明稀硝酸能使锌钝化
参考答案:A
本题解析:分析:A.见光受热易分解的物质应盛放在棕色瓶内,避光保存;
B.根据消耗药品的量与生成气体对环境污染分析;
C.过量的铁与铁离子反应生成亚铁离子;
D.钝化是反应生成致密的氧化物保护膜,阻止金属与硝酸继续反应,硝酸为氧化性酸,与金属反应不能生成氢气,生成氮的氧化物等.
解答:A.浓硝酸通常保存在棕色的试剂瓶中避光保存,说明浓硝酸见光易分解,故A正确;
B.1mol铜反应需要消耗4mol浓硝酸,同时生成二氧化氮,污染环境,通常利用硝酸与氧化铜反应取硝酸铜,与浓硝酸挥发性无关,故B错误;
C.铁与硝酸反应首先生成硝酸铁,溶液呈浅绿色由过量的铁与铁离子反应生成亚铁离子所致,故C错误;
D.硝酸为氧化性酸,与锌反应不能生成氢气,生成氮的氧化物等,与钝化无关,故D错误;
故选A.
点评:本题考查硝酸的性质,难度不大,旨在考查学生对据此知识的理解掌握,注意基础知识的理解掌握.
本题难度:简单
3、选择题 下列材料中最不适宜制造储存浓硫酸的容器的是
A.铁
B.铝
C.铜
D.陶瓷
参考答案:C
本题解析:铁、铝在冷的浓硫酸中发生钝化,陶瓷与浓硫酸不反应。铜能与浓硫酸反应,不能用铜为原料制造储存浓硫酸的容器。
本题难度:一般
4、选择题 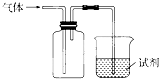 如图装置可用于收集气体并验证其化学性质,下列对应关系完全正确的是
如图装置可用于收集气体并验证其化学性质,下列对应关系完全正确的是
A.A
B.B
C.C
D.D
参考答案:C
本题解析:分析:A.NO不能用排空法收集;
B.乙烯密度比水空气略小,不能用向上排空法收集;
C.二氧化硫密度比空气大,可用向上排空法收集,具有还原性,可与酸性高锰酸钾反应;
D.氨气密度比空气小,不能用向上排空法收集.
解答:A.NO易与氧气反应,不能用排空法收集,故A错误;
B.乙烯密度比水空气略小,不能用向上排空法收集,可用排水法收集,故B错误;
C.二氧化硫密度比空气大,可用向上排空法收集,具有还原性,可与酸性高锰酸钾反应,故C正确;
D.氨气密度比空气小,不能用向上排空法收集,应用向下排空法收集,故D错误.
故选C.
点评:本题考查实验方案的评价,侧重于气体的收集和性质检验的考查,注意常见气体的收集方法,把握性质是解答的关键.
本题难度:一般
5、填空题 工业上以硫铁矿为原料制硫酸所产生的尾气除了含有N2、O2外,还含有SO2、微量的SO3和酸雾。为了保护环境,同时提高硫酸工业的综合经济效益,应尽可能将尾气中的SO2转化为有用的副产品。
请按要求回答下列问题:
(1)将尾气通入氨水中,能发生多个反应,写出其中可能发生的两个氧化还原反应的化学方程式______________________、 _______________________。
(2)在尾气与氨水反应所得到的高浓度溶液中,按一定比例加入氨水或碳酸氢铵,此时溶液的温度会自行降低,并析出晶体。
①导致溶液温度降低的原因可能是_______________________________;
②析出的晶体可用于造纸工业,也可用于照相用显影液的生产。已知该结晶水合物的相对分子质量为
134,则其化学式为_____________;
③生产中往往需要向溶液中加入适量的对苯二酚或对苯二胺等物质,其目的是______________。
(3)能用于测定硫酸尾气中SO2含量的是_________。(填字母)
(A)NaOH溶液、酚酞试液 (B)KMnO4溶液、稀H2SO4 (C)碘水、淀粉溶液 (D)氨水、酚酞试液
参考答案:(1)2SO2+O2+2H2O = 2H2SO4(或2H2SO3+O2 = 2H2SO4);2(NH4)2SO3+O2 = 2(NH4)2SO4;
2NH4HSO3+O2 = 2NH4HSO4(任意两个即可)
(2)①反应吸热;②(NH4)2SO3・H2O;③防止+4的硫被氧化
(3)BC
本题解析:
本题难度:一般