��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� һ�������´��ڷ�Ӧ��CO(g)��H2O(g) CO2(g)��H2(g)��������Ӧ���ȡ�����������ͬ��2 L���ݾ���(�����û����������)�ܱ��������ڢ��г���1 mol CO��1 mol H2O���ڢ��г���1 mol CO2��1 mol H2���ڢ��г���2 mol CO��2 mol H2O,700 �������¿�ʼ��Ӧ���ﵽƽ��ʱ������˵����ȷ����(����)
CO2(g)��H2(g)��������Ӧ���ȡ�����������ͬ��2 L���ݾ���(�����û����������)�ܱ��������ڢ��г���1 mol CO��1 mol H2O���ڢ��г���1 mol CO2��1 mol H2���ڢ��г���2 mol CO��2 mol H2O,700 �������¿�ʼ��Ӧ���ﵽƽ��ʱ������˵����ȷ����(����)
A��������������Ӧ������ͬ
B���������з�Ӧ��ƽ�ⳣ����ͬ
C����������CO�����ʵ������������еĶ�
D����������CO��ת��������������CO2��ת����֮��С��1
�ο��𰸣�CD
����������������з�Ӧ������У��ų��������������з�Ӧ������У��������������������з�Ӧ�¶Ȳ�ͬ�����������Ӧ���ʲ���ͬ��A�����������м��뷴Ӧ��������������ж࣬���ڸ÷�ӦΪ���ȷ�Ӧ�����зų������Ȣ�࣬���з�Ӧ������еij̶ȱȢ�С������������з�Ӧ�Ļ�ѧƽ�ⳣ���Ȣ�С��B����?���з�Ӧ������У��ų����������з�Ӧ������У���������������������Ϊ������������͢��з�Ӧ���еij̶Ⱦ���С����C��D����ȷ��
�����Ѷȣ�һ��
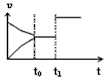
2��ѡ���� ��ͼ�DZ�ʾ��2X(g) ��Y(g)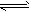 Z(g)��2R(g) ��H<0�����巴Ӧ���ʣ��ԣ���ʱ�䣨t���Ĺ�ϵ��t1ʱ��ʼ�ı������������ı�������������ߵ���
Z(g)��2R(g) ��H<0�����巴Ӧ���ʣ��ԣ���ʱ�䣨t���Ĺ�ϵ��t1ʱ��ʼ�ı������������ı�������������ߵ���
[? ]
A������Z����
B�������¶�
C���Ӵ�ѹǿ
D��ʹ�ô���
�ο��𰸣�CD
���������
�����Ѷȣ�һ��
3������� ��1923����ǰ���״�һ������ľ�Ļ�����ϵķֽ������������ġ����ڹ�ҵ�Ϻϳɼ״�����ȫ������һ����̼�������̼��ѹ������ķ��������չ��̰����������ϳɾ������״��ϳɺʹּ״�����ȹ���
��֪�״��Ʊ����йػ�ѧ��Ӧ�Լ��ڲ�ͬ�¶��µĻ�ѧ��Ӧƽ�ⳣ�����±���ʾ��

��1����Ӧ����____________(����ȡ����ȡ�)��Ӧ��
��2��ij�¶��·�Ӧ����H2��ƽ��ת����(a)����ϵ��ѹǿ(P)�Ĺ�ϵ����ͼ��ʾ����ƽ��״̬��A�䵽Bʱ��ƽ�ⳣ��K(A)_____K(B)(�����������������)��
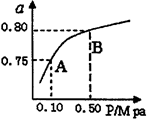
�ݷ�Ӧ����ڿ��Ƶ���K1��K2��K3֮��Ĺ�ϵ����K3��_________(��K1��K2��ʾ
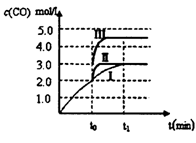
��3����3L�ݻ��ɱ���ܱ������з�����Ӧ�ڣ���֪c(CO)�뷴Ӧʱ��t�仯���ߢ�����ͼ��ʾ������t0ʱ�̷ֱ�ı�һ�������������ߢ�ɱ�Ϊ���ߢ�����ߢ����ߢ��Ϊ���ߢ�ʱ���ı��������_____________�������ߢ��Ϊ���ߢ�ʱ���ı��������________��
��4���״�ȼ�ϵ�����Ź㷺����;�������ò�Ϊ�缫���ϣ������Ϸֱ�ͨ��״���������
������������ҺΪ�������Һ����ü���ȼ�ϵ�صĸ�����Ӧʽ��_________________��
��5��һ�������¼״���һ����̼��Ӧ���Ժϳɴ��ᡣͨ��״���£���a mol��L�Ĵ�����b mol��L Ba(OH)2��Һ�������ϣ���Ӧƽ��ʱ��2c(Ba2��)=c(CH3COO��)���ú�a��b�Ĵ���ʽ��ʾ�û����Һ�д���ĵ��볣��Ϊ_____________��
�ο��𰸣���1������(2��)?��2�� =(2��)? K1��K2?(2��)
��3���������(2��)�� �����������(����)ѹ����2L(2�֣����𡰼�ѹ����1��)
��4�� CH3OH��6 e-��8 OH-=CO32-��6 H2O��
��5��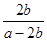 ?��10��7 (3��)
?��10��7 (3��)
�����������1�� ��Ӧ�������¶ȵ�����K��������ӦΪ���ȷ�Ӧ��
��2��ƽ�ⳣ��ֻ���¶ȱ仯����ѹǿ�أ�ƽ�ⳣ��K(A)=K(B)���ݷ�Ӧ��+��=�ۿ��Ƶ���Ӧ���ʵ�Ũ����K������֮���Ĺ�ϵ����K3��K1��K2��
��3�����ߢ��Ϊ����IIʱ����Ӧ���ʼӿ죬��c(CO)ƽ��Ũ�Ȳ��䣬�ı�������Ǽ�����������ߢ��Ϊ����IIIʱ����Ӧ���ʼӿ죬c(CO)ƽ��Ũ�����ӣ��ı�������ǽ����������(����)ѹ����2L(���𡰼�ѹ����ȷ)
��4�� �״��Ǹü���ȼ�ϵ�صĸ�����ʧȥ���ӣ���Ӧʽ��CH3OH��6 e-��8 OH-=CO32-��6 H2O ��
��5����a mol/L�Ĵ�����b mol/L Ba(OH)2��Һ�������ϣ���Ӧƽ��ʱ��2c(Ba2��)=c(CH3COO��)="2b" mol/L���ɵ���غ�ó�c(H��)=c(OH��)= 10��7 mol/L����CH3COOH CH3COO-+H+������ĵ��볣��Ϊ
CH3COO-+H+������ĵ��볣��Ϊ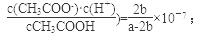
�����Ѷȣ���
4��ѡ���� ����ij��ѧ��Ӧ�ķ�Ӧ���ʵ���Ҫ�����ǣ�������
A����Ӧ���¶�
B��������ʹ��
C����Ӧ���Ũ��
D����Ӧ�������
�ο��𰸣��������ѧ��Ӧ���ʵĸ���ԭ��Ӧ�ﱾ�������ʣ���Ũ�ȡ��¶ȡ�ѹǿ��������Ӱ�����أ���ѡ��D��
���������
�����Ѷȣ�һ��
5������� 300��ʱ����2mol A��2mol B������������2L�ܱ������У��������·�Ӧ��3A(g)+B(g) 2C(g)+2D(g)?��H��2minĩ�ﵽƽ�⣬����0.8mol D��
2C(g)+2D(g)?��H��2minĩ�ﵽƽ�⣬����0.8mol D��
(1)��2minĩʱ��A��ƽ��Ũ��Ϊ_____________��B��ת����___________��0-2min��D��ƽ����Ӧ����Ϊ_____________��
(2)�÷�Ӧ��ƽ�ⳣ������ʽΪ��K=_____________�����¶��µĻ�ѧƽ�ⳣ����ֵΪ =____________��
=____________��
��֪350��ʱ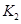 =l�����H________0���>����<������
=l�����H________0���>����<������
(3)��300��ʱ�����÷�Ӧ����ѹ�����ΪlL����A��ת����___________�����������С�����䡱����ԭ����__________________���������µ�ƽ�ⳣ��Ϊ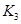 �� ��K3________
�� ��K3________ �����<����>����=������ԭ����_______________________��
�����<����>����=������ԭ����_______________________��
(4)���жϸ÷�Ӧ�Ƿ�ﵽ��ѧƽ��״̬��������__________________����ѡ�۷֣���
A��������ѹǿ���� ?B�����������c(A)����
C�� (A)=
(A)=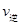 (C)? D����������ܶȲ���
(C)? D����������ܶȲ���
�ο��𰸣���1��0.4mol�ML? 20�G? 0.2 mol�M(L��min)? (2)K={C2(C)C2(D) }�M{C3(A)C (B)}? 0.5? >
(3)���䡣����ѹǿ��ƽ�ⲻ�ƶ�= Kֵֻ���¶��й� ��?��4��B
���������(1)���ݷ�Ӧ����ʽ��3A(g)+B(g) 2C(g)+2D(g)�ɿ�������ӦʱA ��B��C��D�����ʵ����Ĺ�ϵ��3��1��2��2����Ϊ����0.8mol��D����������A1.2mol������B0.4mol������C0.8mol����A��ƽ��Ũ��Ϊ����2-1.2��mol��2L="0.4mol�ML" . B��ת����Ϊ��0.4mol��2mol�� 100%="20%," 0-2min��D��ƽ����Ӧ����ΪV="��C�M" ��t="(0.8mol��2L)" �M2min=" 0.2" mol�M(L��min).(2)��ѧƽ�ⳣ���ǿ��淴Ӧ�ﵽ��ѧƽ��ʱ��������Ũ����ָ���Ļ������Ӧ��Ũ����ָ���Ļ�֮K={C2(C)C2(D) }�M{C3(A)C (B)}���ﵽ��ѧƽ��ʱ�����ʵ�Ũ�ȷֱ���C(A)=" 0.4mol�ML" ;C(B)="(2-0.4)mol��2L=0.8mol�ML" ;C(C)=" 0.8mol" ��2L="0.4" mol�ML ;C(D)=" 0.8mol" ��2L="0.4" mol�ML�����Ի�ѧƽ�ⳣ��Ϊ��K1={��0.4��2����0.4��2}�M{��0.4��3��0.8}=0.5.����Ϊ��350��ʱK2=l���ɼ������¶ȣ�K����˵�������¶Ȼ�ѧƽ��������Ӧ�����ƶ������ݻ�ѧƽ���ƶ�ԭ���������¶ȣ���ѧƽ�������ȷ�Ӧ�����ƶ���������Ӧ�����ȷ�Ӧ���ʡ�H>0.��3������Ӧ�������ѹ����Ҳ��������ѹǿ�����ݻ�ѧƽ���ƶ�ԭ��������ѹǿ����ѧƽ�������������С�ķ����ƶ������÷�Ӧ�Ǹ���Ӧǰ�����������ȵķ�Ӧ����������ѹǿ����ѧƽ�ⲻ�ƶ�����ʱA��B��ת�����ʶ����ᷢ���仯����ѧƽ�ⳣ��ֻ���¶��йء���������Ͷ�ϵĶ��ټ������ء�����K1=K3. (4)����Ӧ�ﵽ��ѧƽ��ʱ�����ʵ�Ũ�Ȳ��䣬��ͬһ���ʱ�ʾ������Ӧ���ʺ��淴Ӧ������ȣ������ʵĺ������䡣����������������䣬�÷�Ӧ�Ǹ���Ӧǰ�����������ȵķ�Ӧ�������κ�ʱ��ѹǿ���䣬������ܶ�Ҳ���䣬�����Dz�����Ϊ�ж�ƽ��ı�־����ȷѡ��Ϊ��B��
2C(g)+2D(g)�ɿ�������ӦʱA ��B��C��D�����ʵ����Ĺ�ϵ��3��1��2��2����Ϊ����0.8mol��D����������A1.2mol������B0.4mol������C0.8mol����A��ƽ��Ũ��Ϊ����2-1.2��mol��2L="0.4mol�ML" . B��ת����Ϊ��0.4mol��2mol�� 100%="20%," 0-2min��D��ƽ����Ӧ����ΪV="��C�M" ��t="(0.8mol��2L)" �M2min=" 0.2" mol�M(L��min).(2)��ѧƽ�ⳣ���ǿ��淴Ӧ�ﵽ��ѧƽ��ʱ��������Ũ����ָ���Ļ������Ӧ��Ũ����ָ���Ļ�֮K={C2(C)C2(D) }�M{C3(A)C (B)}���ﵽ��ѧƽ��ʱ�����ʵ�Ũ�ȷֱ���C(A)=" 0.4mol�ML" ;C(B)="(2-0.4)mol��2L=0.8mol�ML" ;C(C)=" 0.8mol" ��2L="0.4" mol�ML ;C(D)=" 0.8mol" ��2L="0.4" mol�ML�����Ի�ѧƽ�ⳣ��Ϊ��K1={��0.4��2����0.4��2}�M{��0.4��3��0.8}=0.5.����Ϊ��350��ʱK2=l���ɼ������¶ȣ�K����˵�������¶Ȼ�ѧƽ��������Ӧ�����ƶ������ݻ�ѧƽ���ƶ�ԭ���������¶ȣ���ѧƽ�������ȷ�Ӧ�����ƶ���������Ӧ�����ȷ�Ӧ���ʡ�H>0.��3������Ӧ�������ѹ����Ҳ��������ѹǿ�����ݻ�ѧƽ���ƶ�ԭ��������ѹǿ����ѧƽ�������������С�ķ����ƶ������÷�Ӧ�Ǹ���Ӧǰ�����������ȵķ�Ӧ����������ѹǿ����ѧƽ�ⲻ�ƶ�����ʱA��B��ת�����ʶ����ᷢ���仯����ѧƽ�ⳣ��ֻ���¶��йء���������Ͷ�ϵĶ��ټ������ء�����K1=K3. (4)����Ӧ�ﵽ��ѧƽ��ʱ�����ʵ�Ũ�Ȳ��䣬��ͬһ���ʱ�ʾ������Ӧ���ʺ��淴Ӧ������ȣ������ʵĺ������䡣����������������䣬�÷�Ӧ�Ǹ���Ӧǰ�����������ȵķ�Ӧ�������κ�ʱ��ѹǿ���䣬������ܶ�Ҳ���䣬�����Dz�����Ϊ�ж�ƽ��ı�־����ȷѡ��Ϊ��B��
�����Ѷȣ�һ��