��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ����Ͽ�ѧ�ķ�չ�����������仯����õ���Խ��Խ�㷺��Ӧ�ã�Ϊ�������ú�������������V2O5��VOSO4�������Բ�������������Ա����������һ�����ӽ��������շ����¹��գ������ʴ�91.7%���ϣ��ù��յ���Ҫ������ͼ1��
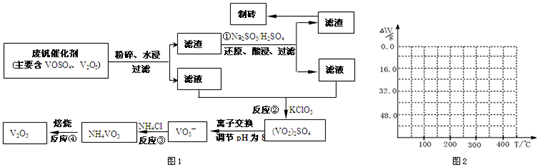
���ַ��Ļ�������ˮ�е��ܽ������±���ʾ���ɴ˻ش��������⣺
| ���� | VOSO4 | V2O5 | NH4VO3 | ��VO2��2SO4
�ܽ���
����
����
����
����
|
��1��23V��Ԫ�����ڱ�λ�ڵ�______����______�壮��ҵ����V2O5ұ���������������ȼ������仯ѧ����ʽΪ______��
��2����Ӧ�ٵ�Ŀ����______��
��3���ⶨ��Ӧ����Һ�з��ĺ�����������֪Ũ�ȵ��ữH2C2O4��Һ�ζ���VO2��2SO4��Һ����Ҫ����ΪCO2��VOSO4�������ӷ���ʽΪ��______��
��4����֪NH4VO3�ڱ��չ�����150��200��ʱ��ʧȥ������300��350����ʧȥˮ�������ұ�����ͼ2�л�������234g?NH4VO3���������ļ���ֵ��W���¶ȣ�T���仯�����ߣ�
�ο��𰸣���1������23V��������������Ϊ23��ԭ�ӣ����Է�Ԫ��λ�ڵ������ڣ���?VB?���壻������ȷ�Ӧ��ԭ��д����ѧ����ʽ���ʴ𰸣��ģ�VB��?3V2O5+10A?����?.?l6V+5Al2O3��
��2������������������ƣ�Ŀ��������������ԭ��Ӧ�����������ƻ�ԭV2O5����V2O5?ת��Ϊ�����Ե�VOSO4�������ᴿ���ʴ𰸣���V2O5?ת��Ϊ�����Ե�VOSO4��
��3���ⶨ��Ӧ����Һ�з��ĺ�����������֪Ũ�ȵ��ữH2C2O4��Һ�ζ���VO2��2SO4��Һ����Ҫ����ΪCO2��VOSO4�����ݻ��ϼ�������д�����ӷ���Ϊ2VO2++H2C2O4+2H+=2?VO2++2?CO2��+2?H2O��
�ʴ𰸣�2VO2++H2C2O4+2H+=2?VO2++2?CO2��+2?H2O��
��4����ʽΪ��
2NH4VO3�TV2O5+2NH3��+H2O
234g?34g?18g
����ֵ��ʼΪ0��34g�����ߴ�150�濪ʼ���٣�34gNH3������200��ʱ����32.0g�����������߿�ʼƽֱ����300��ʱ�ֿ�ʼ���٣�H2O������������350��ʱ����52gʱ����48.0g�Եͣ��Ͳ��ٱ仯������ͼ������

�ʴ�Ϊ��

���������
�����Ѷȣ�һ��
2������� ���ǵؿ��к����ܷḻ��Ԫ�أ�Ҳ���������������Ԫ�أ����������ڸ�¯��ұ���ģ���ұ��ҵ�У����ý�̿��ұ������
��1��д��������CO��ԭ�����Ļ�ѧ����ʽ��______��
��2��ʵ�����п���CO��ԭFe2O3��ʵ��װ��ͬCO��ԭCuO�����ڼ���Fe2O3ǰӦ______��ֱ����______����ʱ���ܵ�ȼ�ƾ��Ƽ��ȣ�������ܷ���______����δ��Ӧ��ȫ��CO______����ܡ��������ܡ����ŷŵ������У�Ӧ��______������
�ο��𰸣���1��CO���л�ԭ�ԣ�������CuO��Fe2O3�����ʣ��ڸ��������£�Fe2O3��CO��ԭ����Fe��CO2����Ӧ����ʽΪ��Fe2O3+3CO����.2Fe+3CO2��
�ʴ�Ϊ��Fe2O3+3CO����.2Fe+3CO2��
��2��CO��ȼ�գ���ȼ������CO������ը������ʵ��ʱӦ���鴿��ʵ��ʱ��ͨ��COһ��ʱ�䣬�ų�װ���еĿ�������û�б�������ʱ�ٵ�ȼ�ƾ��ƣ���ֹ������ȫ�¹ʣ���CO�ж�������ֱ���ŷ��ڿ����У��������Ⱦ������Ӧ��ȼ������
�ʴ�Ϊ���鴿����������ը�����ܣ���ȼ��
���������
�����Ѷȣ�һ��
3��ѡ���� ����˵��������ǣ�������
A��ͨ�����ȷֽ�HgO���Ƶõ���Hg
B������ʱ����ԭ��CO�����������л�ԭ����
C��ɳ���Խ������ý��ɳ�ӵ��ܶȲ�ͬ���Ӷ��������������
D�����ý���Na��Mg��Al��ұ������ͨ�����������״̬���Ȼ����Ƶõ�
�ο��𰸣�D
���������
�����Ѷȣ���
4��ѡ���� ﮳����������������أ���֪﮵Ľ����Խ����ƺ�þ֮�䣬��ұ�������Ӧ���õķ����ǣ� ? ��
A���Ȼ�ԭ��
B����ⷨ
C���ȷֽⷨ
D�����ȷ�
�ο��𰸣�B
���������
�����Ѷȣ���
5��ѡ���� ����ͭ���й㷺����;����ͭ�纬������Fe��Ni��Au �����ʣ����õ�ⷨ�Ʊ��ߴ��ȵ�ͭ������������ȷ����(��֪��������Fe2+��Ni2+��Cu2+)
[? ]
A.������Һ�д��ڵĽ���������ֻ��Cu2+
B.�������У��������ٵ��������������ӵ��������
C.����������ԭ��Ӧ����缫��Ӧʽ��Cu2++2e-=Cu
D.�����۵ײ����������������Ľ������ʺ���Ni��Ag��Au
�ο��𰸣�C
���������
�����Ѷȣ�һ��