��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ���з�Ӧ�����ӷ���ʽ��ȷ����
A.CuSO4��Һ����H2S���壺
B.Ca��HCO3��2��Һ��������NaOH��Һ��ϣ���CaCO3��+
C.����������Һ�м����������ữ�Ĺ���������Һ��Fe2++2H++H2O2��Fe2++2H2O
D.���۵⻯����Һ�ڿ����б�����4I-+O2+2H2O��
�ο��𰸣�AD
���������������A����Ӧ����CuS�����
B��������NaOH��Һ��ȫ��Ӧ����Ӧ����̼��ơ�ˮ��̼�����ƣ�
C������������ԭ��Ӧ������������ˮ��
D������������ԭ��Ӧ���ɵ��KOH��
���A��CuSO4��Һ����H2S��������ӷ�ӦΪCu2++H2S�TCuS��+SO42-����A��ȷ��
B��Ca��HCO3��2��Һ��������NaOH��Һ��ϵķ�ӦΪCa2++HCO3-+OH-=CaCO3��+H2O����B����
C������������Һ�м����������ữ�Ĺ���������Һ�����ӷ�ӦΪ2Fe2++2H++H2O2�T2Fe3++2H2O����C����
D�����۵⻯����Һ�ڿ����б��������ӷ�ӦΪ4I-+O2+2H2O�TI2+4OH-����D��ȷ��
��ѡAD��
���������⿼�����ӷ�Ӧ����д����ȷ�����Ļ�ѧ��Ӧ���ջ�ѧ��Ӧ��ʵ���ǽ��Ĺؼ�������������ԭ��Ӧ�����ӷ�Ӧ���飬��Ŀ�ѶȲ���
�����Ѷȣ�һ��
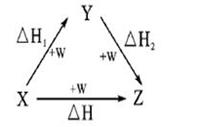
2��ѡ���� ������ͼ��ʾ��ת����ϵ���ҵ�X��Y��Z�����ʵ������ʱ�������ʱ��H=��H1+��H2����������������X��Y�����ǣ� ��
��C��CO ��S��SO2 ��Na��Na2O
��AlCl3��Al��OH��3 ��Fe��Fe��NO3��2 ��NaOH��Na2CO3
A���٢ܢ� B���٢ڢ� C���٢ۢ� D���٢ۢܢݢ�
�ο��𰸣�A
�����������ͼ��ʾ�ĺ�����ָ��ѧ��Ӧ�������뷴Ӧ�����أ�ֻ��ʼ��̬�йأ�����˹���ɣ���X��Z�ķ�Ӧ�ɿ���X��Y�ķ�Ӧ��Y��Z�ķ�Ӧ֮�͡���X��Y��C��CO ����Z�Ƕ�����̼�����ϴ�ͼ����ȷ����X��Y��S��SO2 ����Z����������������ΪS����ֱ����������������X��Y��Na��Na2O ��Na���� 1molNa2Oʱ��Ҫ2molNa�����Ե�X��Y��Z�����ʵ������ʱ���������ʱ��H=��H1+��H2������X��Y��AlCl3��Al��OH��3����Z��NaAlO2�����ϴ�ͼ����ȷ�� ��X��Y��Fe��Fe��NO3��2��Z��Fe��NO3��3,���ϴ�ͼ����ȷ�� ��X��Y��NaOH��Na2CO3����Z��NaHCO3������1mol Na2CO3��NaHCO3ʱ����NaOH�����ʵ�������ȣ����Ե�X��Y��Z�����ʵ������ʱ���������ʱ��H=��H1+��H2������ѡA��
���㣺���ɶԸ�˹���ɵ�����
�����Ѷȣ�һ��
3��ѡ���� ���������У�ֻ���зǼ��Թ��ۼ����ǣ�?��
A��Na2O
B��H2O
C��Cl2
D��NH3
�ο��𰸣�C
���������һ����õĽ����ͻ��õķǽ��������γ����Ӽ����ǽ���Ԫ�ص�ԭ�Ӽ������γɹ��ۼ����ݴ˿�֪ѡ��A��ֻ�����Ӽ���B��ֻ�м��Լ���C��ֻ�зǼ��Լ���D��ֻ�м��Լ�����ѡC��
�����������Ǹ߿��еij������㣬���ڻ���������Ŀ��飬���������ǿ�����ض�ѧ������֪ʶ��ѵ������Ҫ�ǿ���ѧ��������û�ѧ��֪ʶ���ʵ�����������������Ĺؼ�����ȷ���Ӽ������ۼ��ĺ�����ж����ݣ�Ȼ��������������ü��ɡ�
�����Ѷȣ�һ��
4��ѡ���� ijԪ�ص�ԭ�������ֻ��һ�����ӣ�������Ԫ�ؽ��ʱ��������
A��һ���γɹ��ۼ�
B��һ���γ����Ӽ�
C�������γɹ��ۼ���Ҳ�����γ����Ӽ�
D������˵��������
�ο��𰸣���ijԪ�ص�ԭ�������ֻ��һ�����ӣ���Ԫ�ؿ���ΪH��Ҳ����Ϊ�������
��ΪHԪ�أ�����Ԫ�ؽ��ΪHCl�����й��ۼ���
��Ϊ�����������ʧȥ���ӱ�Ϊ���ӣ�H�õ��ӱ�Ϊ�����ӣ��γ����Ӽ���
������γɹ��ۼ���Ҳ�����γ����Ӽ���
��ѡC��
���������
�����Ѷȣ�һ��
5��ѡ���� ���б仯���̷��ȵ���

A��H2O(l)��H2O(g)
B��2HI(g)��H2(g)��I2(g)+QQ����14.9 kJ/mol
C���γɻ�ѧ��ʱ���ų�����862 kJ�Ļ�ѧ��Ӧ
D�������仯����ͼ��ʾ�Ļ�ѧ��Ӧ