��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1���ƶ��� ������������ռӦ�������Ρ��������»�ѧ��Ӧ��ͼ���
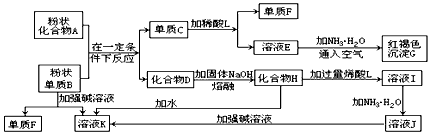
��1������F��________��
��2��д����E����G�����ӷ�Ӧ����ʽ_____________________��
��3����ҺI����������������______��
��4����C��E+F������Ũ�ᣬ����ѡ�õ�Ũ��________��
�ο��𰸣���1��H2
��2��4Fe2++8NH3��H2O+O2+2H2O==4Fe(OH)3��+8NH4+��������������Fe2++2NH3��H2O==Fe(OH)2��+
2NH4+ ��4Fe(OH)2+O2+2H2O==4Fe(OH)3����
��3��Al3+��Na+
��4��H2SO4����HNO3��
���������
�����Ѷȣ�һ��
2������� ��֪X��Y��Z��Ϊ�����г����������ʣ�WΪ���������嵥�ʣ��ס���Ϊ�������������Ϊ����ɫ���壬������Ϊ�Σ����ת����ϵ��ͼ��ʾ��

��ش�
��1����Ӧ��Ļ�ѧ����ʽΪ______����ҵ�����ô˷�Ӧԭ��������ұ���Ľ���Ϊ______����ѡ����ĸ����A��ͭB����C����D��þ
��2����Ӧ��Ļ�ѧ����ʽΪ______������5.6g����Y��ת�Ƶĵ�����ĿΪ______NA��
��3����Ӧ������ʪ��ұ��ԭ�����ڽ���Y���渽��һ���ɫ�Ľ���Z��д���÷�Ӧ�����ӷ���ʽ______�������鶡��ˮ��Һ�н��������ӣ�����еIJ���Ϊ______��
�ο��𰸣���֪X��Y��Z��Ϊ�����г����������ʣ�WΪ���������嵥�ʣ��ס���Ϊ�������������Ϊ����ɫ���壬�ж�X+��=��+Y�ƶϳ��Ʒ�Ӧ�����ȷ�Ӧ��XΪAl����ΪFe2O3����ΪAl2O3��WΪO2��YΪFe��������Ϊ��˵��Y+��=Z+����Z�dz��������ж�ΪCu����Ϊͭ�Σ���Ϊ�����Σ�
��1����Ӧ���ǵ�������������ķ�Ӧ����Ӧ����������������Ӧ�Ļ�ѧ����ʽΪ��2Al2O3�����ڣ�ͨ��.4AL+3O2������ҵ�����ô˷�Ӧԭ��������ұ���Ľ�������Ҫ���ϵ��ԭ���ĵ��Ӧ�ã�ͭ�Ʊ���Ҫ��ԭ�����õ�������ҵ��������ȷֽ�õ����ƺ�þ�ǻ��ý������������õ�����ڵ��Ȼ���õ������Է���ԭ���Ľ����Ʊ�ΪCD��
�ʴ�Ϊ��2Al2O3�����ڣ�ͨ��.4AL+3O2����CD��
��2����Ӧ�������ȷ�Ӧ�����ͺ�ɫ���������·�Ӧ������������������Ӧ�Ļ�ѧ����ʽΪ��2Al+Fe2O3����.2Fe+Al2O3������5.6g����YΪFe�����ʵ���Ϊ0.1mol����ѧ����ʽ������2molFe��ת�Ƶ���Ϊ6mol���ӣ�����0.1mol�����ɣ���Ӧת�Ƶĵ�����Ŀ0.3mol��0.3NA��
�ʴ�Ϊ��2Al+Fe2O3����.2Fe+Al2O3��0.3��
��3����Ӧ������ʪ��ұ��ԭ�����ڽ���YΪFe�����渽��һ���ɫ�Ľ���ZΪCu���÷�Ӧ�����ӷ���ʽΪ��Cu2++Fe=Fe2++Cu������ˮ��Һ�н���������Ϊ�������ӣ���������еIJ�����ȡ��������ˮ��Һ����������KSCN��Һ�������Ա仯��Ȼ���ټ���һ����������ˮ������Һ��죬˵������ˮ��Һ�е�������ΪFe2+��
�ʴ�Ϊ��Cu2++Fe=Fe2++Cu��ȡ��������ˮ��Һ����������KSCN��Һ�������Ա仯��Ȼ���ټ���һ����������ˮ������Һ��죬˵������ˮ��Һ�е�������ΪFe2+��
���������
�����Ѷȣ�һ��
3������� ��14�֣�A��J����ѧ��ѧ�г��������ʣ�����֮���ת����ϵ���¿�ͼ��ʾ�����ֲ�������ȥ������֪A��һ�ָ��۵����ʣ�J��һ�ֺ��ɫ������

��ش��������⣺
(1)A�Ļ�ѧʽΪ?��
(2)H��I��Һ��Ϻ�����Ӧ�����ӷ���ʽ��?��
G��J�Ļ�ѧ����ʽΪ?��
(3)D����ǡ������һ������ϡ������ú��ʵĻ�ѧ�����ʾ������Һ������ԭ��?��
(4) ʵ��֤�������ᷢ��������ԭ��Ӧʱ������Խϡ��Ӧ��ԭ�����е�Ԫ�صĻ��ϼ�Խ�͡�ijͬѧȡһ������C��E�Ͻ���һ�����ĺ�ϡ�������ַ�Ӧ����Ӧ������������ų����ڷ�Ӧ���������Һ�У���μ���һ��Ũ�ȵ�����������Һ�������������Ƶ����ʵ���������ij��������ʵ�����mol���Ĺ�ϵ����ͼ��ʾ���Իش��������⣺
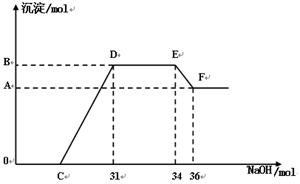
��ͼ��OC��û�г������ɣ��˽η��������ӷ���ʽΪ��_______________________________��
����DE��û�г��������ʵ���û�б仯����˽η�����Ӧ�����ӷ���ʽΪ��_________________________________��
��B���Ӧ�ij�����Ϊ________________ mol,C���Ӧ�ĺ�����Ϊ___________mol��
�ο��𰸣���1��Al2O3��2�֣�
��2��3AlO2����Al3����6H2O=4Al(OH)3��?��2�֣�4Fe(OH)2+2H2O+O2�T4Fe(OH)3?��2�֣�
��3��Fe3++3H2O  ?Fe(OH)3+3H+����д��ѧ����ʽ��2�֣�
?Fe(OH)3+3H+����д��ѧ����ʽ��2�֣�
��4����H++OH��====H2O?��2�֣�
��NH4++OH��==NH3��H2O��2�֣�?��8 ��1�֣�? 7��1�֣�
�������������������ͼ�⣬�ؼ�����ͻ�Ƶ㡣A��һ�ָ��۵����ʣ�J��һ�ֺ��ɫ����������A����������J��������������D����������C������B��������E������F���Ȼ�������G��������������H��ƫ�����ƣ�I���Ȼ�����
��1���������Ȼ�ѧʽ��Al2O3��
��2��ƫ�����ƺ��Ȼ���ˮ����ٽ�������������������Ӧ�ķ���ʽ��3AlO2����Al3����6H2O=4Al(OH)3�����������������ȶ������ױ�����������������������ʽ��4Fe(OH)2+2H2O+O2�T4Fe(OH)3 ��
��3���������������������Ȼ������Ȼ���ˮ�⣬��Һ�����ɣ�����ʽ��Fe3++3H2O  ?Fe(OH)3+3H+��
?Fe(OH)3+3H+��
��4����ͼ��OC��û�г������ɣ�˵�������ǹ����ģ����Է�Ӧ�ķ���ʽH++OH��====H2O��
����DE��û�г��������ʵ���û�б仯��˵����Һ�л�����NH4+�����Է�Ӧ�ķ���ʽ��NH4++OH��==NH3��H2O��
�۸���ͼ���֪��NH4+���ĵ�����������3mol����˷�Ӧ��ת�Ƶ��ӵ����ʵ�����24mol���ܽ������������ĵ�����������2mol�������������������ĵ�����������6mol�����Խ����������ʵ�����2mol��ʧȥ6mol���ӣ���˸��ݵ��ӵĵ�ʧ�غ��֪���������ʵ����ǣ�24mol��6mol����3��6mol������BB���Ӧ�ij�����8mol������6mol����������������������18mol������C����31mol��18mol��6mol��7mol��
�����Ѷȣ�һ��
4������� ��֪����ס�E��I��F��Ϊ�����ĵ��ʣ�����E�ڳ�����Ϊ��̬��GΪ��ɫ��״�����������ܽ������ᣬ�����ܽ�������������Һ��A�ڳ�����Ϊ��̬����������ȫ��Ӧʱ���������1:2��W�������ִ��ڲ�ͬ�����ڵ�Ԫ����ɵĻ������ˮ��Ӧ����A��Gʱ�Ļ�ѧ������֮��Ϊ1:3:3:1��������������ͼ��ʾ��ת����ϵ�����ַ�Ӧ�IJ���δȫ����ʾ�����Իش��������⣺

��1��B�ĵ���ʽΪ?�������ҵĻ�ѧʽ������?��
��2������ת���У���C��E? ��D��F? ��E��F? ��I��F? ��I��E? ��A��B ������
�û���Ӧ���ǣ�����ţ�?��
��3��д��W��ˮ��Ӧ�Ļ�ѧ����ʽ_____________________________________________,
I��NaOH��Һ��Ӧ�����ӷ���ʽ__________________________________________��
�ο��𰸣���1�� ? Fe2O3?��2���٢ۢ�
? Fe2O3?��2���٢ۢ�
��3��Al(CH3)3+3H2O=3CH4��+Al(OH)3��?Al+2OH-+2H2O=2AlO2-+3H2��
���������GΪ��ɫ��״��������Gˮ��������������ת����A�����ʿ��ƣ�A�Ǽ��飬B��CO2��C��ˮ������̼��E��������I������H��ƫ�����ƣ��ҿ�������������F����������W�����Ԫ�أ��Լ���ˮ��Ӧ����A��Gʱ�Ļ�ѧ������֮��Ϊ1:3:3:1��֪��W��Al(CH3)3+3H2O=3CH4��+Al(OH)3��
�����Ѷȣ�һ��
5���ƶ��� ��֪��A��FΪ�������ʣ�D��EΪ��̬���ʣ������Ϊ���������C����ɫ��Ӧ�ʻ�ɫ��BΪ��ɫ��ĩ��JΪ��ɫ�����������ʼ��ת����ϵ����ͼ��ʾ(��������������ȥ)��
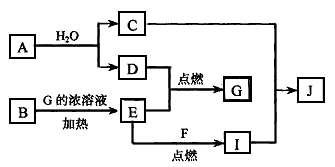
(1)A��ԭ�ӽṹʾ��ͼΪ ________________�� B�Ļ�ѧʽΪ_______________��
(2)д����ӦC+I��J�����ӷ���ʽ��________________________��
(3)д��E+F��I�Ļ�ѧ��Ӧ����ʽΪ______________��D��E�е�ȼʱ������Ϊ_________________��
�ο��𰸣���1��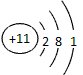 �� MnO2
�� MnO2
��2��Cu2+ + 2OH-��Cu(OH)2��
��3��Cu + Cl2 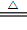 CuCl2?�� ������ɫ����
CuCl2?�� ������ɫ����
���������
�����Ѷȣ�һ��