微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列是卤素单质(F2、Cl2、Br2、I2)的沸点与相对分子质量的关系图,下列说法错误的是(? )
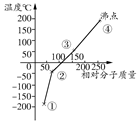
A.单质①是最活泼的非金属单质
B.单质②能使品红溶液褪色
C.单质③在常温下是液态
D.单质的氧化性强弱顺序是④>③>②>①
参考答案:D
本题解析:依据题意,按相对分子质量可以确定①为F2、②为Cl2、③为Br2、④为I2,单质的氧化性强弱顺序是①>②>③>④。
本题难度:一般
2、实验题 (16分)氯气可与潮湿的消石灰反应制取少量漂白粉,也可在浓溶液条件下与石灰石反应生成较浓的HClO溶液。
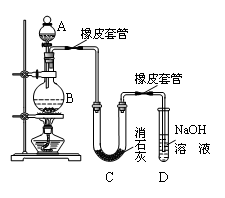
Ⅰ.甲研究性学习小组利用氯气制少量漂白粉(如图所示):
 ?
?
(1)A仪器的名称是?,所盛试剂是?。
(2)此实验结果所得Ca(ClO)2产率太低。经分析并查阅资料发现主要原因是在U型管中存在两个副反应:
①温度较高时氯气与消石灰反应生成了Ca(ClO3)2,为避免此副反应的发生,可采取的措施是?。此副反应的化学方程式为:?。
②写出另一个副反应的化学方程式?。为避免此副反应发生,可在BC之间加多一个装置,请在答题卷的方框中画出该装置,并标明所用的试剂。
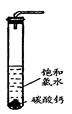
Ⅱ. 乙研究性学习小组研究饱和氯水与石灰石的反应:
①在试管中加入过量的块状碳酸钙,再加入约20mL饱和氯水(如图所示),充分反应,有少量气泡产生,溶液浅黄绿色褪去;
②过滤,将滤液滴在有色布条上,发现其比氯水的漂白性更强;
③为了确定反应产物,将滤液分为三份,分别进行以下实验:
第一份与石灰水混合,立即产生大量白色沉淀;
第二份与稀盐酸混合,立即产生大量无色气体;
将第三份加热,看到溶液变浑浊且有大量无色气体产生。 经检测,上述实验中产生的无色气体均为CO2。请回答:
(3)反应后所得的溶液漂白性增强的原因是?。
(4)依据上述实验可推知:②的滤液中的溶质除CaCl2、HClO外,还含有?。
参考答案:(1)分液漏斗; (2分)浓盐酸 (2分)
(2)将U型管置于冷水浴中(2分)? 6Cl2+6Ca(OH)2 =Ca(ClO3)2+5CaCl2+6H2O(2分)
2HCl+Ca(OH)2 =CaCl2+ 2H2O?(2分)?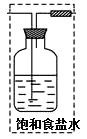 (2分)
(2分)
(3)CaCO3消耗了氯水中的 HCl, 使 Cl2+H2O HCl+HClO 平衡向右移动, HClO 浓度增大(2分)?(4)Ca(HCO3)2( 写名称正确同样得分 )(2分)
HCl+HClO 平衡向右移动, HClO 浓度增大(2分)?(4)Ca(HCO3)2( 写名称正确同样得分 )(2分)
本题解析:(1)根据仪器构造特点可知,A仪器的名称是分液漏斗,实验室制取氯气是用浓盐酸与二氧化锰,因此A中所盛试剂是浓盐酸。
(2)①温度较高时氯气与消石灰反应生成Ca(ClO3)2,根据化合价变化可知,还有氯化钙生成,因此反应的化学方程式为6Cl2+6Ca(OH)2 =Ca(ClO3)2+5CaCl2+6H2O,为避免此副反应的发生,用冰水或冷水冷却即可;?
②置中无氯气的除杂装置,挥发出的氯化氢会和氢氧化钙反应,反应的化学方程式为:2HCl+Ca(OH)2=CaCl2+2H2O;要除去氯气中的氯化氢可以将气体通过盛有饱和食盐水的洗气瓶,装置如图所示: 。
。
(3)氯水中含有盐酸和次氯酸,次氯酸与碳酸钙不反应,但盐酸与碳酸钙反应,即CaCO3消耗了氯水中的 HCl,使Cl2+H2O HCl+HClO 平衡向右移动,HClO 浓度增大,因此漂白性增强。
HCl+HClO 平衡向右移动,HClO 浓度增大,因此漂白性增强。
(4)将第三份加热,看到溶液变浑浊且有大量无色气体产生。 经检测,上述实验中产生的无色气体均为CO2,这说明反应中还有碳酸氢钙生成,Ca(HCO3)2加热分解生成碳酸钙、水和二氧化碳。
本题难度:一般
3、选择题 在标准状况下H2和Cl2的混合气体a L,经光照后完全反应,所得气体恰好能使b mol的NaOH完全转化为盐,则a、b的关系不可能是下列的(?)
A.b=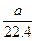
B.b>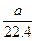
C.b≥
D.b<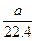
参考答案:C
本题解析:所发生的反应有:H2+Cl2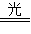 2HCl? HCl+NaOH====NaCl+H2O
2HCl? HCl+NaOH====NaCl+H2O
若Cl2过量还有:2NaOH+Cl2====NaCl+NaClO+H2O
由以上反应可知:n(NaOH)=2n(Cl2),故可用极值法求解。
若a L全为H2时,耗NaOH的物质的量为0,若a L全为Cl2时,消耗NaOH量最大: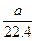 ×2 mol=
×2 mol= mol,故对二者混合气体耗NaOH量应介于0与
mol,故对二者混合气体耗NaOH量应介于0与 mol之间。
mol之间。
本题难度:简单
4、选择题 下列关于氯及其化合物说法正确的是(?)
A.漂白粉是混合物,有效成分是Ca(ClO)2
B.光照氯水有气泡逸出,该气体是Cl2
C.Cl2能使湿润的有色布条褪色,说明Cl2具有漂白性
D.实验室用二氧化锰与稀盐酸反应制取Cl2
参考答案:A
本题解析:B、气体是O2,故错;C、应是HClO具有漂白性,故错;D、应是浓盐酸,故错。故选A。
点评:本题考查了常见物质的性质,完成此题,可以依据已有的知识进行,要求同学们在平时的学习中加强基础知识的储备,以便灵活应用。
本题难度:简单
5、选择题 氯气是一种重要的工业原料。工业上利用反应在3Cl2+2NH3=N2+6HCl检查氯气管道是否漏气。下列说法正确的是(?)
A.若管道漏气遇氨就会产生白雾
B.该反应利用了Cl2的强还原性
C.该反应属于氧化还原反应
D.生成1molN2有3mol电子转移
参考答案:C
本题解析:略
本题难度:简单