微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
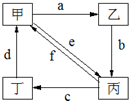
1、选择题 下表所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是( )
物质
编号 | 物质转化关系 | 甲 | 乙 | 丙 | 丁
① |
Cu
CuO
CuCl2
Cu(NO3)2
②
Na2CO3
NaOH
NaHCO3
CO2
③
(NH4)2SO3
CaSO3
SO2
NH4HSO3
④
Al(OH)3
Al2O3
Na[Al(OH)4]
AlCl3
|
A.①②③④
B.①②③
C.①③④
D.②④
参考答案:A
本题解析:
本题难度:一般
2、简答题 非金属单质A经下图所示的过程转化为含氧酸D,已知D为强酸,请回答下列问题:
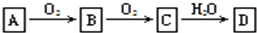
(1)若A在常温下为固体,B是能使品红溶液褪色的有刺激性气味的无色气体.
①D的化学式是______;
②在工业生产中,大量排放的B气体被雨水吸收后形成了______而污染环境.
(2)若A在常温下为气体,C是红棕色气体.
①A、C的化学式分别是:A______;C______.
②D的浓溶液在常温下可与铜反应并生成C气体,请写出该反应的化学方程式______.该反应______(填“属于”或“不属于”)氧化还原反应.
参考答案:非金属单质A,经如下图所示的过程转化为含氧酸D,D为强酸,B和C都是氧化物,则A元素为可变价元素,符合条件的元素有S、N元素,则A是氮气或硫单质,
(1)若A在常温下为固体,则A是S单质,B是能使品红溶液褪色的有刺激性气味的无色气体,则B是SO2,二氧化硫被氧化生成三氧化硫,则C是SO3,三氧化硫和水反应生成硫酸,则D是H2SO4,
①通过以上分析知,D是硫酸,其化学式为:H2SO4,
故答案为:H2SO4;
②B是二氧化硫,二氧化硫和水反应生成亚硫酸,亚硫酸不稳定易被氧化生成硫酸,硫酸溶液呈酸性,雨水中含有硫酸而形成酸雨,
故答案为:酸雨;
(2)若A在常温下为气体,C是红棕色气体,则A是N2,C是NO2,B是NO,D是HNO3,
①通过以上分析知,A、C的化学式分别是:N2、NO2,故答案为:N2;NO2;
②常温下,铜和浓硝酸反应生成硝酸铜、二氧化氮和水,反应方程式为:Cu+4HNO3(浓)=Cu(NO3)2+2H2O+2NO2↑,该反应中有电子转移,所以属于氧化还原反应,
故答案为:Cu+4HNO3(浓)=Cu(NO3)2+2H2O+2NO2↑;属于.
本题解析:
本题难度:简单
3、简答题 已知常温下E为最常见的无色无味液体,F为淡黄色粉末,G为常见的气体单质(反应条件均已省略).
请回答下列问题:
(1)请写出反应②的化学方程式______.
(2)若A为黑色固体,C、D均为气体且都能使澄清石灰水变浑浊,则A为______(写化学式);反应过程中,B表现出______性.
(3)若A为黄绿色气体,C、D均含有氯元素,且A的化合价介于C与D之间,写出稀溶液中反应①的离子方程式:______.
(4)若A与B均为固体化合物,C是一种能使红色石蕊试纸变蓝的气体,则反应①的化学方程方程式为______.实验室制取该气体常用的收集方法是______.
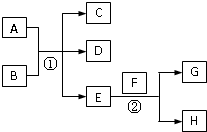
参考答案:E常温下为无色无味的液体,F为淡黄色粉末,G为常见的无色气体,则E为H2O,F为Na2O2,G为O2,
(1)反应②为过氧化钠与水的反应,其化学方程式为2Na2O2+2H2O=4NaOH+O2↑,故答案为:2Na2O2+2H2O=4NaOH+O2↑;
(2)C、D是两种均能使澄清的石灰水变浑浊的无色气体,即C、D是二氧化碳和二氧化硫,E为水,所以C、D、E是浓硫酸和碳反应的产物,反应中S元素的化合价降低,体现其氧化性,故答案为:C;氧化;
(3)若A、C、D均含氯元素,且A中氯元素的化合价介于C与D之间,则A是氯气,与碱反应,反应①生成盐酸盐、次氯酸盐和水,该离子反应为Cl2+2OH-=Cl-+ClO-+H2O,
故答案为:Cl2+2OH-=Cl-+ClO-+H2O;
(4)A与B均为固体化合物,C是一种能使红色石蕊试纸变蓝的气体,C为氨气,则反应①的化学方程方程式为2NH4Cl+Ca(OH)2△.CaCl2+2H2O+2NH3↑,氨气的密度比空气的小,常用向下排空气法收集,故答案为:2NH4Cl+Ca(OH)2△.CaCl2+2H2O+2NH3↑;向下排空气法.
本题解析:
本题难度:简单
4、判断题 (15分)物质之间的转化关系如下图,其中A、D、E、F、H为常见单质,其余为化合物,且单质E和单质F在点燃或加热的条件下生成淡黄色的固体,B常温下为液态化合物。 
试回答下列有关问题:
(1)A在元素周期表的位置?周期?族
(2)以上7个化学反应属于非氧化还原反应的是 ??(用编号①→⑦填写)
(3)写出反应①是?;
(4)写出引发反应④的实验操作 ?
写出该反应一种重要的工业用途?
(5)反应⑤的化学方程式是?。
(5)写出用A与H作电极材料插入G溶液闭合电路后的正极反应式是
?。
参考答案:(1) 四?Ⅷ(2分)?
(2) ⑦(2分)
(3) 3Fe+4H2O(g) ?Fe3O4+4H2 (3分)
?Fe3O4+4H2 (3分)
(4) 加少量KClO3,插上镁条并将其点燃(2分),
焊接钢轨(制高熔点金属)(其他合理答案也给分)(2分)
(5) 2H2O+2e-=2OH-+H2↑(3分)
本题解析:此题明显的突破口单质E和单质F在点燃或加热的条件下生成淡黄色的固体,马上知道是Na202,说明E、F一定为Na和02。结合反应②条件是高温,马上就推出,E是02,F是Na(Na活泼不需要高温)。结合由B常温下为液态化合物,推出B为是水,D为H2,G为NaOH。反应⑤与NaOH反应产生氢气的单质中学阶段只有Al和Si,结合⑥电解推出H为Al,J为Al2O3。由反应②高温条件下产生氢气体的单质有Fe和C,结合反④高温条件得到Al2O3,那只有A是Fe。验证反应⑦符合条件。写出用Fe与Al作电极材料插入电解溶液NaOH ,总方程式是:2NaOH+2Al+2H2O =2NaAlO2+3H2↑,总方程式减去负极反应式2Al+8OH--6e-=2AlO2-+4H2O即为正极反应式:6H2O+6e-=6OH-+3H2↑。
本题难度:简单
5、填空题 (14分)图中A~X分别代表一种反应物或生成物,其中F、G、X为单质,短周期元素X原予的核电荷数是其最外层和最内层电子数之和的3倍。已知A受热分解得到等物质的量的B、C、D三种气态物质,D气体能使湿润的红色石蕊试纸变蓝色,其它为化合物,图中部分生成物未列出。
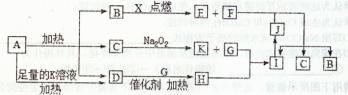
请回答:
(1)B的电子式________,写出F的一种同素异形体____,D分子的空间构型为____。?
(2)写出反应B与X反应的化学方程式________ 。
(3)写出A与足量K溶液加热时反应的离子方程式________。
(4)在一定条件下,2 L的H气体与0.5 L的G气体相混合,若该混合气体被NaOH溶液恰好完全吸收,只生成一种盐。请写出该反应过程中总的化学反应方程式:________。
(5)在F与J的反虚中当转移了1.5 mol电子时,产生标准状况下的I气体的体积为_______L。
参考答案:(14分)
(1)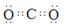 (2分);金刚石(C60、石墨等)(2分);三角锥形(2分)
(2分);金刚石(C60、石墨等)(2分);三角锥形(2分)
(2) ?(2分)
?(2分)
(3)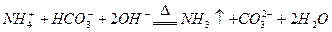 (2分)(分步写也得分)
(2分)(分步写也得分)
(4)4NO+O2+4NaOH =" 4NaNO2+2" H2O(2分)
(5)33.6 (2分)
本题解析:略
本题难度:一般