��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� �ɶ�����Ԫ����ɵ�����A-K������֮�������ͼ��ת����ϵ����ͼ�з�Ӧ������ʡ�ԣ���֪��A�dz���������B�dz����ǽ������ʣ�����Ϊ���壬����ɫ���ʺ�ɫ����ɫ��E��FΪ�������壬���ʱ��ȼ������ը��
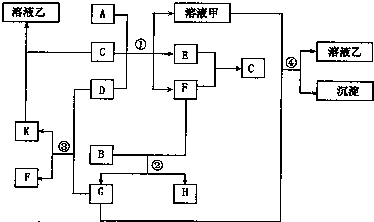
��1��д������������A��ԭ�ӽṹʾ��ͼ��______��D�ĵ���ʽ��______��K��������______��
��2��д����Ӧ�ٸ�����ǡ����ȫ��Ӧ�Ļ�ѧ����ʽ��______��
��3����Ӧ���У���B��F�����ʵ���֮��Ϊ4��3ǡ����ȫ��Ӧ�������������ʵ���֮��n��G����n��H��______��
�ο��𰸣�B�dz����ǽ������ʣ�����Ϊ���壬����ɫ���ʺ�ɫ����ɫ��E��FΪ�������壬���ʱ��ȼ������ը��ӦΪO2��H2�ķ�Ӧ����CΪH2O��A�dz�������������һ�ֹ�����ˮ�з�Ӧ����O2��H2����ù������ΪAl������DΪNa2O2������ˮ��CO2��Ӧ����GΪCO2��������K������ˮ��˵��KΪNa2CO3��FΪO2�� �����Ϣ��ɫ����B��������F����Ӧ�õ�G��CO2����˵��BΪC��̼����C��������Ӧ������CO2��CO����HΪCO������F��O2����E��Ӧ����C��ˮ����֪EΪ������
��AΪAl��BΪC��CΪH2O��DΪNa2O2��EΪH2��FΪO2��GΪCO2��HΪCO��KΪNa2CO3��
��1��AΪAl��ԭ�Ӻ�����3�����Ӳ㣬����������Ϊ3��ԭ�ӽṹʾ��ͼΪ
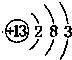
��DΪNa2O2��Ϊ���ӻ��������ʽΪ
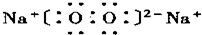
��KΪNa2CO3���׳ƴ��
�ʴ�Ϊ��
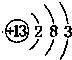
��
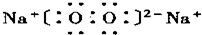
�����
��2����Ӧ��ΪAl��Na2O2��ˮ�ķ�Ӧ����ǡ����ȫ��Ӧʽ������NaAlO2��
��Ӧ�ķ���ʽΪ2Na2O2+4Al+6H2O�T4NaAlO2+6H2��+O2��
�ʴ�Ϊ��2Na2O2+4Al+6H2O�T4NaAlO2+6H2��+O2��
��3��BΪC��FΪO2�������ʵ���֮��Ϊ4��3ǡ����ȫ��Ӧ����Ӧ�Ļ�ѧ����ʽΪ��4C+3O2?��ȼ?.?2CO2+2CO�����������ʵ���֮��n��G����n��H��=1��1��
�ʴ�Ϊ��1��1��
���������
�����Ѷȣ�һ��
2������� ��15�֣������и��仯�У�EΪ��������ɫ��ζ��Һ�壬FΪ����ɫ��ĩ��GΪ��������ɫ���壨��Ӧ��������ʡ�ԣ���
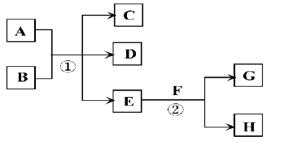
�ش��������⣺
��1��д��H�ĵ���ʽ��?
��2������Ӧ���ڼ��������½��У�AΪ���ʣ�CΪ��ɫ�д̼�����ζ�����壬DΪ��ɫ��ζ�����壬��C��D�����������ʹ�����ʯ��ˮ����ǣ���Ӧ�ٵĻ�ѧ����ʽ��?��
��ʵ����Ҫ�����C��D��E�����������������������Ⱥ�˳����?���û�ѧʽ��գ����ڼ���D����ǰ�����ȥC���壬�����Լ���?����Ӧ�����ӷ���ʽ��?��
����֪��A(s)+O2(g) =AO2(g)?��H����393.5kJ��mol-1
2A(s)+O2(g) =2AO(g)?��H����221.0kJ��mol-1
��AO��ȼ���ȵ��Ȼ�ѧ����ʽ___________________________________.
��AO2����Ȼ��ѭ��ʱ����̼��Ʒ�Ӧ��̼�����һ���������ʣ�����Ksp=2.8��10-9��CaCl2��Һ��Na2CO3��Һ��Ͽ��γ�CaCO3�������ֽ��������CaCl2��Һ��Na2CO3��Һ��ϣ���Na2CO3��Һ��Ũ��Ϊ2��10-4mol/L�������ɳ�������CaCl2��Һ����СŨ��Ϊ?��
��3������Ӧ������Һ�н��У�A��һ�ֳ���һԪǿ�B��һ����ʽ�Σ�D��һ�����壬��B�����������ʹƷ����Һ��ɫ�����壬�ڼ��������£���A����ʱ����Ӧ�ٵ����ӷ���ʽ��?��
��4������Ӧ������Һ�н��У�A��һ��ǿ�ᣬB��һ�ֺ������ֽ���Ԫ�ص��Σ���B��ˮ��Һ�Լ��ԣ�A��B���ɶ�����Ԫ����ɣ���A����ʱ��C��D��������ˮ����A����ʱ��Ӧ�ٵ����ӷ���ʽ��?��
�ο��𰸣���15�֣���1��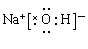 ��1�֣�
��1�֣�
��2��C��2H2SO4��Ũ��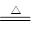 CO2����2SO2����2H2O��2�֣�
CO2����2SO2����2H2O��2�֣�
��H2O��SO2��CO2 ��1�֣�������KMnO4��Һ��1�֣���
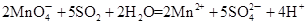 ��2�֣�
��2�֣�
��CO��g��+ 1/2 O2��g��=CO2(g)?��H=��283.0kJ��mol-1��2�֣���5.6��10-5mol/L��2�֣�
��3��2OH����NH4����HSO3��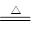 NH3����2H2O��SO32����2�֣�
NH3����2H2O��SO32����2�֣�
��4��4H����AlO2����Al3����2H2O��2�֣�
�������������������ͼ�⣬�ؼ�����ͻ�Ƶ㡣
��1��EΪ��������ɫ��ζ��Һ�壬FΪ����ɫ��ĩ������E��ˮ��Fˮ�������ơ���Gˮ������H���������ƣ������ʽ��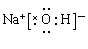 ��
��
��2���������ʵ����ʿ��жϣ�C��SO2��D��CO2������A��̼��B��Ũ���ᣬ��˷�Ӧ�ٵķ���ʽΪC��2H2SO4��Ũ��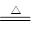 CO2����2SO2����2H2O��
CO2����2SO2����2H2O��
�ټ���CO2�ó����ʯ��ˮ��SO2��Ʒ����Һ���飬ˮ��������ˮ����ͭ���顣������SO2Ҳ��ʹ�����ʯ��ˮ��Ӧ����ͨ����Һʱ�����ˮ�������������ȼ������ˮ�����������SO2�������CO2��SO2���л�ԭ�ԣ��������Ը��������Һ��������ȥSO2������ʽΪ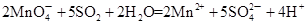 ��
��
��ȼ������ָ��һ�������£�1mol��ȼ����ȫȼ�������ȶ���������ʱ���ų������������Ը��ݸ�˹���ɿ�֪��COȼ���ȵ��Ȼ�ѧ����ʽΪCO��g��+ 1/2 O2��g��=CO2(g)?��H=��283.0kJ��mol-1��
�������ɳ�������CaCl2��Һ����СŨ��Ϊx�����Ϻ�CO32����Ca2����Ũ�ȷֱ���1��10-4mol/L��0.5x�����Ը����ܶȻ�������֪1��10-4��0.5x��2.8��10-9�����x��5.6��10-5mol/L��
��3������B�����ʿ�֪��B�����������Ρ�����D��һ�����壬����B����������泥���˷���ʽΪ2OH����NH4����HSO3��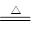 NH3����2H2O��SO32����
NH3����2H2O��SO32����
��4��B��һ�ֺ������ֽ���Ԫ�ص��Σ���B��ˮ��Һ�Լ��ԣ���˵��B��ƫ�����ƣ����Է�Ӧ�ķ���ʽΪ4H����AlO2����Al3����2H2O.
�����Ѷȣ�һ��
3������� ��A��B��C��D��E������������ɾ�����Ԫ�أ��ҵ�������Ϊ10����A��˫ԭ�ӵ������ӣ�����֮���ܷ������б仯��
��1��A+B
C+D����2��C+C
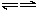
A+E��3��D+E��B+C
�ɴ˿�֪���ǵĻ�ѧʽ�ֱ�Ϊ��
A______��B______��C______��D______��E______��
�ο��𰸣���������Ϊ10�����ӵ����У����ӣ�CH4��NH3��H2O��HF��Ne�������ӣ�N3-��O2-��F-��OH-��NH2-�������ӣ�Na+��Mg2+��Al3+��NH4+��H3O+��
�������⣬A��˫ԭ�ӵ������ӣ�ȷ��AΪOH-����Ӧ��1��A+B��
���������
�����Ѷȣ�һ��
4������� ��9�֣��ɶ�����Ԫ����ɵ�X��Y��Z��M����ѧ��ѧ�������������ʣ���������ͼ��ʾ��ת����ϵ�����������ش����⡣
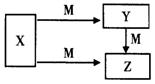
��1����X��Y��Z����ͬ�ֳ�������Ԫ�أ�M��O2��XΪ___________��Z��������һ�������»�������һ�ֲ��д���÷�Ӧ�Ļ�ѧ����ʽ________��
��2����X��Y��Z����ͬ�ֳ����ǽ���Ԫ�أ�����Z��ʹƷ����Һ��ɫ��
��X�ĵ���ʽΪ__________________ _______��
_______��
��Z�����������������Һ��Ӧ�����ӷ���ʽ�ǣ�_____________________________��
��3����X��ˮ��Һ�Լ��ԣ�X��M ��Ϊ���壬����ת�����̾���ˮ��Һ�н��С���дһ����������ת������Y��Z��Ӧ�Ļ�ѧ����ʽ______________________��
��Ϊ���壬����ת�����̾���ˮ��Һ�н��С���дһ����������ת������Y��Z��Ӧ�Ļ�ѧ����ʽ______________________��
�ο��𰸣���9�֣�
��1��Na���ƣ���1�֣�? Na2O2+H2=2NaOH��2�֣�
��2���� ��2�֣�?��SO2+2OH-=SO32-+H2O��2�֣�
��2�֣�?��SO2+2OH-=SO32-+H2O��2�֣�
��3��(NH4)2CO3+CO2+H2O=2NH4HCO3��(NH4)2S+H2S =2NH4HS
(NH4)2SO3+SO2+H2O=2NH4HSO3��2�֣�
�����������
�����Ѷȣ�һ��
5������� ��13�֣��ס��ҡ���Ϊ�����ڳ����ĵ��ʣ��ҡ�����Ԫ�ص�ԭ���������8��X��A��B��C��D��E��F��G��Ϊ�����Ļ��������A��G����ɫ��ӦΪ��ɫ��A��X��Ħ��������ͬ����һ�������£��������ת����ϵ����ͼ��
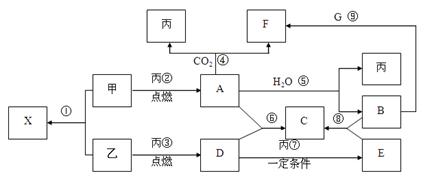
��ش�
(1) д��ѧʽ��X?��C?D?��
(2)д����Ӧ�ܡ��ݵĻ�ѧ��Ӧ����ʽ����?��
��?
��3��д����Ӧ�ࡢ������ӷ���ʽ��?
��?��
��4������ͼ�ķ�Ӧ�У�������������ԭ��Ӧ���ǣ�����ţ�?��
�ο��𰸣�����13�֣�(1) Na2S?��1�֣� Na2SO4��1�֣� SO2��1�֣�
(2) ��2Na2O2 + 2H2O ??4NaOH + O2����2�֣�
��2Na2O2 + 2CO2??2Na2CO3 + O2��2�֣�
��3���� SO3+2OH-??SO42��+ H2O?��2�֣�
�� HCO3�� + OH��??CO32�� + H2O ��2�֣�
(4) ��ᣨ2�֣�
����������ס��Ҿ��ɺͱ���Ӧ������Ϊ��ȼ����֪��ΪO2����Oԭ���������8����Ԫ�ر�ΪS��
��ȼ�����ɵ�AΪ���������CO2��Ӧ����O2������֪AΪNa2O2����Ϊ�ƣ�
Na2O2��SO2�ɷ���������ԭ��Ӧ����Na2SO4��
�����Ѷȣ�һ��