| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学知识点归纳《原电池原理》试题强化练习(2017年最新版)(八)
(4)燃料电池是一种高效、环境友好的供电装置,如图是甲烷燃料电池原理示意图,回答下列问题: 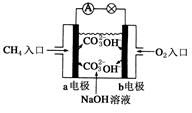 ①电池的负极是__________(填“a”或“b”),该极的电极反应式是:________________。 ②电池工作一段时间后电解质溶液的pH_________(填“增大”、“减小”或“不变”)。 参考答案:(16分) 本题解析: 本题难度:一般 2、选择题 氢氧燃料电池是一种高效、环境友好的发电装置,它是以铂作电极,KOH溶液作电解液,总反应为:2H2 + O2 = 2H2O,正极反应为:O2 + 2H2O + 4e- = 4OH-,下列叙述不正确的是 |
参考答案:C
本题解析:正极反应:O2 + 2H2O + 4e- = 4OH- 负极反应:2H2 + 4OH- - 4e- = 4H2O
原电池中,负极失电子,被氧化,正极得电子,被还原
本题难度:一般
3、选择题 将锌片和铜片用导线连接置于同一稀硫酸中,下列叙述正确的是
A.锌片是正极
B.电流方向从锌片流向铜片
C.氢气在锌片上产生
D.若锌片、铜片同时有气泡冒出,则说明锌片不纯
参考答案:D
本题解析:考查原电池
相对活泼的锌极为负极,失电子,电子经导线流向正极铜,电流方向是从铜片至锌片,氢离子在正极得电子生成氢气,排除ABC,答案为D:若锌片不纯,则可在锌片上形成微电池,也可产生气泡
本题难度:一般
4、填空题 根据可逆反应: +2I-+2H+
+2I-+2H+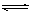
 +I2+H2O,设计如下图所示实验装置。B烧杯中装有Na3AsO4和Na3AsO3溶液,A烧杯中装有I2和KI溶液。两烧杯中用一倒置的装有饱和KI溶液的U型管相连,该装置称为盐桥,其作用是避免两烧杯中的溶液相混合,又能使两烧杯中的溶液因相连通而导电。C1、C2棒为惰性电极。进行如下操作:
+I2+H2O,设计如下图所示实验装置。B烧杯中装有Na3AsO4和Na3AsO3溶液,A烧杯中装有I2和KI溶液。两烧杯中用一倒置的装有饱和KI溶液的U型管相连,该装置称为盐桥,其作用是避免两烧杯中的溶液相混合,又能使两烧杯中的溶液因相连通而导电。C1、C2棒为惰性电极。进行如下操作: 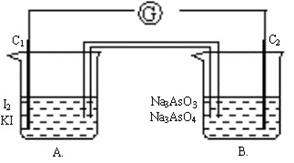
①向A溶液中逐滴加入浓HCl,发现电流计指针发生偏转;
②若改向B溶液中滴加40%的 NaOH溶液,发现电流计指针向相反方向偏转。
试回答以下问题:
(1)两次操作中,可以观察到电流计指针偏转方向相反,为什么?试用化学平衡原理解释之 ;
(2)操作①过程中,C1棒上发生的电极反应式为: ,操作②过程中C2棒上发生的电极反应式为: 。
参考答案:
(1)操作①使平衡正向移动,C1作负极;操作②使平衡逆向移动,C2作负极。故两次电流方向相反(答案合理即可给分)。
(2)2I- ― 2e- = I2 ; AsO33- + 2 OH- ― 2e- = AsO43- + H2O 。
本题解析:由图可知,该装置为原电池,(Ⅰ)发生AsO43-+2I-+2H+?AsO33-+I2+H2O,C1棒为负极,电极反应发生2I--2e-=I2;
(Ⅱ)发生AsO33-+I2+2OH-?AsO43-+2I-+H2O,C2棒为负极,电子由负极流向正极,
(1)因两次操作过程均能形成原电池,都是把化学能转化为电能,形成电流指针偏转,)但是操作①使平衡正向移动,C1作负极;操作②使平衡逆向移动,C2作负极。故两次电流方向相反
(2)操作①过程中,C1棒为负极,电极反应发生2I--2e-=I2;
操作②过程中C2棒为负极,电极反应为AsO33- + 2 OH- ― 2e- = AsO43- + H2O
考点:考查电解池和原电池
本题难度:一般
5、选择题 将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是( )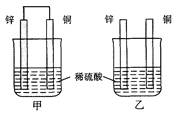
A.两烧杯中铜片表面均无气泡产生
B.甲中铜片是正极,乙中铜片是负极
C.产生气泡的速度甲比乙快
D.两烧杯中溶液的pH均减小
参考答案:C
本题解析:试题分析:根据装置的特点可知,甲是原电池,锌比铜活泼,属于锌是负极,失去电子。铜是正极,溶液中的氢离子得到电子,放出氢气。乙装置中不能构成原电池,锌和稀硫酸直接发生置换反应生成硫酸锌和氢气。据此可知选项C是正确的,其余选项都是错误的,答案选C。
考点:考查原电池的有关判断和应用
点评:该题是基础性试题的考查,主要是考查学生对原电池原理的熟悉了解程度,旨在巩固学生的基础,提高学生灵活运用基础知识解决实际问题的能力,有利于培养学生的逻辑推理能力和发散思维能力。
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学知识点整理《醇》高频考.. | |