微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在标准状况下,一个装满氧气的容器质量为74g,若装满氮气时质量是66g,此容器的体积是(?)
A.4.48L
B.11.2L
C.22.4L
D.44.8L
参考答案:D
本题解析:假设气体的物质的量为nmol,容器的质量为mg,则:
mg+nmol×32g/mol=74g
mg+nmol×28g/mol=66g
联立方程,解得n=2mol
气体的体积为V=mol×22.4L/mol=44.8L.
所以容器的容积为44.8L.
点评:本题考查阿伏伽德罗定律及推论,难度不大,氯气的体积等于氮气体积等于容器的体积,是解题的关键。
本题难度:一般
2、简答题 欲配制500ml?0.2mol/L的碳酸钠溶液,回答下列问题:
(1)通过计算可知,应称取______?g十水合碳酸钠晶体
(2)配制该溶液所用的仪器有______
(3)若砝码和药品位置放颠倒(假设称量时未用烧杯)天平平衡时,实际称得碳酸钠晶体的质量是______.
(4)下列操作使所配溶液浓度偏高的是______
A.称取28.6g?Na2CO3进行配制
B.称量时用了生锈的砝码
C.往容量瓶转移溶液时,有少量液体飞溅
D.未洗涤溶解碳酸钠的烧杯
E.定容时,仰视刻度线
F.容量瓶未干燥即用来配制溶液.
参考答案:(1)需十水合碳酸钠的质量为m=0.5L×0.2mol?L-1×286g/mol=28.6g.
故答案为:28.6.
(2)操作步骤有计算、称量、溶解、移液、洗涤移液、定容、摇匀等操作,一般用托盘天平称量,用药匙取用药品,在烧杯中溶解(可用量筒量取水加入烧杯),并用玻璃棒搅拌,加速溶解.冷却后转移到500mL容量瓶中,并用玻璃棒引流,洗涤烧杯、玻璃棒2-3次,并将洗涤液移入容量瓶中,加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,最后定容颠倒摇匀.所以所需仪器有托盘天平、烧杯、玻璃棒、500mL容量瓶、胶头滴管、药匙.
故答案为:托盘天平、烧杯、玻璃棒、500mL容量瓶、胶头滴管、药匙.
(3)天平平衡原理为左盘内质量=右盘内质量+游码数值,所以实际称得碳酸钠晶体的质量为28g-0.6g=27.4g.
故答案为:27.4g.
(4)A.称取28.6gNa2CO3进行配制,碳酸钠的质量增大,所配溶液浓度偏高;
B.称量时用了生锈的砝码,砝码质量增大,所称碳酸钠晶体质量增大,所配溶液浓度偏高;
C.往容量瓶转移溶液时,有少量液体飞溅,移入容量瓶中的碳酸钠的质量减小,所配溶液浓度偏高;
D.未洗涤烧杯、玻璃棒,少量碳酸钠沾在烧杯壁与玻璃棒上,碳酸钠的实际质量减小,溶液浓度偏低;
E.定容时,仰视刻度线,导致溶液体积增大,所配溶液浓度偏低;
F.最后需要定容,容量瓶不干燥,含有少量蒸馏水,对溶液浓度无影响.
故选:ABC.
本题解析:
本题难度:一般
3、选择题 2008年9月13日中央电视台报导了三鹿某奶粉中三聚氰胺超标使全国1200多名婴幼儿患上肾结石的“三鹿奶粉重大安全事故”。三聚氰胺是一种纯白色晶体,其化学式为C3H6N6(其相对分子质量是126)。下列关于三聚氰胺的叙述正确的是
[? ]
A.三聚氰胺的摩尔质量为126 g
B.标准状况下1mol三聚氰胺的体积约为22.4 L
C.1 mol三聚氰胺含15 NA个原子
D.63g三聚氰胺含3 g H2分子
参考答案:C
本题解析:
本题难度:简单
4、选择题 在一定条件下,使CO和O2的混合气体26 g充分反应,所得混合物在常温下跟足量的Na2O2固体反应,结果固体增重14 g,则原混合气体中O2和CO的质量比可能是(?)?
A.9∶4
B.1∶1
C.7∶6
D.6∶7
参考答案:D
本题解析:由反应2Na2O2+2CO2=2Na2CO3+O2,可知混合物在常温下跟足量的Na2O2固体反应生成固体为Na2CO3,1molNa2O2生成1molNa2CO3,质量增加28g,恰好为CO的质量,固体增重14g,说明混合气体中CO为14g,则O2为26g-14g=12g,所以原混合气体中O2和CO的质量比为
12g:14g=6:7,,故本题的答案选择D。
点评:本题考查了混合物的相关计算,该题需要一定的观察能力,本题难度中等。
本题难度:简单
5、填空题 (4分)现有m g某气体,它由四原子分子构成,它的摩尔质量为M g/mol.则:
(1)该气体的物质的量为________mol。
(2)该气体中所含的原子总数约为 个。
(3)该气体在标准状况下的体积为________L。
(4)该气体溶于水后形成V L溶液,其溶液的物质的量浓度为________mol/L。
参考答案:(每空1分,共4分) (1) 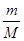 (2)
(2) 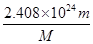 (3)
(3) 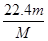 (4)
(4) 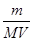
本题解析:考查物质的量的有关计算。
(1)根据n=m/M可知,该气体的物质的量为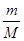 mol。
mol。
(2)该气体是由4个原子构成的,所以该气体中所含的原子总数约为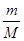 mol× 4×6.02×1023/mol=
mol× 4×6.02×1023/mol=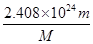 个。
个。
(3)根据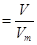 可知,该气体在标准状况下的体积为
可知,该气体在标准状况下的体积为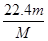 L。
L。
(4)根据c=n/V可知,该气体溶于水后形成V L溶液,其溶液的物质的量浓度为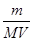 mol/L。
mol/L。
本题难度:一般