��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� 2014��ȫ�˻��������ٰ죬�俪Ļʽ����һ�����ʢ�硣
��1����������˲��ֽ���Ԫ��������________��Ӧ���÷�Ӧ����________�����������ѧ�����仯��
��2����ͼ��ʾ����Ԫ������A��B��C��D��E���ֻ����ԲȦ���沿��ָ���ֻ����ﺬ��һ����ͬԪ�أ����ֻ����������ֶ�����Ԫ����ɣ�ÿ�ֻ������������Ԫ�ء�
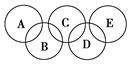
ͼ��A����������Ҫ�ɷ֣�B��E������������������Ϊ18��B���ȶ������н�ǿ�������ԣ���ϡ��Һ��ҽ���Ϲ㷺ʹ�õ���������E���ӽṹ�����ģ��Ϊ ��C�봿���ڸ����µķ�Ӧ�ǹ�ҵ�Ʋ�������Ҫ��Ӧ֮һ��D����������Ԫ�ص�ԭ�Ӹ�����Ϊ3��4����������֮��Ϊ3��2������������Ϣ�ش��������⣺
��C�봿���ڸ����µķ�Ӧ�ǹ�ҵ�Ʋ�������Ҫ��Ӧ֮һ��D����������Ԫ�ص�ԭ�Ӹ�����Ϊ3��4����������֮��Ϊ3��2������������Ϣ�ش��������⣺
��B��ˮ��Һ�������ԣ�����Ҫ�ĵ��뷽��ʽ�ɱ�ʾΪ________________��D�Ļ�ѧʽ��________��
��A��B��E�о����е�һ��Ԫ�ط���Ϊ________��
��C�봿�Ӧ�Ļ�ѧ����ʽΪ____________________________________��
��Һ̬B��Һ̬E��Ӧ������һ�ֵ��ʺ�һ�ֳ���Һ�壬1 mol B�μӷ�Ӧ�ų�����Q kJ���䷴Ӧ���Ȼ�ѧ����ʽΪ________________________��
�ο��𰸣���1����ɫ������?��2����H2O2?HO��H����Si3N4����H
��SiO2��Na2CO3Na2SiO3��CO2��
��N2H4��l����2H2O2��l��=N2��g����4H2O��l������H����2Q kJ��mol��1
����������������⣬AΪCH4��BΪH2O2��CΪSiO2����E���ӽṹ�����ģ�ͺ�N��HԪ�صļۼ�����֪��������ʾNԭ�ӣ�С�����ʾHԭ�ӣ���EΪN2H4��D������Si��N����Ԫ�أ���ԭ�Ӹ�����Ϊ3��4����������֮��Ϊ3��2���ʻ�ѧʽΪSi3N4��
�����Ѷȣ�һ��
2������� A��B��C����������Ԫ����ɵ�������Ǻ͵��ʼס��ҡ���������ͼ��ʾ��ת����ϵ��ת�����̶�����Ҫʹ�ô�������
����������⣺

��1�������dz������������dz����ǽ������嵥�ʣ�A��C�ڳ����¾�Ϊ��ɫ���壬��A��B��C���ס��ҡ������ɶ�����Ԫ����ɣ���B�ĵ���ʽ��______��A���Ӧ�Ļ�ѧ����ʽ��______��
��2������ͼ��ʾ�ķ�Ӧ��ˮ��Һ�н��У����ڳ�����Ϊ��ɫ���壬���ڳ�����ΪҺ�壬���������г����Ľ�������
�ٱ���C��Ӧ�����ӷ���ʽΪ______��
����A��Һ����μ���NaOH��Һʱ���ܳ��ֵ�������______��
�ο��𰸣��ɿ�ͼ��֪������A+���ʼ�����B+������Ϊ�û���Ӧ����Ϊ������AΪ��ɫ��������ɻ�����A��һ��Ԫ��Ϊ�ɱ��̬�������ƶϼ�ΪMg��AΪCO2��������Һ�з�������Ϊ��۽����������Ƴ���������Fe����Ϊ��ɫ���壬��ΪCl2���ɲ�ȡ���뷨���飮�������ڳ�������Һ�壬������һ����Һ�壮
��1�������dz������������dz����ǽ������嵥�ʣ�A��C�ڳ����¾�Ϊ��ɫ���壬��A��B��C���ס��ҡ������ɶ�����Ԫ����ɣ��ƶϳ���ΪMg����ΪC����ΪO2��AΪCO2��BΪMgO��CΪCO��B�ĵ���ʽΪ��
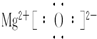
��A���Ӧ�Ļ�ѧ����ʽ��2Mg+CO2?��ȼ?.?2MgO+C��
�ʴ�Ϊ��
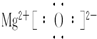
��2Mg+CO2?��ȼ?.?2MgO+C��
��2������ͼ��ʾ�ķ�Ӧ��ˮ��Һ�н��У����ڳ�����Ϊ��ɫ���壬���ڳ�����ΪҺ�壬���������г����Ľ��������ΪCl2��������ΪBr2����ΪFe��AΪFeBr2��BΪFeCl3��CΪFeBr3��
�ٱ�Fe��CFeBr3��Ӧ�����ӷ���ʽΪFe+2Fe3+�T3Fe2+���ʴ�Ϊ��Fe+2Fe3+�T3Fe2+��
����A��FeBr2����Һ����μ���NaOH��Һʱ���ܳ��ֵ����������ɰ�ɫ������Ѹ�ٱ�ɻ���ɫ������ɺ��ɫ���ʴ�Ϊ�����ɰ�ɫ������Ѹ�ٱ�ɻ���ɫ������ɺ��ɫ��
���������
�����Ѷȣ�һ��
3���ƶ��� ����A��B��C�ڳ����¾�Ϊ��̬���ֱ��ɼס��ҡ������ֶ�����Ԫ����ɣ���֪��Ԫ�ص�ԭ�ӽṹ�д�����������������������1��������D�ڳ����³�Һ̬��G�dz����Ľ������ʣ�H�dz�������ɫ�����������ʼ��ת����ϵ��ͼ��ʾ(��Ӧ������������ȥ)

��ش�
(1)?�ڷ�Ӧ���У���֪1?g?B��ȫȼ������Һ̬Dʱ���ų�142.9?kJ�����������ʾB��ȼ���ȵ��Ȼ�ѧ����ʽ��____________________________________________��
(2)��Ӧ��Ҳ������Ƴ�ԭ���װ�ý��У����ò����缫����KOH��Һ���������Һʱ�������ĵ缫��Ӧʽ��_______________________________________________��
(3)?��Ӧ�ۢ���ͨ������²����Է����У���ͼ�е�����a��________����ʹ��Ӧ�ۢ��ܹ�������װ���У���һ���缫���ϱ�����ͬ��д���õ缫��Ӧʽ___________��
(4)?��Ӧ�����ӷ���ʽ��_______________________________________________��
(5)?�ס�����Ԫ�س��γɻ�����D�⣬�����γ�һ�ֺ���4��ԭ�Ӻ˺�18�����ӵĻ�����û�����ĵ���ʽ��________��
�ο��𰸣�(1)H2(g)��1/2O2(g)===H2O(l)?��H����285.8 kJ/mol
(2)2H2��4e����4OH��===4H2O
(3)ͨ��(����)��Cu��2e��===Cu2��
(4)Cu(OH)2��2H��===Cu2����2H2O
(5) 
���������
�����Ѷȣ�һ��
4������� ����ӵ�صĹ㷺Ӧ��ʹ��������﮻�Դ��Ϊ��Ҫ���⣺ij�о���ѧϰС��ԷϾ�����ӵ���������ϣ�LiMn2O4��̼�۵�Ϳ���������ϣ�������Դ�����о������ʵ����������?

��1���ڢڲ���Ӧ�õ��ij���X�Ļ�ѧʽΪ______��
��2���ڢ۲���Ӧ�����ӷ���ʽ��______��
��3���ڢܲ���Ӧ����Li2CO3����IJ���������______��������ʱ������Һ�����������ǣ���ʵ������ĽǶȸ������ֿ��ܵ�ԭ��______��______��
��4�����Ͼ�����ӵ���������Ϻ�LiNB2O4������Ϊ18.1g�ڢ۲���Ӧ�м���20.0mL3.0mol?L-1��H2SO4��Һ�������������е�﮾���Ӧ�ۺ͢���ȫΪLi2CO3��ʣ������______Na2CO3�μ��˷�Ӧ��
�ο��𰸣���һ���������ܽ�������������Һ�У�ע��LiMn2O4������ˮ���������ǻ��������ƣ�����Һ����Ҫ�ɷ֣��ڶ����������ǻ����������������̼��Ӧ������������������̼�����ƵĹ��̣���������LiMn2O4�����Ի������ܱ������е���������������������ԭ��Ӧ���õ�����Һ�������ɵ�����ﮣ������й��������ᣬ���һ������̼����֮�����õ���Һ��Ҫ�ɷ�Ϊ�����ƣ�
��1�����ǻ��������������������̼��Ӧ�ò�����Al��OH��3������̼�����ƣ��ʴ�Ϊ��Al��OH��3��
��2�������Ի����£�LiMn2O4�ܱ������е��������������ӷ���ʽΪ��4?LiMn2O4+O2+4H+=4Li++8MnO2+2H2O���ʴ�Ϊ��4?LiMn2O4+O2+4H+=4Li++8MnO2+2H2O��
��3���������ò��������У�©�������������ձ�������ʱ������Һ�����������ǣ�ԭ������У���ֽ������Һ������ֽ��Ե�ȣ��ʴ�Ϊ��©�������������ձ�����ֽ������Һ������ֽ��Ե
��4������LiMn2O4��0.5H2SO4��Li+��18.1gLiMn2O4��0.1molLiMn2O4�����������Ϊ0.05mol����������ʣ�࣬ʣ�����������ɵ�Li+������̼����0.05mol����5.3g���ʴ�Ϊ��5.3g��
���������
�����Ѷȣ�һ��
5������� ��֪������A��B���Ԫ����ͬ���ڳ����¾���Һ̬��D��E��Ϊ�������ʣ���D��E���Ũ��Һ�ڳ������ö��� 91ExAm.org����������ʱ�д�������ɫ���������E��D��������ķ�Ӧ�����ں��Ӹֹ죮
��1��A�ĽṹʽΪ______��˵��A��ҽ���е�һ����Ҫ����______��
��2��д������D���ϡ��Һ��Ӧ�����ӷ���ʽ��______��
��3����D��EΪ�缫��NaOH��ҺΪ�������Һ�������ԭ��أ�ԭ��ظ����ĵ缫��ӦʽΪ______�������ô�װ�õ��CuSO4��Һ�����һ��ʱ����������������������ڱ�״���¶���2.24L����д�������ĵ缫��Ӧʽ______�������ǰCuSO4��Һ�����Ϊ200mL���������ʵ���Ũ����______��
��4������D��EԪ�ص�һ���������߷��Ӳ��ϸ�Ч��ˮ��[ED��OH��4Cl2]m�����Ũ������Һ���Է�Ӧ���䷴Ӧ�Ļ�ѧ����ʽΪ______��
�ο��𰸣�������A��B���Ԫ����ͬ���ڳ����¾���Һ̬��ΪH2O��H2O2��
D��E��Ϊ�������ʣ�E��D��������ķ�Ӧ�����ں��Ӹֹ죬Ϊ���ȷ�Ӧ��EΪAl��DΪFe��Fe��Al���Ũ��Һ�ڳ������ö�������������ʱ�д�������ɫ�����������ΪHNO3��
��1��A��ҽ��������Ҫ���ã���֪AΪH2O2��BΪH2O��H2O2�ǹ��ۻ������������ԭ��֮���γ�1�Թ��õ��Ӷԣ���ԭ������ԭ��֮���γ�1�Թ��õ��Ӷԣ��ṹʽΪH-O-O-H����ҽ���г�����ɱ��������
�ʴ�Ϊ��H-O-O-H��ɱ��������
��2��������Fe��ϡ���ᷴӦ��������������NO��ˮ����Ӧ���ӷ���ʽΪ3Fe+8H++2NO3-=3Fe2++2NO��+4H2O��
�ʴ�Ϊ��3Fe+8H++2NO3-=3Fe2++2NO��+4H2O��
��3����������������Һ��Ӧ������Ϊ������Al�ŵ磬�ڼ�������������ƫ�������ˮ��
�缫��ӦʽΪAl+4OH--3e-=AlO2-+2H2O��
���CuSO4��Һ�����������������ӷŵ磬����������ˮ����ⷴӦʽΪ��4OH--4e-=O2��+2H2O��
����������2.24L�������������ڱ�״�������������ʵ���Ϊ2.24L22.4L/mol=0.1mol������������2.24L�������������ڱ�״�������������ʵ���ΪΪ2.24L22.4L/mol=0.1mol����ԭ��Һ��Cu2+Ϊamol�����ݵ���ת���غ��У�2��amol+0.1mol��2=0.1mol��4�����a=0.1����CuSO4��Һ�����ʵ���Ũ��Ϊ0.1mol0.2L=0.5mol/L��
�ʴ�Ϊ��Al+4OH--3e-=AlO2-+2H2O��4OH--4e-=O2��+2H2O��0.5mol/L��
��4����ˮ��[AlFe��OH��4Cl2]m�����Ũ������Һ��Ӧ�����Ȼ������Ȼ�����ˮ����Ӧ����ʽΪ��[AlFe��OH��4Cl2]m+4mHCl=mAlCl3+mFeCl3+4mH2O��
�ʴ�Ϊ��[AlFe��OH��4Cl2]m+4mHCl=mAlCl3+mFeCl3+4mH2O��
���������
�����Ѷȣ�һ��