微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (9分)现有A、B、C三种均含同一种元素的无机物,它们之间的转化关系如下图所示(部分产物已略去):
 ?
?
(1)若A、D为非金属单质:
①当M(A)>M(D)时,D为:?;
②当M(D)>M( A)时,A为:?;
A)时,A为:?;
(2)若A为非金属单质,D为金属单质时,A为:?;
(3)若D为非金属单质,A、B、C为卤化物时,写出①的化学反应方程式:?。
参考答案:(1)①D:C (2分);②A:C (2分)(2)A:Cl2 (2分)(3)A:FeI2 +Cl2=FeCl2 +I2 (3分)
本题解析:略
本题难度:简单
2、简答题 锂离子电池的广泛应用使回收利用锂货源成为重要课题:某研究性学习小组对废旧锂离子电池正极材料(LiMn2O4、碳粉等涂覆在铝箔上)进行资源回收研究,设计实验流程如下?

(1)第②步反应得到的沉淀X的化学式为______.
(2)第③步反应的离子方程式是______.
(3)第④步反应后,过滤Li2CO3所需的玻璃仪器有______.若过滤时发现滤液中有少量浑浊,从实验操作的角度给出两种可能的原因:______、______.
(4)若废旧锂离子电池正极材料含LiNB2O4的质量为18.1g第③步反应中加入20.0mL3.0mol?L-1的H2SO4溶液.定正极材料中的锂经反应③和④完全为Li2CO3,剩至少有______Na2CO3参加了反应.
参考答案:第一步就是铝溶解在氢氧化钠溶液中(注意LiMn2O4不溶于水)生成四羟基合铝酸钠,即滤液的主要成分,第二步就是四羟基合铝酸钠与二氧化碳反应生成氢氧化铝沉淀和碳酸氢钠的过程,第三步是LiMn2O4在酸性环境下能被空气中的氧气氧化发生的氧化还原反应,得到的滤液中有生成的硫酸锂,可能有过量的硫酸,最后一步加入碳酸钠之后所得的滤液主要成分为硫酸钠;
(1)四羟基合铝酸钠与过量二氧化碳反应得产物是Al(OH)3沉淀和碳酸氢钠,故答案为:Al(OH)3;
(2)在酸性环境下,LiMn2O4能被空气中的氧气氧化,离子方程式为:4?LiMn2O4+O2+4H+=4Li++8MnO2+2H2O,故答案为:4?LiMn2O4+O2+4H+=4Li++8MnO2+2H2O;
(3)过滤所用玻璃仪器有:漏斗、玻璃棒、烧杯;过滤时发现滤液中有少量浑浊,原因可能有:滤纸破损、滤液超过滤纸边缘等,故答案为:漏斗、玻璃棒、烧杯;滤纸破损、滤液超过滤纸边缘
(4)根据LiMn2O4~0.5H2SO4~Li+得18.1gLiMn2O4即0.1molLiMn2O4消耗硫酸的量为0.05mol,故硫酸有剩余,剩余的硫酸和生成的Li+共消耗碳酸钠0.05mol,即5.3g,故答案为:5.3g.
本题解析:
本题难度:一般
3、填空题 (7分)已知:①x是短周期元素组成的单质,Z是一种常见化合物。②A、B、C、D、E、F都是常见的化合物,常温下C是气体,D是液体。A溶液的焰色反应为黄色。自然界中存在较多的E矿石,工业生产中常用这种矿石来制取F。③存在下列转化关系:

试回答:
(1)Y的电子式:?,X元素在周期表中的位置
C分子中的化学键类型 ?
(2)Y转化为Z的化学方程式: ?
A转化为E的离子方程式(Z过量):
参考答案:(7分)(1)Ca2+ 2- 第二周期、IVA族 共价键
2- 第二周期、IVA族 共价键
(2) CaC2+2H2O=Ca(OH)2+C2H2↑? HCO3-+Ca2++OH-=CaCO3↓+H2O
本题解析:略
本题难度:一般
4、填空题 在一定条件下,下列各物质(均为中学化学常见物质,其中A是淡黄色固体.)可发生如下图所示的变化(反应中生成的水未写出):

请回答下列问题:
(1)固体A是______(填化学式),A中含有的化学键为______(填化学键类型).
(2)反应(Ⅰ)的离子方程式为______;反应(Ⅱ)的化学方程式为______.
(3)H与液体X反应的化学方程式为______;固体B与溶液L反应的离子方程式为______.
参考答案:A是淡黄色固体,应为Na2O2,能与水反应,则X为H2O,则C为NaOH,D为O2,气体F能与O2和溴水反应,则说明气体F具有还原性,则F应为SO2,H为SO3,NaOH与SO2过量反应生成NaHSO3,则B为NaHSO3,G为NaBr,E为H2SO4,L为HBr,则
(1)A为Na2O2,为离子化合物,含有离子键和共价键,故答案为:Na2O2;离子键和共价键;
(2)反应(Ⅰ)为NaOH与SO2过量反应生成NaHSO3,反应的离子方程式为OH-+SO2 =HSO3-,
反应(Ⅱ)为SO2与溴水的反应,生成HBr和H2SO4,反应的化学方程式为SO2+Br2+2H2O=H2SO4+2HBr,
故答案为:OH-+SO2 =HSO3-;SO2+Br2+2H2O=H2SO4+2HBr;
(3)H为SO3,与水反应生成H2SO4,反应的化学方程式为SO3+H2O=H2SO4,
B为NaHSO3,L为HBr,反应生成SO2,反应的离子方程式为HSO3-+H+=SO2↑+H2O,
故答案为:SO3+H2O=H2SO4;HSO3-+H+=SO2↑+H2O.
本题解析:
本题难度:一般
5、选择题 化合物A、B、C、D各由两种元素组成,甲、乙、丙是前两周期元素的三种单质。这些常见的化合物与单质之间存在如下关系(已知C是一种有机物),以下结论不正确的是(?)
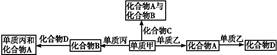
A.甲、乙、丙三种单质均为气态非金属单质
B.上述转化关系所涉及的化合物中有一种是电解质
C.上图所示的五个转化关系中,有三个是化合反应
D.上图所示的五个转化关系中,均为氧化还原反应
参考答案:A
本题解析:根据甲(单质) 化合物A和B,据题意可推知甲为O2,C为烃,化合物A和B为CO2和H2O中的一种。再根据甲(O2)
化合物A和B,据题意可推知甲为O2,C为烃,化合物A和B为CO2和H2O中的一种。再根据甲(O2) 化合物A
化合物A 化合物D,可推知A为CO2,单质乙为C,D为CO,故化合物B为H2O,单质丙为H2。题中的单质C是固态非金属单质,故A错误;题中所涉及的化合物中H2O是电解质,其余是非电解质,B正确;题中的五个转化关系所涉及的反应方程式分别为CxHy+(x+
化合物D,可推知A为CO2,单质乙为C,D为CO,故化合物B为H2O,单质丙为H2。题中的单质C是固态非金属单质,故A错误;题中所涉及的化合物中H2O是电解质,其余是非电解质,B正确;题中的五个转化关系所涉及的反应方程式分别为CxHy+(x+ )O2
)O2 xCO2+
xCO2+ H2O,
H2O,
O2+C CO2,CO2+C
CO2,CO2+C 2CO,2H2+O2
2CO,2H2+O2 2H2O,H2O+CO
2H2O,H2O+CO CO2+H2,故C、D正确。
CO2+H2,故C、D正确。
本题难度:一般