微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下表列出短周期8种元素的部分性质,有关叙述不正确的是 (? )
原子
| ①
| ②
| ③
| ④
| ⑤
| ⑥
| ⑦
| ⑧
|
原子半径
(10-10m)
| 0.74
| 1.52
| 1.60
| 1.10
| 0.99
| 0.75
| 1.86
| 0.82
|
最高价/
最低价
| -2
| +1
| +2
| +5
-3
| +7
-1
| +5
-3
| +1
| +3
|
?
A.②号元素原子半径小于⑦号元素的原子半径
B.④号元素原子序数大于⑥号元素的原子序数
C.②号元素和③号元素处在同一周期
D.⑤号元素最高价氧化物对应的水化物的酸性比其他7种元素的最高价氧化物对应的水化物的酸性都强
参考答案:C
本题解析:②号与⑦号元素都是碱金属元素,②在⑦上边,②号元素的原子半径小,A正确;④号与⑥号元素都是第ⅤA族元素,⑥在④上边,⑥号元素原子序数小,B正确;②号与③号元素若在同一周期,则②号元素原子半径应该大于③号元素原子半径,C错;⑤号元素最高价氧化物对应的水化物是HClO4。
本题难度:一般
2、填空题 (9分)、(1)下表是部分短周期元素的原子半径及主要化合价
元素代号
| L
| M
| Q
| R
| T
|
原子半径/nm
| 0.160
| 0.143
| 0.112
| 0.104
| 0.066
|
主要化合价
| +2
| +3[
| +2
| +6、-2
| -2
|
①L元素的名称是______,R元素的名称是______。
②能与T元素组成的化合物具有两性的是________________(写化学式)。?
(2)某种融雪剂主要成分为XY2,X、Y均为周期表中前20号元素,其阳离子和阴离子的电子层结构相同,且1molXY2含有54mol电子。
①该融雪剂主要成分的化学式为__________;X与氢元素形成的化合物的电子式为____________________。
②元素D、E原子的最外层电子数是相应原子电子层数的2倍,D与Y相邻,D元素是______,E元素是______。
参考答案:(1)①镁;硫(2分)?②BeO、Al2O3(2分)
(2)①CaCl2(1分);[H:]-Ca2+[:H]-(2分)②S(或硫);C(或碳)(2分)
本题解析:(1)根据元素的主要化合价和原子半径可知,L是Mg,M是Al,Q是Be,R是S,T是O。铍和铝处于对角线上,所以性质是相似的。
(2)1molXY2含有54mol电子,且阳离子和阴离子的电子层结构相同,所以离子的所带电子是18,即X是Ca,Y是Cl。钙是活泼的金属,和氢可以形成离子化合物氢化钙,电子式为[H:]-Ca2+[:H]-。最外层电子数是相应原子电子层数的2倍,则可以是C或S。又因为D与Y相邻,是由D是S,E是C。
本题难度:一般
3、选择题 硒(Se)是人体必需的微量元素,它的一种同位素是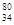 Se。下列有关该同位素的说法正确的是(?)
Se。下列有关该同位素的说法正确的是(?)
A.质子数为80
B.电子数为114
C.中子数为46
D.质量数为34
参考答案:C
本题解析:考查原子的组成及表示方法。在表示原子组成时元素符号的左下角表示质子数,左上角表示质量数。因为质子数和中子数之和是质量数,所以中子数是80-34=46。又因为电子数等于质子数,所以选项C是正确的,答案选C。
本题难度:简单
4、填空题 (6分)A、B、C都是短周期元素,原子序数的相对大小为A<B<C,A、B同主族,B、C可形成共价化合物BC4,试回答:
(1)写出BC4的电子式?。
(2)这三种元素对应氢化物的稳定性由强 到弱的顺序是?。(用氢化物的化学式表示)
(3)BC4不稳定,遇水易生成B的含氧酸及C的氢化物,近代海战中常采用喷BC4和液氨的方法形成烟幕,有关化学反应的方程式为?。
参考答案:(1) SiCl4
(2)HCl>CH4>SiH4(3)SiCl4+4H2O====4HCl+HH4SIO4,? NH3+HCl=NH4Cl
本题解析:【分析预测及备考建议】由周期表中“位―构―性”的关系进行推断是高考常考题型,复习中要牢记周期表中的三角关系,并在练习中进行迁移运用,可提高这类题的解决能力。
【答题技巧】由BC4化学式可知其中B元素显+4价,C显-1价,且A、B同族B原子序数大于A,所以可知B为Si,A为C,则C为Cl。(1)SiCl4是一个共价化合物,形成的是共用电子对。(2)据同周期、同主族元素非金属性的变化规律可知,非金属性Cl>C>Si,所以可得稳定性HCl>CH4>SiH4?。由于该物质水解时生成HCl气体,形成白雾,同时喷入NH3时会与HCl反应而生成NH4Cl,从而形成白烟。这样可以形成一道烟幕,起到伪装作用。
本题难度:一般
5、选择题 已知质量数为A的某阳离子Rn+,核外有X个电子,则核内中子数为
A.A-x
B.A-x-n
C.A-x+n
D.A+x-n
参考答案:B
本题解析:中子数+质子数=质量数,所以中子数=质量数―质子数。而现在质量数给我们了是A, 质子数是计算出来就可以,原子质子数=电子数,该阳离子核外有X个电子,也就是R原子失去n个电子之后剩下了x个电子,所以R原子核外有X+n个电子,
所以中子数=A--(X+n)个中子
本题难度:一般