��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �������з�������NaCl������K2CO3������ǣ�������
A����ϡ����
B����NaOH��Һ
C����ɫ��Ӧ
D������
�ο��𰸣�A�������ᷴӦ���������ΪK2CO3���壬NaCl�������Ӧ������ͬ�����Լ��𣬹�Aѡ��
B��������NaOH��Һ������Ӧ��������ͬ�����ܼ��𣬹�B��ѡ��
C���Ƶ���ɫΪ��ɫ���ص���ɫΪ��ɫ�����Լ��𣬹�Cѡ��
D���������Ⱦ����ֽ⣬������ͬ�����ܼ��𣬹�D��ѡ��
��ѡAC��
���������
�����Ѷȣ���
2��ʵ���� �ں�����ߺ�DZˮͧ�п��ù���������Ϊ����������ѡ���ʵ��Ļ�ѧ�Լ���ʵ����Ʒ������ͼ�е�ʵ��װ�ý���ʵ�飬֤���������ƿ�����������
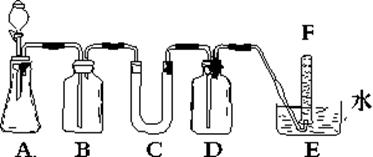
��1�����Ӻ�װ�ú���ҩƷǰӦ���е�ʵ������ǣ�
?
?
?
?
?
��2��A����ʯ��ʯ��������ȡCO2��װ�á�д��A�з�����Ӧ�����ӷ���
ʽ��?��
(3)��B��Cװ���з����ҩƷ����Ϊ��B??C��?
��4��D�з�������������Һ�������ǣ�?
(5)�Թ�F���ռ����������һ��ʵ������ǣ���E�еĵ����Ƴ�ˮ�棬�رշ�Һ©����������Ĵָ��ס�Թܿڣ�ȡ���Թܣ������Ѵ����ǵ�ľ�������Թܿ��ڣ�ľ����ȼ��֤���Թ����ռ���������������
�ο��𰸣���1��?�رշ�Һ©����������E�������ܽ���ˮ�У�����ƿ�������ܿ�������ð��������ȴ�����γ�һ���ȶ���ˮ�����������Ժá�?
��2��д���ӷ���ʽ�� CaCO3? +? 2H+ ="?" Ca2+?+? CO2�� +? H2O?��
(3)B?����NaHCO3��Һ??C��? Na2O2?
��4��?��ȥδ��Ӧ���CO2����?
�����������
�����Ѷȣ���
3��ʵ���� ������ͼ��ʾװ�ã�β�����������ԣ�����ȡһ����̼�������Բⶨijͭ����Ʒ������CuO��ĩ���н���ͭ�ĺ���

��1���Ʊ�һ����̼�Ļ�ѧ����ʽ����?����
��2�������У��۲쵽��Ӧ���з�������������?����β������Ҫ�ɷ�����?����
��3����Ӧ��ɺ���ȷ�IJ���˳��Ϊ��?��������ĸ��
a���ر�©������? b��Ϩ��ƾ�1? c��Ϩ��ƾ���2
��4���������г�ȡͭ����Ʒ5.0g����ַ�Ӧ��Ӧ����ʣ����������Ϊ4.8g����ԭ��Ʒ�е���ͭ����������Ϊ��?����
��5����Ũ���ᡢŨ���ᡢ����ˮ��˫��ˮ��ѡ�ú��ʵ��Լ������һ���ⶨ��Ʒ�н���ͭ���������ķ�����
����Ʒ�������Ҫ�����ǣ����������������̵�ϸ�ڣ���?����
��д���йط�Ӧ�Ļ�ѧ����ʽ��?����
�ο��𰸣���1��HCOOH CO��+H2O��2����Ʒ�ɺ�ɫ���ɫ��CO��CO2��3��cab��4��80%��5����Ũ����������ˮϡ�ͣ�����Ʒ��ϡ�����ַ�Ӧ���ˣ��������ʣ�����ͭ���������ɣ�CuO+H2SO4=CuSO4+H2O
CO��+H2O��2����Ʒ�ɺ�ɫ���ɫ��CO��CO2��3��cab��4��80%��5����Ũ����������ˮϡ�ͣ�����Ʒ��ϡ�����ַ�Ӧ���ˣ��������ʣ�����ͭ���������ɣ�CuO+H2SO4=CuSO4+H2O
�����������1��������Ũ���ᡢ���ȵ������·ֽ�����CO��H2O��
��2��ʵ���У���Ӧ���з�����ӦCuO+CO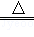 Cu+CO2����Ӧ���з����������Ǻ�ɫ��ĩ��죻β������Ҫ�ɷ���CO��CO2��
Cu+CO2����Ӧ���з����������Ǻ�ɫ��ĩ��죻β������Ҫ�ɷ���CO��CO2��
��3��ʵ�鲽�裺��ͨ��COһ������ȴ���Ӧ���ڵ�ҩƷ��ȫ��ֹͣ���ȣ�Ȼ�����ͨ��CO����������ȴΪֹ��
��4���������г�ȡͭ����Ʒ5.0g����ַ�Ӧ��Ӧ����ʣ����������Ϊ4.8g��ʣ�����ȫ��Ϊͭ�����ò����������ԭ��Ʒ������ͭ����������������ͭ������������
��5����Ҫ�ⶨͭ����������������Ũ����ϡ�ͣ�ͭ��ϡ�����Ӧ������ͭ��ϡ���ᷴӦ���������ͭ��������������Ʒ�������Ҫ�����ǽ�Ũ����������ˮϡ�ͣ�����Ʒ��ϡ�����ַ�Ӧ���ˣ��������ʣ�����ͭ���������ɣ��ڷ�Ӧ�Ļ�ѧ����ʽΪCuO+H2SO4=CuSO4+H2O��
�⣺��1��������Ũ���ᡢ���ȵ������·ֽ�����CO��H2O����Ӧ����ʽΪHCOOH CO��+H2O��
CO��+H2O��
�ʴ�Ϊ��HCOOH CO��+H2O��
CO��+H2O��
��2��ʵ���У���Ӧ���з�����ӦCuO+CO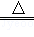 Cu+CO2����Ӧ���з����������Ǻ�ɫ��ĩ��죻β������Ҫ�ɷ���CO��CO2��
Cu+CO2����Ӧ���з����������Ǻ�ɫ��ĩ��죻β������Ҫ�ɷ���CO��CO2��
�ʴ�Ϊ����Ʒ�ɺ�ɫ���ɫ��CO��CO2��
��3����Ӧ�����˳���ȳ��ƾ���2����ʱ���װ��������ȡCO��Ȼ���ٹرշ�Һ©���Ŀ��أ����ټ��뷴Ӧ�Լ�����ƾ���1ֹͣ��Ӧ������������ֹ������O2�����ұ�װ��ͭ�ֱ�����Ϊ����ͭ�ˣ���ȷ�IJ���˳��Ϊ��Ϩ��ƾ���2���ر�©�����أ����Ϩ��ƾ�1����cab��
�ʴ�Ϊ��cab��
��4���������г�ȡͭ����Ʒ5.0g����ַ�Ӧ��Ӧ����ʣ����������Ϊ4.8g��ʣ�����ȫ��Ϊͭ������Ʒ��CuO������Ϊm����
CuO+CO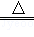 Cu+CO2�������������١�m
Cu+CO2�������������١�m
80? 16
m? 5g��4.8g=0.2g
��m=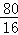 ��0.2g=1g��
��0.2g=1g��
����ԭ��Ʒ�н���ͭ����������Ϊ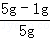 ��100%=80%��
��100%=80%��
�ʴ�Ϊ��80%��
��5����Ҫ�ⶨͭ����������������Ũ����ϡ�ͣ�ͭ��ϡ�����Ӧ������ͭ��ϡ���ᷴӦ���������ͭ��������������Ʒ�������Ҫ�����ǽ�Ũ����������ˮϡ�ͣ�����Ʒ��ϡ�����ַ�Ӧ���ˣ��������ʣ�����ͭ���������ɣ�
�ʴ�Ϊ����Ũ����������ˮϡ�ͣ�����Ʒ��ϡ�����ַ�Ӧ���ˣ��������ʣ�����ͭ���������ɣ�
�ڷ�Ӧ�Ļ�ѧ����ʽΪCuO+H2SO4=CuSO4+H2O��
�ʴ�Ϊ��CuO+H2SO4=CuSO4+H2O��
���������⿼��ѧ����ʵ��ԭ����ʵ����������⡢ʵ�鷽����ơ�Ԫ�ػ��������ʡ���ѧ����ȣ��Ѷ��еȣ����ʵ��ԭ���ǽ���Ĺؼ�����Ҫѧ���߱���ʵ�Ļ���֪ʶ���ۺ�����֪ʶ�������⡢��������������
�����Ѷȣ�һ��
4������� ��֪FeSO4�ڲ�ͬ�����·ֽ�õ��IJ��ﲻͬ��������FeO��SO3��Ҳ������Fe2O3��SO3��SO2��ij�о�С��̽���ھƾ���Ƽ���������FeSO4�ֽ����������֪SO3���۵���16.8�棬�е���44.8�档

��1��װ�â���Թ��в�װ�κ��Լ�����������_______________________���Թܽ�����50���ˮԡ�У�Ŀ����________________________________��
��2��װ�â��װ�â���������̽����ʵ���������ɷ֡������ʵ����ƣ���д�����Լ���Ԥ����������ۡ�
��ѡ�Լ���3 mol��L��1 H2SO4��6 mol��L��1 NaOH��0.5 mol��L��1 BaCl2��0.5 mol��L��1 Ba(NO3)2��0.01 mol��L��1����KMnO4��Һ��0.01 mol��L��1��ˮ��
�����Լ�
| Ԥ������ͽ���
|
װ�â���Թ��м���________________��
| ����������ɫ������֤����������к���SO3��
|
װ�â����Թ��м���________________��
| ______________________________
______________________________
______________________________
______________________________
|
��3��װ�â��������Ƿ�ֹβ����Ⱦ�������ձ���Ӧ������Լ���?��
�ο��𰸣���1����ֹ��Һ������װ�â�2�֣�?��ֹSO3Һ�������̣�2�֣�
��2����10�֣�
�����Լ�
Ԥ������ͽ���
װ�â���Թ���װ��BaCl2��Һ��
����������ɫ������֤����������к���SO3��
װ�â����Թ���װ������KMnO4��Һ��
����Һ��ɫ��ȥ��֤����������к���SO2��
����Һ��ɫ�����Ա仯��֤����������в���SO2��
��
�����Լ�
Ԥ������ͽ���
װ�â���Թ���װ��BaCl2��Һ��
����������ɫ������֤����������к���SO3��
װ�â����Թ���װ����ˮ��
����ˮ��ɫ��ȥ��֤����������к���SO2��
����ˮ��ɫ�����Ա仯��֤����������в���SO2��
��3��NaOH��Һ?��2�֣�
�����������
�����Ѷȣ�һ��
5������� ����ǻ�ѧѧϰ�г��õķ���֮һ����֪�����ܰ��������� Fe ( NO3)3��������������ʱ�������� Fe ( NO3 ) 2��ijͬѧ�ܴ����������һ�����ƵĹ۵㣺���������۷�Ӧ���� C12����ʱ���� FeC13 , �����۹���ʱ������ FeCl2��Ϊ��֤�ù۵��Ƿ���ȷ����ͬѧ��һ��ϸ�Ĵ���˿�ֱ��������������� C12�е�ȼ��ȡ����������ﲢ�ֱ���Ϊ A��B ��Ȼ��ͨ��ʵ��ȷ����ɷ֡�̽���������£�
( 1 ��������裺 A �� FeCl3, B �� FeCl 2��
( 2 �����ʵ�鷽�����ֱ�ȡ A��B ����Һ����������ʵ�飬��ʵ��������ͬ������д�±��е���Ӧ�ո�

( 3 ����������ʵ����ۣ�д�� C12�����ۼ���ʱ������Ӧ�Ļ�ѧ����ʽ��
_________________________________________________________________��
( 4 ��Ϊ��һ��̽�� FeC13��Һ�����ʣ��������� A ��Һ��������һЩʵ�飬�������Դ������____________________��
A���� A ��Һ�����ˮ�У����������ȵõ����ɫҺ�壬��Һ���ܲ������������
B���� A ��Һ�м����������ۣ������ܽ⣬��Һ��ɫ����
C���� A ��Һ�еμ� Na OH Ũ��Һ�����ֺ��ɫ����
D���� A ��Һ�������ɲ����գ��õ� FeC13����
( 5 ��ʵ��Ӧ�ã�
FeCl3��Һ����ӡˢ��·ͭ�帯ʴ������ʴ��ķ�Һ�к��� FeC13��FeCl2��CuCl2��ij�о���ѧϰС���ͬѧ����������ִӷ�Һ�л��� Cu�ķ�����
����1�����Һ�м��˹��������ۣ���ַ�Ӧ���ˡ������������м������������ᣬ��ַ����ٹ��˼��õ�ͭ������1 ���漰�����������ӵ���������ǿ������˳��Ϊ��
_____________________________________��
����2 ���ڷ�Һ�м������������������Һ�� pH =" 1" ����ͭ��ʯī���缫���е�⡣���۲쵽���������������ݲ���ʱ����ֹͣ��⣬��ʱҪ���յ� Cu ��ȫ������������ 2 ��ͭ��_________�����������ĵ缫��ӦΪ�����ж���缫��Ӧ���밴�շ�Ӧ�������Ⱥ�˳��ȫ��д����___________________________________________________
���� 2 �ڵ缫��ֱ�ӻ���ͭ�������ϱȷ��� 1 ��㣬������ 2 Ҳ�в���֮������Ҫ����Ϊ��_____________________________________________________��
�ο��𰸣���2����Һ���ɫ��1�֣� FeCl2 ( 1 �֣� ( 3 ) 2Feʮ3Cl2 2FeCl3 ( l �֣�
2FeCl3 ( l �֣�
( 4 ) BD (2�֣� ( 5 ������ 1 : Fe3+ ��Cu2+ > H + > Fe2+ ( l �֣�
���� 2 ������ l �֣�2Fe 3+��2eһ��2Fe2+ ;
Cu2+ + 2eһ��Cu ( l �֣�;
2H + + 2eһ��H2���� ( l �֣�
����Ⱦ������ C12������ l �֣���ʹ���˵��װ�ã��ɱ��ϸߵȡ��� l �֣�
���������Fe3+��SCNһ���ɫ�� Fe2+��ʹ KMnO4��Һ��ɫ�� FeC13��Һ�������ۣ�����������ԭΪ����������ɫ��dz�� FeC13��Һ�����������õ����������������� ( 5 �����Һ�м��˹��������ۣ��������Ⱥ����������ӷ�Ӧ������ת��Ϊ���������ӣ�Ȼ���ͭ���ӷ�Ӧ���ټ������ᣬ������������۷�Ӧ���ɶ��������ӣ��ɴ�֪�������ӵ���������ǿ������˳��ΪFe3+ ��Cu2+ > H+ ��Fe2+������ 2 ����ͭ���������缫�ϵķ�ӦΪ2Fe3+��2eһ��2Fe2+��Ȼ�� Cu2+��2eһ��Cu , 2H+ʮ2eһ��H 2�� , ����֮�������������������Ⱦ�������Ĵ����ĵ��ܵȡ�
�����Ѷȣ�һ��