��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� �о�NO2��SO2��CO�ȴ�����Ⱦ����Ĵ�������Ҫ���壮
��1��NO2����ˮ���գ���Ӧ�Ļ�ѧ����ʽΪ______�����÷�Ӧ
6NO2+8NH3
7N2+12H2OҲ���Դ���NO2����ת��1.2mol����ʱ�����ĵ�NO2�ڱ�״������______L��
��2����֪��2SO2��g��+O2��g��?2SO3��g����H=-196.6kJ?mol-1
2NO��g��+O2��g��?2NO2��g����H=-113.0kJ?mol-1
��ӦNO2��g��+SO2��g��?SO3��g��+NO��g���ġ�H=______kJ?mol-1
һ�������£����������1��2�����ܱ������з���������Ӧ��������˵����ӳ�ﵽƽ��״̬����______��
a����ϵѹǿ���ֲ���
b�����������ɫ���ֲ���
c��SO3��NO������ȱ��ֲ���
d��ÿ����1molSO3��ͬʱ����1molNO2
���������Ӧƽ��ʱ��NO2��SO2�����Ϊ1��6����ƽ�ⳣ��K=______��
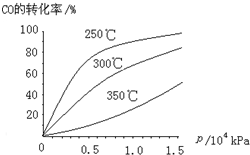
��3��CO�����ںϳɼ״�����Ӧ����ʽΪCO��g��+2H2��g��?CH3OH��g����CO�ڲ�ͬ�¶��µ�ƽ��ת������ѹǿ�Ĺ�ϵ��ͼ��ʾ���÷�Ӧ��H______0���������������ʵ����������������250�桢1.3��104kPa���ң�ѡ���ѹǿ��������______��
�ο��𰸣���1��NO2��H2O��Ӧ�ķ���ʽΪ��3NO2+H2O�T2HNO3+NO��6NO2+8NH3�T7N2+12H2O������Ӧ����1 mol NO2�μӷ�Ӧʱ����ת����4 mol���ӣ���ת��1.2mol����ʱ�����ĵ�NO2Ϊ1.2��4��22.4L=6.72L��
��2�����ݸ�˹���ɣ����ڶ�������ʽ�ߵ����������һ������ʽ��ӵã�2NO2+2SO2�T2SO3+2NO����H=-83.6 kJ?mol-1����NO2+SO2?SO3+NO����H=-41.8 kJ?mol-1������Ӧ�Ƿ�Ӧǰ���������������ķ�Ӧ������ϵ��ѹǿ���ֲ��䣬��a����˵����Ӧ�Ѵﵽƽ��״̬�����ŷ�Ӧ�Ľ��У�NO2��Ũ�ȼ�С����ɫ��dz����b����˵����Ӧ�Ѵ�ƽ�⣻SO3��NO�����������������1��1����c������Ϊƽ��״̬���ж����ݣ�d���������������ʶ����淴Ӧ���ʣ�������Ϊƽ��״̬���ж����ݣ�
NO2��g��+SO2��g�� SO3��g��+NO��g��
SO3��g��+NO��g��
��ʼ���ʵ���� 1a 2a 0 0
ת�����ʵ���� x x x x
ƽ�����ʵ���� 1a-x 2a-xxx
��1a-x������2a-x��=1��6����x=45a����ƽ�ⳣ��Ϊ=x2/��1a-x����2a-x��=8/3��
��3����ͼ��֪���¶����ߣ�CO��ת���ʽ��ͣ�ƽ�����淴Ӧ�����ƶ������淴Ӧ�����ȷ�Ӧ������Ӧ�Ƿ��ȷ�Ӧ����H��0��ѹǿ�������ڼӿ췴Ӧ���ʣ�������ʹƽ�������ƶ�����ѹǿ������Ҫ�Ķ������豸��Ҫ��Ҳ�ߣ���ѡ��250�桢1.3��104kPa���ҵ���������Ϊ��250�桢ѹǿΪ1.3��104 kPaʱ��CO��ת�����ѽϴ�������ѹǿ��CO��ת���ʱ仯����û�б�Ҫ������ѹǿ��
�ʴ�Ϊ����1��3NO2+H2O=2HNO3+NO��6.72
��2��-41.8��b��2.67��8/3
��3��������1.3��104kPa�£�CO��ת�����ѽϸߣ�������ѹǿCO��ת������߲��������ɱ����ӵò���ʧ��
���������
�����Ѷȣ�һ��
2�������� ��һ�ܱյ�2L������װ��4molSO2��2molO2����һ�������¿�ʼ��Ӧ��2minĩ�����������1.6mol SO2 ��
������2minĩSO3��Ũ�ȣ�
��2min��O2��ƽ����Ӧ���ʡ�
�ο��𰸣�(10�֣�ÿ��5��) �� 1.2mol/L?�� 0.3mol/(L��min)
���������? 2SO2��O2 2SO3
2SO3
��ʼŨ�ȣ�mol/L��? 2? 1? 0
ת��Ũ�ȣ�mol/L�� 1.2? 0.6? 1.2
2min��Ũ�ȣ�mol/L��0.8? 0.4? 1.2
����2minĩSO3��Ũ����1.2mol/L
2min��O2��ƽ����Ӧ������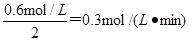
�����������Ǹ߿��еij������ͣ������е��Ѷȵ����⡣���������ǿ�����ض�ѧ����������������������������ѧ���Ĺ淶�������������ѧ��������û���֪ʶ���ʵ�����������������������Ҫע������ڽ��п��淴Ӧ���йؼ���ʱ��һ����á�����ʽ�����У����ֱ��г���ʼ����ת������ƽ������ij��̵�����Ȼ��������֪������ʽ���㼴�ɡ�
�����Ѷȣ���
3��ѡ���� ���й��ڻ�ѧ��Ӧ�ȵ�˵����ȷ���ǣ�������
A����һ�����淴Ӧ�ﵽƽ��״̬ʱ������������Ӧ���ܴﵽ����
B����һ�����淴Ӧ���е�ƽ��״̬ʱ�������Ӧ������Ӧ���ʺ�����Ӧ�������
C��ƽ��״̬��һ�־�ֹ��״̬����Ϊ��Ӧ����������Ũ���Ѿ����ٸı�
D����ѧ��Ӧ���Ȳ�����ͨ���ı��������ı�
�ο��𰸣�A����ͬ����������Ӧ��ͬ�ķ�Ӧ�ȣ�Ӧ�ü���һ��ǰ�ᣬ�ڸ������£���Ҫ������ͬ�¶ȡ�ѹǿ�£�����A����
B������Ӧ�ﵽ��ѧƽ��״̬ʱ�����淴Ӧ������ȣ������ʵ�Ũ�Ȳ��ٸı䣬��B��ȷ��
C����ѧƽ��״̬����������ĸı���ı䣬Ϊ��̬ƽ�⣬���Ǿ�ֹ��״̬����C����
D����һ�������£���һ�����淴Ӧ�ﵽƽ��״̬ʱ������������Ӧ���ܴﵽ���ȣ���ͬ����������Ӧ��ͬ�ķ�Ӧ�ȣ���D����
��ѡB��
���������
�����Ѷȣ���
4������� ��һ�������£���ӦA(��)��B(��) ?C(��)?������ӦΪ���ȷ�Ӧ���ﵽƽ���������ͼ���жϣ�
?C(��)?������ӦΪ���ȷ�Ӧ���ﵽƽ���������ͼ���жϣ�
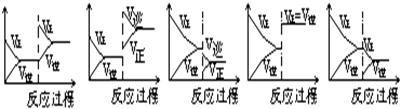
A��
B��
C��
D��E��