��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��11�֣���֪N2O4 (g)  ?2NO2 (g)?��H<0��
?2NO2 (g)?��H<0��
��1���ֽ�1 mol N2O4 ����һ��ѹ�ܱ������У�����ʾ��ͼ��ȷ����˵����Ӧ�ﵽƽ��״̬����________��

��2��������ͬ�¶��£�������Ӧ�������Ϊ1L�ĺ����ܱ������н��У�ƽ�ⳣ��________������������䡱��С�� ������Ӧ3s��NO2�����ʵ���Ϊ0.6mol����0~3s�ڵ�ƽ����Ӧ����v��N2O4��=________mol��L-1��S-1��
��3��NO2���ð�ˮ��������NH4NO3��25��ʱ����amol NH4NO3����ˮ����Һ�����ԣ�ԭ����?�������ӷ���ʽ��ʾ���������Һ�μ�bL��ˮ����Һ�����ԣ���μӰ�ˮ�Ĺ����е�ˮ�ĵ���ƽ�⽫______������������������ƶ���
�ο��𰸣���2�֣���1��a��d
(4��)(2)����? 0.1mol��L-1��s-1
(5��)(3)NH4++H2O NH3��H2O+H+?����
NH3��H2O+H+?����
�����������1����ѧ��Ӧƽ����жϿɴ����¼����濼�ǣ���ϵ�����з�Ӧ������������������Ũ�ȣ����ֲ��䣬����Ӧ���ʵ����淴Ӧ���ʡ�����N2O4 (g)  ?2NO2 (g)����Ӧ��������a�ܶȲ��䣬˵��������䣬��ƽ�⣻b��H=E��-E������H����ʱ��ı仯���������Ż�ѧ�������ı仯���仯��c��ѧƽ��Ӧ�������淴Ӧ������ȣ���ͼ�б�ʾ�Ķ�������Ӧ���ʣ�dN2O4��ת���ʲ��䣬Ҳ˵���˻�ѧ��Ӧ�ﵽƽ�⡣
?2NO2 (g)����Ӧ��������a�ܶȲ��䣬˵��������䣬��ƽ�⣻b��H=E��-E������H����ʱ��ı仯���������Ż�ѧ�������ı仯���仯��c��ѧƽ��Ӧ�������淴Ӧ������ȣ���ͼ�б�ʾ�Ķ�������Ӧ���ʣ�dN2O4��ת���ʲ��䣬Ҳ˵���˻�ѧ��Ӧ�ﵽƽ�⡣
��2����ѧƽ�ⳣ��ֻ���¶ȵĺ��������¶Ȳ��䣬ƽ�ⳣ���Ͳ��䡣
N2O4 (g)  ?2NO2 (g)
?2NO2 (g)
nǰ?1?0
n��?0.3 ?0.6
n��?0.7? 0.6
V��N2O4��=0.3molL_1/3s=0.1molL_1/s
(3)NH4NO3��ǿ�������Σ���ˮ��Һ笠���ˮ�⣬ʹ��Һ�����ԣ�����ʽΪNH4++H2O NH3��H2O+H+����ˮ���������������ˮ�ĵ��룬��ˮ�ĵ���ƽ�⽫������С�
NH3��H2O+H+����ˮ���������������ˮ�ĵ��룬��ˮ�ĵ���ƽ�⽫������С�
���������⿼���˻�ѧ��Ӧƽ����жϣ�Ҳ�����˻�ѧƽ�ⳣ����֪ʶ�͵���ˮ��֪ʶ��Ҫ�μ������ˮ��ٽ�ˮ�ĵ��룬��������ĵ�������ˮ�ĵ��롣
�����Ѷȣ�һ��
2������� �״���һ�ֿ�������Դ�����й㷺�Ŀ�����Ӧ��ǰ����
��1����ҵ��һ��������ַ����Ʊ��״���
��Ӧ��CO(g) + 2H2 (g)  CH3OH (g)?DH1
CH3OH (g)?DH1
��Ӧ��CO2(g)+ 3H2(g)? ?CH3OH (g)+H2O(g)?DH2
?CH3OH (g)+H2O(g)?DH2
�� �±����������Ƿ�Ӧ���ڲ�ͬ�¶��µĻ�ѧƽ�ⳣ����K����
�¶�
| 250��
| 300��
| 350��
|
K
| 2.041
| 0.270
| 0.012
|
�ɱ��������ж�DH1_______________0���<������=����>������
�� ij�¶��£���2molCO��6molH2����2L�ܱ������г�ַ�Ӧ��4���Ӻ�Ӧ�ﵽƽ�⣬���CO�����ʵ���Ϊ0.4mol����CO�ķ�Ӧ����Ϊ________________����ʱ��ѹǿ�Ƿ�Ӧǰѹǿ��___________����
��2����Ӧ���ƽ�ⳣ������ʽΪ____________________��Ϊ�˼ӿ췴Ӧ��ķ�Ӧ���ʣ��������H2��ת���ʣ���ȡ�Ĵ�ʩ��_______________����д��ȷѡ�����ĸ����
a������CO2��Ũ��? b������H2��Ũ��
c������ѹǿ? d���������
��3����ҵ������CO��ˮ�����ķ�Ӧ�����ж���COת��Ϊ����CO2����д�й��Ȼ�ѧ��Ӧ����ʽ__________________________________���÷�Ӧ��830K�½���ʱ����ʼŨ�ȵ���ƽ���ʱ�������µĹ�ϵ��
CO�ij�ʼŨ��(mol/L)
| 2
| 4
| 1
| 3
|
H2�ij�ʼŨ��(mol/L)
| 3
| 2
| 3
| 3
|
ʱ�䣨min��
| 8
| 6
| 12
| n
|
?
��n Ϊ________min��
��4����������������Ա�¿�����һ�ּ״���������ǿ����ҺΪ�������Һ�������ֻ���ء��õ���м״�������Ӧ��һ��Ϊ______������缫��ӦʽΪ_________________��
��5���øõ������Դ���ö��Ե缫��ⱥ��NaCl��Һʱ��ÿ����0.2mol CH3OH�����������������������Ϊ?L��
�ο��𰸣���1����<(1��)��?�� 0.2mol/(L��min) (1��)��? 0.6(2��)��
��2��K= c(CH3OH ) ��c(H2O) / c(CO2) ��c3(H2) (1��)��? a��c(1��)��
��3��CO(g)+ H2O(g)  CO2(g)+H2(g)?DH = DH 1 - DH 2(2��)��? 4(2��)��
CO2(g)+H2(g)?DH = DH 1 - DH 2(2��)��? 4(2��)��
��4������1�֣���? CH3OH �C 6e- + 8OH-? = CO32- + 6H2O��2�֣���
��5��13.44(2��)��
��������������������¶����ߣ�ƽ�ⳣ��K��С�����Է�Ӧ���ȣ�
CO(g) + 2H2 (g)  CH3OH (g)
CH3OH (g)
��ʼ��mol����? 2? 6? 0
�仯����mol����1.6? 3.2? 1.6
ƽ������mol����0.4? 2.8? 1.6
ƽ��ʱ���������Ϊ0.4+2.8+1.6=4.8mol��Ϊԭ����4.8/8=0.6������ѹǿΪԭ����0.6������3���ɸ�˹���ɿ�֪��Ӧ��-�ɵ÷�ӦCO(g)+ H2O(g)  CO2(g)+H2(g)?DH = DH 1 - DH 2������
CO2(g)+H2(g)?DH = DH 1 - DH 2������
CO�ij�ʼŨ��(mol/L)
2
4
1
3
H2�ij�ʼŨ��(mol/L)
3
2
3
3
ʱ�䣨min��
8
6
12
n
?
H2�ij�ʼŨ����ͬ��CO��Ũ��Ϊ2��1ʱ������ʱ��Ϊ2��3����CO��Ũ��Ϊ2��3ʱ������ʱ��Ϊ2��1����n=4����4����? CH3OH �C 6e- + 8OH-? = CO32- + 6H2O����5��ÿ����0.2mol CH3OH��ת�Ƶĵ���Ϊ1.2mol�����ص�������ӦΪ2H++2e-=H2�����Բ���������Ϊ0.6mol������µ����Ϊ13.44L.
�����Ѷȣ�����
3��ѡ���� ��25��ʱ��������ƽ�⣺2NO2?N2O4��H��0��������ƿ����100��ķ�ˮ�У����������
����ɫ?��ƽ��Ħ������?������?��ѹǿ?���ܶȣ�
���дﵽ��ƽ��ǰ������ǣ�������
A���ۢ�
B���ۢ�
C���ڢ�
D���٢�
�ο��𰸣������¶ȣ���ѧƽ���������ȷ�����У����Ի�ѧƽ��2NO2?N2O4������У�
�ٻ�ѧƽ��2NO2?N2O4������У����ɶ�������Ũ��������ɫ��������ı䣬�ʢٴ���
�ڻ�ѧƽ��2NO2?N2O4������У������غ㣬�����ܵ����ʵ��������ˣ�����ƽ��Ħ������Ҫ��С���ᷢ���ı䣬�ʢڴ���
�ۻ�ѧƽ��2NO2?N2O4������У�������������������غ�ģ������������䣬�ʢ���ȷ��
�ܻ�ѧƽ��2NO2?N2O4������У������غ㣬�����ܵ����ʵ��������ˣ�����ѹǿ�ᷢ���ı䣬�ʢܴ���
�ݻ�ѧƽ��2NO2?N2O4������У���������������غ�ģ���ƿ�����Ҳ�Dz���ģ������ܶȲ��䣬�ʢ���ȷ��
��ѡ��A��
���������
�����Ѷȣ���
4������� һ���¶��£�����ͼ��ʾ���п��ƶ��������ܱ������г���2 L SO2��1 L O2�Ļ�����壬�������·�Ӧ2 SO2 (g) + O2 (g) 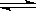 2 SO3 (g) ��
2 SO3 (g) ��
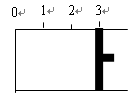
��1���������������ƶ���ƽ�����ֹͣ�ڡ�2.1��������÷�Ӧ��SO2��ת����Ϊ____?____��
��2������ʼʱ��������������ʼ���ʷֱ���
��2 L SO2��1 L O2��
��2 L SO3 (g) �� 1 L N2 ��
��1 L SO2��1 L O2�� 1 L SO3 (g)��
ʹ�����̶��ڡ�3�������ﵽƽ���������SO3 (g)ռ��Ӧ��������������Ĵ�С��ϵ�ǣ�
?������ź͡�<������=������>����ʾ����
��3����1��ƽ���������г���0.2 mol ��SO3�������ƶ����ٴδﵽƽ��ʱ����ô˹����д���繲������1.96 kJ ��������
д��SO2����������Ӧ���Ȼ�ѧ����ʽ��________?��
�ο��𰸣���1��90%
��2���٣���>��
��3��2 SO2 (g) + O2 (g) 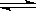 2 SO3 (g)?��H��-196 kJ?mol-1
2 SO3 (g)?��H��-196 kJ?mol-1
���������(1)2 SO2 (g) + O2 (g) 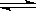 2 SO3 (g)
2 SO3 (g)
��ʼ��? 2? 1? 0
�仯��? 2x? x? 2x
ƽ����? 2-2x? 1-x? 2x
(2-2x)+( 1-x)+2x=2.1��x=0.9
��÷�Ӧ��SO2��ת����=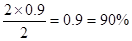
(2)��ӦΪ���������µĿ��淴Ӧ��2 L SO2��1 L O2�ij����൱��2 L SO3 (g)�ij��룬Ϊ��Чƽ�⣻��2 L SO3 (g)�����ں����������൱��2 L SO3 (g) �� 1 L N2 ���룬���Ԣ٢�Ϊ��Чƽ�⣬������SO3 (g)ռ��Ӧ���������������ȣ�1 L SO2��1 L O2�� 1 L SO3 (g)�ij��뷽ʽ�൱��2L SO2��1.5 L O2�ij��룬�൱�ڢٴﵽƽ����ٳ���0.5L��O2ƽ��������Ӧ�����ƶ���������SO3 (g)ռ��Ӧ����������������ڢ٢ڣ�
��3�����¡���ѹ�����淴Ӧ��Ͷ�����ɱ�����ϵ�ķ�Ӧ��Ϊ��Чƽ�⣬���ԣ���1���ﵽƽ�����Ͷ��0.2 mol ��SO3�ķ�ӦΪ��Чƽ�⣬�˹���SO3��ת����Ϊ10%����0.02 mol ��SO3��Ӧ�ﵽƽ�⣬��������1.96 kJ����SO2����������Ӧ���Ȼ�ѧ����ʽ��
2 SO2 (g) + O2 (g)  2 SO3 (g)?��H��-196 kJ?mol-1
2 SO3 (g)?��H��-196 kJ?mol-1
�����Ѷȣ���
5������� (6��) ��ͼ��ʾ800��ʱ��һ����Ӧ��ϵ��A��B��C�����������ʵ�Ũ����ʱ��仯�������t�Ƿ�Ӧʱ�䡣��ش�
��1���÷�Ӧ�ķ�Ӧ����______��
��2���÷�Ӧ�Ļ�ѧ����ʽΪ_?_____��
��3���ﵽƽ��״̬������ʱ����2min�����2min��A���ʵ�ƽ����Ӧ����Ϊ___? ____��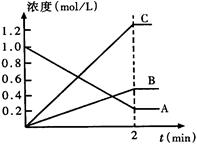
�ο��𰸣���1��A ��2��2A 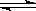 ?B + 3C?��3��0.4 mol��mol��1��min��1
?B + 3C?��3��0.4 mol��mol��1��min��1
�����������
�����Ѷȣ���