微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 把分别盛有熔融的氯化钾、氯化镁、氯化铝的三个电解槽串联,在一定条件下通电一段时间后,析出钾、镁、铝的物质的量之比为
[? ]
A.1:2:3
B.3:2:1
C.6:3:1
D.6:3:2
参考答案:D
本题解析:
本题难度:一般
2、填空题 (8分)用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到H2SO4,其原理如下图所示。(电极材料为石墨)
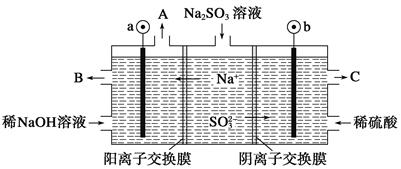
(1)图中a极要连接电源的(填“正”或“负”)________极,C口流出的物质是________。
(2) 放电的电极反应式为________ ____。
放电的电极反应式为________ ____。
(3)电解过程中阴极区碱性明显增强,用平衡移动原理解释原因____ ____。
参考答案:(1)负 硫酸;(2)  ;(3)H2O
;(3)H2O H++OH-,在阴极H+放电生成H2,c(H+)减小,水的电离平衡正向移动,碱性增强
H++OH-,在阴极H+放电生成H2,c(H+)减小,水的电离平衡正向移动,碱性增强
本题解析:(1)根据电解池中阴阳离子的移动方向:阳离子移向阴极可以判断①图中a极要连接电源的负极,SO32-在阳极失去电子变成SO42-,所以C口流出的物质是H2SO4,(2)SO32-放电的电极反应式为SO32--2e-+H2O=SO42-+2H+;(3)在阴极H+放电生成H2,c(H+)减小,水的电离平衡H2O?H++OH-正向移动,所以碱性增强;故答案为:(1)负 ;硫酸;(2)  ;(3)H2O
;(3)H2O H++OH-,在阴极H+放电生成H2,c(H+)减小,水的电离平衡正向移动,碱性增强
H++OH-,在阴极H+放电生成H2,c(H+)减小,水的电离平衡正向移动,碱性增强
考点:电解原理
本题难度:一般
3、选择题 (08陕西四校联考,8)下列叙述不正确的是(?)
A.电解法精炼铜时,纯铜作阴极,Cu2+发生还原反应
B.电解饱和食盐水时,用铁作阳极,C1-发生氧化反应
C.电镀锌时,金属锌作阳极,电镀液可用硫酸锌溶液
D.铜锌原电池中,锌作负极,电子沿导线从锌极流向铜极
参考答案:B
本题解析:本题考查原电池和电解池,中等题。电解法精炼铜时,纯铜作阴极,粗铜作阳极,A对;电解饱和食盐水时,应用惰性电极(如Pt、石墨等)做阳极,B错;电镀锌时,镀层金属(Zn)作为阳极,含有镀层金属离子的溶液作电镀液,C对;铜锌原电池中,锌作负极,铜作正极,电子从负极经导线流向正极,D对。
本题难度:一般
4、选择题 按下图装置进行电解(均是惰性电极),已知A烧杯中装有500 mL20%的NaOH溶液,B烧杯中装有500 mL pH为6的1 mol・L-1CuSO4溶液。通电一段时间后,在b电极上收集到28mL气体(标准状况),则B烧杯中溶液pH变为(溶液体积变化忽略不计)
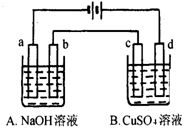
A.4
B.3
C.2
D.1
参考答案:C
本题解析:A烧杯的b电极上产生氧气:2H2O=2H2↑+O2↑
B烧杯有硫酸生成:2CuSO4+2H2O=2Cu+O2↑+2H2SO4
以上两式均有4个电子转移,根据电子守恒,可知:O2∽2H2SO4∽4H+
求得B烧杯中得到0.005molH+,c(H+)="0.02" mol・L-1,pH=2
故答案为C
本题难度:一般
5、选择题 用惰性电极电解一定质量的某浓度的NaCl溶液,一段时间后停止电解.此时若加入100g36.5%的浓盐酸,所得溶液正好与原溶液完全相同,则下列说法正确的是( )
A.电解过程中,两极所得到的气体,在相同的条件下体积相等
B.电解过程中,在相同的条件下,阳极所得到的气体的体积比阴极的大
C.电解过程中转移电子的物质的量约为8mol
D.原某浓度的NaCl溶液中溶有117gNaCl
参考答案:A、如果纯粹电解NaCl,那么应该补充纯粹的HCl气体即可,而现在加入的是100g36.5%的浓盐酸,其中含HCl为100×36.5%g36.5g/mol=1mol,相当于电解HCl即2HCl?电解?.?H2↑+Cl2↑,
含水为100×63.5%g18g/mol=3.5mol,由此知还应该有水的电解,即2H2O?电解?.?2H2+O2,
根据反应:2HCl?电解?.?H2↑+Cl2↑,
? 2? 1? 1
?1mol? 0.5mol?0.5mol?
? 2H2O?电解?.?2H2+O2
? 2? 2? 1
? 3.5mol?3.5mol?1.75mol
阳极生成的气体为:0.5+1.75=2.25mol;阴极产生的气体为:0.5+3.5=4mol,两极产生的气体体积不相等,故A错误;
B、阴极产生的是H2,物质的量为4mol,阳极产生的是Cl2和O2,物质的量为2.25mol,阴极所得的气体体积比阳极多,故B错误;
C、1molCl转移1mol电子,1molH2O转移2mol电子,转移电子的总数是1×1+3.5×2=8mol,故C正确;
D、原某浓度的NaCl溶液中溶有1mol的Cl-离子,则NaCl的物质的量也是1mol,可得原某浓度的NaCl溶液中溶有(23+35.5)×1=58.5gNaCl,故D错误;
故选C.
本题解析:
本题难度:一般