��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ������Ե�ص��ܷ�Ӧʽ��HM+NiO(OH)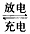 NiO+M+ H2O��HM��ʾ�Ͻ�M�������ļ�ʽ�������ݴ˷�Ӧʽ�жϣ�����������ȷ����
NiO+M+ H2O��HM��ʾ�Ͻ�M�������ļ�ʽ�������ݴ˷�Ӧʽ�жϣ�����������ȷ����
[? ]
A����طŵ�ʱ����ظ�����Χ��Һ��OH-Ũ�Ȳ�������
B����طŵ�ʱ����Ԫ�ر�����
C����س��ʱ����Ԫ�ر���ԭ
D����س��ʱ��������ӦΪNiO- e- + OH- = NiO(OH)
2��ѡ���� ��֪��pHΪ4-5����Һ�У�Cu2+������ˮ�⣬��Fe3+������ȫˮ�⡣ijѧ�����õ��CuSO4��Һ�ķ����ⶨͭ�����ԭ����������ͬѧ��pH=3.8�ĺ���Fe2(SO4)3���ʵ�CuSO4��Һ�м��������ĺ�ɫ��ĩX����ֽ������ˣ�����Һ������ͼ��ʾװ�õ�⣬����ij�缫����ag����һ�缫�ϲ�����״���µ���
VmL������˵����ȷ����

[? ]
A����ɫ��ĩX������
B��ͭ�缫���ӵ�Դ����
C��ʯī�缫�Ϸ����ķ�Ӧ��4OH--4e-=O2��+2H2O
D��ͭ�����ԭ�������ļ���ʽ��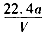
3��ѡ���� �ӵ�ʳ���к��е���أ�KIO3�������Ե�ⷨ�Ʊ�����أ�ʵ��װ����ͼ��ʾ���Ƚ�һ�����ĵ����ڹ�������������Һ��������Ӧ��3I2+6KOH=5KI+KIO3+3H2O��������Һ��������������������������Һ��������������ʼ��⣮����˵����ȷ���ǣ�������
A��a�缫������
B��a������KI����ת��ΪKIO3
C�������缫��Ӧ��4OH--4e-�T2H2O+O2��
D����������OH-��a����ͨ�����ӽ���Ĥc����b����