微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列物质中,摩尔质量最大的是
A.10mlH2O
B.0.8molH2SO4
C.54gAl
D.1gCaCO3
参考答案:D
本题解析:试题分析:在数值上,摩尔质量等于其相对分子质量。水的摩尔质量是18g/mol,硫酸的摩尔质量是98g/mol,铝的摩尔质量是27g/mol,碳酸钙的摩尔质量是100g/mol,所以摩尔质量最大的是碳酸钙。
考点:摩尔质量
本题难度:一般
2、实验题 有A、B、C、D、E、F、G七瓶不同物质的溶液,它们各是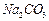 、
、 、
、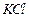 、
、 、
、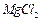 、
、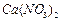 和
和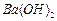 溶液中的一种。为了鉴别,各取少量溶液进行两两混合,实验结果如下表所示。表中“↓”表示生成沉淀或微溶化合物,“-”表示观察不到明显现象。试回答下列问题。
溶液中的一种。为了鉴别,各取少量溶液进行两两混合,实验结果如下表所示。表中“↓”表示生成沉淀或微溶化合物,“-”表示观察不到明显现象。试回答下列问题。
?
| A
| B
| C
| D
| E
| F
| G
|
A
| -
| -
| -
| -
| -
| -
| ↓
|
B
| -
| -
| -
| -
| ↓
| ↓
| ↓
|
C
| -
| -
| -
| ↓
| -
| ↓
| ↓
|
D
| -
| -
| ↓
| -
| ↓
| ↓
| ↓
|
E
| -
| ↓
| -
| ↓
| -
| ↓
| -
|
F
| -
| ↓
| ↓
| ↓
| ↓
| -
| ↓
|
G
| ↓
| ↓
| ↓
| ↓
| -
| ↓
| -
|
(1)A的电子式是 ,G的化学式是 。判断理由
是 。
(2)写出其余几种物质的化学式B ,C ,D 。
(3)①写出D与E反应的化学方程式 ;
②G与过量氨水总反应的离子方程式 。
参考答案:(1)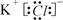 (2分) AgNO3(2分)
(2分) AgNO3(2分)
混合时只生成一种沉淀的是KCl,生成的是AgCl,所以A是KCl,G是AgNO3(2分)
(2) (2分)
(2分) 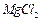 (2分)
(2分) 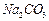 (2分)
(2分)
(3)①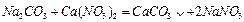 (2分)
(2分)
②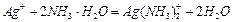 (2分)
(2分)
本题解析:略
本题难度:一般
3、选择题 20℃时,NaCl的溶解度是36 g,此时NaCl饱和溶液的密度是1.12 g/cm3,此时NaCl饱和溶液中NaCl的物质的量浓度为
A.1.36 mol/L
B.5.07 mol/L
C.6.15 mol/L
D.0.15 g/mol
参考答案:B
本题解析:
本题难度:困难
4、选择题 纯净的氯化钠是不潮解的,但粗盐很容易潮解,这主要是因为其中含有杂质MgCl2的缘故.为得到纯净的氯化钠,有人设计了一个实验:把买来的粗盐放入纯氯化钠饱和溶液一段时间,过滤,洗涤,可得纯净的氯化钠晶体.则下列说法中,正确的是( )
A.粗盐的晶粒大一些有利于提纯
B.设计实验的根据是MgCl2比NaCl易溶于水
C.在整个过程中NaCl饱和溶液浓度会变大(温度不变)
D.设计实验的根据是NaCl的溶解平衡
参考答案:A.NaCl固体在NaCl饱和溶液中的溶解是一种动态平衡,食盐颗粒小一些能加快溶解和析出的速率,有利于提纯,故A错误;
B.设计实验的根据是NaCl固体在NaCl饱和溶液中的溶解不在增加,而MgCl2在NaCl饱和溶液中溶解未达到饱和,因此MgCl2溶解只剩下纯净的NaCl,故B错误;
C.NaCl溶液已达到饱和,浓度不可能变大,故C错误;
D.在饱和NaCl溶液中,NaCl固体的溶解处于平衡状态,溶解和析出同时存在,NaCl溶解的量不会再增加,但对于MgCl2并未达到饱和,因此最后的固体中只会存在NaCl,故D正确.
故选D.
本题解析:
本题难度:一般
5、选择题 下列说法正确的是(?)
A.可用加热的方法除去混在碳酸钠固体中的碳酸氢钠固体
B.除去CO中少量的O2,可将混合气体通过灼热的Cu网
C.向某溶液中加入盐酸,产生使澄清石灰水变浑浊的气体,该溶液中一定含有CO32-
D.向某溶液中加入盐酸酸化的BaCl2溶液有白色沉淀,该溶液中一定含有SO42-
参考答案:A
本题解析:A、根据2NaHCO3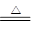 Na2CO3+CO2↑+ H2O知,可用加热的方法除去混在碳酸钠固体中的碳酸氢钠固体,正确;B、除去CO中少量的O2,将混合气体通过灼热的铜网会引入新的杂质CO2,错误;C、向某溶液中加入盐酸,产生使澄清石灰水变浑浊的气体,该溶液中不一定含有CO32-还可能含有HCO3-、SO32-、HSO3-等离子,错误;D、向某溶液中加入盐酸酸化的BaCl2溶液有白色沉淀,该溶液中不一定含有SO42-,还可能是含有Ag+,错误。
Na2CO3+CO2↑+ H2O知,可用加热的方法除去混在碳酸钠固体中的碳酸氢钠固体,正确;B、除去CO中少量的O2,将混合气体通过灼热的铜网会引入新的杂质CO2,错误;C、向某溶液中加入盐酸,产生使澄清石灰水变浑浊的气体,该溶液中不一定含有CO32-还可能含有HCO3-、SO32-、HSO3-等离子,错误;D、向某溶液中加入盐酸酸化的BaCl2溶液有白色沉淀,该溶液中不一定含有SO42-,还可能是含有Ag+,错误。
本题难度:一般