��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��14�֣���1������Ũ�ȸ�Ϊ1 mol/L��FeCl3��FeCl2��CuCl2�Ļ����Һ100mL������һ���������ۣ������������գ�
�ٳ�ַ�Ӧ��������ʣ�࣬����Һ��һ������__________������,һ��û��__________�����ӡ���2�֣��йط�Ӧ�����ӷ���ʽ��__________________________
__________________________________________________________����2�֣�
�ڳ�ַ�Ӧ��������ʣ�࣬��ͭ���ɡ���Ӧ�����Һ��һ������_________�����ӣ���Һ�п��ܺ���_________�����ӣ�������������Һ�����ʵ����Ŀ��ܴ��ڷ�Χ�ǣ�? ______________________����4�֣�
�۳�ַ�Ӧ�������������ڣ���Ӧ�����Һ��һ������____��____�����ӡ���2�֣�
��2������AlCl3��FeCl3�Ļ����Һ������Al3+��Fe3+�����ʵ���֮��Ϊ0.1 mol���ڴ���Һ�м���90 mL 4 mol / L��NaOH��Һ��ʹ���ַ�Ӧ;��Al3+ �����ʵ����������ʵ����ı�ֵΪx��
�ٸ��ݷ�Ӧ�Ļ�ѧ����ʽ����x��0.4ʱ����Һ�в����ij�����___________;���ʵ�����__________mol����2�֣�
�ڼ��������ֻ��Fe��OH��3ʱ��x��ȡֵ��Χ��_____________________����2�֣�
2��ѡ���� �����±�����ʵ�鼰����ó��Ľ��۲���ȷ���ǣ�?��
ʵ����Ŀ
| ʵ������
|
FeCl3��Һ�м���ά����C(VC)
| ��Һ��ɫΪdz��ɫ
|
����FeCl3��Һ�����ˮ��
| �õ����ɫҺ��
|
��ͭ�����������
| ����ɫ���ݲ���
|
?
A��ά����C(VC)���л�ԭ��
B��FeCl3ˮ������Fe(OH)3����
C��ͭ�������ᷴӦ��H2����
D��ͭ���к���̼���
3������� A�������ʽṹ�����ʡ�ģ�飨12�֣�
��ï����(C5H5)2 Fe������һ�����������Ӻ�2������ϩ�������ӹ��ɣ����ķ��ֿ���˵���л������������о��о�����̱�������¼����������˽����л��������о��������ٽ��˽����л���ѧ�ķ�չ����ï�������û�ԭ�����뻷���ϩ�ڵ�����Χ�з�����Ӧ���Ƶã�
2C5H6��Fe(��ԭ����)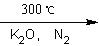 (C5H5)2 Fe��H2��
(C5H5)2 Fe��H2��
��ش��������⣺
��1��д�����������ӵĻ�̬�����Ų�ʽ��?��
��2����ï�����۵���173�棨��100��ʱ��ʼ���������е���249�棬������ˮ�������ڱ������ѵȷǼ����ܼ����ݴ˿��ƶ϶�ï������Ϊ?���壬�ɴ˿ɽ�һ����֪���ڶ�ï���ṹ�У�C5H5����Fe2+֮���γɵĻ�ѧ��������?��
��3�������ϩ�ĽṹʽΪ��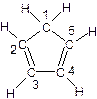 ��ͼ�����ֽ�����̼ԭ�ӱ�ţ�������5��̼ԭ���в�ȡsp3�ӻ�����?����д��ţ���
��ͼ�����ֽ�����̼ԭ�ӱ�ţ�������5��̼ԭ���в�ȡsp3�ӻ�����?����д��ţ��� �ǻ�ï��ϩ��һ��ͬ���칹�壬������ӽṹ�д���ͬһƽ���ϵ�ԭ�Ӹ��������?����
�ǻ�ï��ϩ��һ��ͬ���칹�壬������ӽṹ�д���ͬһƽ���ϵ�ԭ�Ӹ��������?����
��4��ԭ����Ŀ�͵�����������۵�����������ͬ������Ϊ�ȵ����壬�ȵ�����������ƵĽṹ��������N2���ӻ�Ϊ�ȵ�����Ķ�����������?���ѧʽ���������ʽ��?��
B����ʵ�黯ѧ��ģ�飨12�֣�
��12�֣�ij����С��Ϊ�˲ⶨij�Ȼ��ȣ�SrCl2����Ʒ�Ĵ��ȣ��ڽ�ʦָ������������·�����
��ȡ1.0g��Ʒ�ܽ�������ˮ�У������м��뺬AgNO32.38g��AgNO3��Һ����Һ�г�Cl�D�⣬����������Ag+��Ӧ���ɳ��������ӣ���Cl�D����ȫ��������Ȼ���ú�Fe3+����Һ��ָʾ������NH4SCN����Һ�ζ�ʣ���AgNO3��ʹʣ���Ag+��AgSCN��ɫ��������ʽ�������Բⶨ�Ȼ�����Ʒ�Ĵ��ȡ���ش��������⣺
��1���ζ���Ӧ�ﵽ�յ�������ǣ�?��
��2��ʵʩ�ζ�����Һ�Գ�?��ѡ����ԡ��������ԡ����ԡ���Ϊ�ѣ�����?���ѧʽ���Լ��ɴ���һĿ�ġ�
��3�����յ㵽��֮ǰ�ĵζ������У����ֳ����������������Ag+���費�Ͼ���ҡ����ƿ�������ʹn (Cl��)�IJⶨ���?��ѡ�ƫ�ߡ�����ƫ�͡�����Ӱ�족����
��4�������յ�����������ҡ����ƿ������ʱ���þ���ҡ�����Լ�����������������ʹn (Cl��)�ⶨֵƫ�ͣ���˵�����ߵ��ܽ�ȣ�AgCl?AgSCN
���������������
��5������Fe3+����Һ��ָʾ������NH4SCN����Һ�ζ�ʣ���AgNO3ʱ����ȥ����Ũ�ȵ�NH4SCN��Һ20.0mL����ԭ�Ȼ�����Ʒ�Ĵ���Ϊ?��
4��ѡ���� ���������䡢��ˮ��Ӧ��������ˮ������Ӧ�������йظ�ʵ���˵������ȷ���ǣ�������
A����װ��ʵ��װ���õ��IJ��������ɽ�Ϊһ���ƾ��ơ�һ֧���Թܺ͵�����
B����ͨ������ʪ������ˮ����
C���ɽ�����֮һͨ�����Һ����ȼ�շ�����
D��������ˮ������Ӧ�������ô�����ʣ�����۷������
5��ѡ���� ����������Һ�У�����a gͭ����ȫ�ܽ���ּ���b g������ַ�Ӧ��õ�c g������壬��b<c���������ж���ȷ����? (����)
A�����õ�����Һ�к���Fe3��
B������������Ϊ����ͭ�����
C�����õ�����Һ��ֻ��Cu2��
D���������һ��ȫ����ͭ