|
高考化学知识点归纳《物质的量》高频试题巩固(2017年最新版)(十)
2017-08-08 06:36:13
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 将标准状况下11.2L的HCl气体溶解于水配成1L溶液,所得溶液的浓度是
A.2mol/L
B.1.5mol/L
C.1mol/L
D.0.5mol/L
|
参考答案:D
本题解析:标准状况下,11.2LHCl的物质的量为:n(HCl)=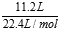 =0.5mol,所得溶液的物质的量浓度为:c(HCl)= =0.5mol,所得溶液的物质的量浓度为:c(HCl)= =0.5mol/L,故选D. =0.5mol/L,故选D.
考点:物质的量浓度的相关计算
本题难度:一般
2、选择题 若NA表示阿伏加德罗常数,下列说法正确的是?(?)
A.1 mol SiO2晶体中含有NASiO2个分子
B.7.8 g Na2O2中含有的离子总数目为0.4NA
C.标准状况下2.24L苯含有的碳原子数目为0.6NA
D.12.8g Cu与足量HNO3反应生成NO和NO2,转移电子数目为0.4NA’
参考答案:D
本题解析:A错,SiO2晶体为原子晶体,无分子;B错,7.8 g Na2O2中含有的离子总数目为0.3NA;C错,标准状况下苯不是气体;D正确;
本题难度:一般
3、简答题 用质量分数为98%,密度为1.84g?cm-3的浓硫酸配制1mol/L稀硫酸100mL,其操作有以下各步:
①用量筒量取______mL浓硫酸
②洗涤烧杯和玻璃棒2-3次,将洗涤液转入容量瓶中
③将稀释、冷却后的硫酸转入100mL容量瓶中
④将浓硫酸倒入盛有水的烧杯中稀释、冷却
⑤加水至液面接近刻度线1~2cm处,定容,摇匀
完成下列填空:
(1)第①步操作中应用量筒量取______mL浓硫酸;应选择______mL量筒(填5、10或50).
(2)本实验用到的基本仪器已有烧杯、量筒、玻璃棒,还缺少的仪器是______.
(3)正确的操作顺序是(用序号填写)______.
(4)定容时,如果俯视刻度线,配制的硫酸浓度将偏______(填大或小).
参考答案:(1)浓H2SO4的物质的量浓度c=1000×1.84×98%98mol/L=18.4mol/L.根据稀释定律,稀释前后溶质的物质的量不变,来计算浓硫酸的体积,设浓硫酸的体积为xmL,所以xmL×18.4mol/L=100mL×1mol/L,解得:x≈5.4.
所需浓硫酸的体积为5.4mL.量筒规格越接近所需浓硫酸体积误差越小,所以选择10mL量筒.
故答案为:5.4;10.
(2)操作步骤有计算、量取、稀释、移液、洗涤移液、定容、摇匀等操作,用量筒量取(用到胶头滴管)浓硫酸,在烧杯中稀释,用玻璃棒搅拌,冷却后转移到100mL容量瓶中,并用玻璃棒引流,洗涤2-3次,将洗涤液转移到容量瓶中,加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,最后定容颠倒摇匀.
由提供的仪器可知还需要仪器有:100mL容量瓶、胶头滴管.
故答案为:100mL容量瓶、胶头滴管.
(3)由(2)中操作步骤可知正确的操作顺序是①④③⑤②.
故答案为:①④③⑤②.
(4)定容时,如果俯视刻度线,导致所配溶液的体积减小,配制的硫酸浓度将偏大.
故答案为:大.
本题解析:
本题难度:一般
4、选择题 某化学反应中,反应混合物A、B、C的物质的量浓度(c )与时间(t)关系如下所表示:
t/ c
| 初始
| 2min
| 4min
| 6min
| 8min
| c(A)(mol/L)
| 1.45
| 1.28
| 1.00
| 1.00
| 1.20
| c(B)(mol/L)
| 0.38
| 0.72
| 1.28
| 1.28
| 0.88
| c(C)(mol/L)
| 0.095
| 0.18
| 0.32
| 0.32
| 0.42
|
下列说法正确的是: ( )
A.该反应的化学方程式为A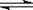 2B+C B.2 min末A的转化率为11.7% 2B+C B.2 min末A的转化率为11.7%
C.4--6min时,反应停止了
D.6--8min之间的变化是由于增加了A的浓度引起的
参考答案:B
本题解析:略
本题难度:一般
5、选择题 如果1 g水中含有n个氢原子,则阿伏加德罗常数是:
A.n/1mol-1
B.9n mol-1
C.2nmol-1
D.nmol-1
参考答案:B
本题解析:水的化学式为H2O,其中含有2个氢原子,18g克水为1mol,其中含有的氢原子数为18n,所以阿伏加德罗常数是18n/2=9n,答案选B。
点评:本题考查了阿伏加德罗常数的计算,该题不难。
本题难度:一般
| 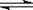 2B+C B.2 min末A的转化率为11.7%
2B+C B.2 min末A的转化率为11.7%