��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��֪25��ʱ�й�����ĵ���ƽ�ⳣ����
���ữѧʽ
| CH3COOH
| HCN
| H2CO3
|
����ƽ�ⳣ����25�棩
| 1.8��l0-5
| 4.9��l0-10
| K1=4.3��l0-7
K2=5.6��l0-11
|
?
�������й�˵����ȷ����
A���������Һ��ˮϡ��ʱ������ĵ���ƽ�������ƶ���
B�������ʵ���Ũ�ȵĸ���ҺpH��ϵΪ��pH��NaCN����pH��Na2CO3����pH��CH3COONa��
C��a mol/L HCN��Һ��b mol/L NaOH��Һ�������Ϻ�������Һ��c(Na��)��c(CN��)����aһ������b
D����ͬŨ�ȵ�CH3COONa��KCN��Һ��c(Na+-)- c(CH3COO-)С�ڵ�c(K+) -c(CN��)
�ο��𰸣�D
���������A����������������ʣ���ˮ�ٽ�����,����ƽ�������ƶ���A����B�����ݵ���ƽ�ⳣ����֪����ǿ��˳��Ϊ��CH3COOH��HCN��HCO3-������Խ������Ӧ�������������ˮ��̶�Խ����Һ��PHԽ�����ʵ���Ũ�ȵĸ���ҺpH��ϵΪ��pH��Na2CO3����pH��NaCN����pH��CH3COONa������B����C���軯����ǿ�������Σ�Ҫʹ����Һ�����ԣ���������ʵ���Ӧ������Щ������Һ�����δ֪�����ж���Ũ�ȴ�С����C����D��CH3COO-��ˮ��̶�С��CN����ˮ��̶ȣ�cCH3COO-)> c(CN��)������D��ȷ��
�����Ѷȣ�һ��
2��ѡ���� 25�棬pH=3�Ĵ�����Һ��I����pH=ll������������Һ��II��������˵����ȷ����(? )
A��I��II��H2O�ĵ���̶Ȳ����
B����Iϡ��l0������Һ��c��CH3COOH����c��OH��������С
C��I��II��Һ��ϣ���c��OH������c��H+��������������һ������
D��I��II�������Ϻ���Һ������Ũ�ȴ�СΪc��CH3COO����+ c(CH3COOH��c��Na+��
�ο��𰸣�D
��������� pH=3�Ĵ�����Һ��I����pH=ll������������Һ��II���е�c��H+��=c��OH����=0.001mol/L����˶�ˮ���������������ȣ�A����I����Һ����ϡ�ͣ���Һ��OH-Ũ��Խ��Խ��B������ΪI�����ᣬII��ǿ���ǡ����ȫ�к͵õ��Ĵ�������ҺҲ�Լ��ԣ�����C������I��II�������ϣ���I�еĴ�����������Ը��������غ�c��CH3COO����+ c(CH3COOH��c��Na+������D��ȷ����ѡD��
�����Ѷȣ���
3������� (6��)����10�������У���NaOH��Һ��H2SO4������ͭ�����Cu ��CH3COOH?��NaOH��������Ǣ�ʯ��ˮ��ˮ���ⰱˮ
�ܵ������?������ǿ����ʵ���?������������ʵ���?��
�ο��𰸣�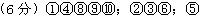
�����������
�����Ѷȣ���
4��ѡ���� ���и������ǿ����ʡ�������ʡ��ǵ���ʵĹ��࣬��ȫ��ȷ����(����)
| A
| B
| C
| D
|
ǿ�����
| Fe
| NaCl
| CaCO3
| HNO3
|
�������
| CH3COOH
| NH3
| H3PO4
| Fe(OH)3
|
�ǵ����
| C12H22O11(����)
| BaSO4
| C2H5OH
| H2O
|
�ο��𰸣�C
������������Ȳ��ǵ���ʣ�Ҳ���Ƿǵ���ʣ�A�����NH3�Ƿǵ���ʣ�BaSO4��ǿ����ʣ�B�����̼������Σ�Ϊǿ����ʣ���������ǿ�ᣬ��������ʣ��Ҵ��Ƿǵ���ʣ�C����ȷ��H2O��������ʣ�D�����
�����Ѷȣ�һ��
5��ѡ���� ��֪0.1mol/L�Ĵ�����Һ�д��ڵ���ƽ�⣺CH3COOH?CH3COO-+H+Ҫʹ��Һ��
ֵ�����Բ�ȡ�Ĵ�ʩ�ǣ�������
A���������ռ����
B�������¶�
C��������������
D����CH3COONa
�ο��𰸣�A�������ռ���壬��Ӧ����CH3COO-��c��H+����С������CH3COO-��CH3COOH�ĵ������������ã���c��H+��/c��CH3COOH��ֵ��С����A����
B��������ʵĵ���Ϊ���ȹ��̣����ȴٽ����룬��c��H+��/c��CH3COOH��ֵ����B��ȷ��
C�������������ᣬ����Ũ������������ʵ�Ũ��Խ����̶�ԽС����c��H+��/c��CH3COOH��ֵ��С����C����
D����CH3COONa������CH3COO-��CH3COOH�ĵ������������ã���c��H+��/c��CH3COOH��ֵ��С����D����
��ѡB��
���������
�����Ѷȣ���