微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 已知HF、CH3COOH均为弱酸,酸性强弱顺序为HF>CH3COOH.下列说法不正确的是( )
A.浓度均为0.1mol?L-1的NaF、CH3COONa溶液相比较,CH3COONa溶液碱性较强
B.0.1mol?L-1CH3COOH溶液,加水稀释过程中,所有离子浓度均减小
C.NaF溶液中含有Na+、F-、H+、OH-、H2O、HF六种微粒
D.NaF溶液中加入少量NaOH固体,溶液中c(F-)变大
参考答案:B
本题解析:
本题难度:简单
2、选择题 现有物质的量浓度为0.1 mol/L的盐酸和0.1 mol/L的氨水,下列说法中正确的是(?)
A.用湿润的pH试纸测定两种溶液的pH时,氨水的误差更大
B.若混合后溶液恰好呈中性时:c(Cl-)= c(NH4+)+ c(NH3・H2O)
C.两溶液等体积混合时,充分反应后:c(Cl-)> c(NH4+)> c(OH-)> c(H+)
D.恰好反应呈中性时,所需氨水的体积大于盐酸的体积
参考答案:D
本题解析:A选项,用润湿的PH试纸测定两种溶液时,弱电解质PH变化更小。故A错误。B选项,若混合后溶液恰好呈中性时:c(Cl-)= c(NH4+),故B错误。C选项,两溶液等体积混合时,充分反应后:c(Cl-)> c(NH4+)>c(H+)>c(OH-),故C选项错误。D选项,正确。
本题难度:一般
3、填空题 (12分)已知氢氟酸、醋酸、氢氰酸(HCN)、碳酸在室温下的电离常数分别为:
①
| HF
| Ka=6.8×10-4 mol?L-1
|
②
| CH3COOH
| Ka=1.7×10-5 mol?L-1
|
③
| HCN
| Ka=6.2×10-10 mol?L-1
|
④
| H2CO3
| Ka1=4.4×10-7mol?L-1
Ka2=4.7×10-11 mol?L-1
|
根据上述数据,回答下列问题:
(1)四种酸中酸性最强的是_____________,四种酸中酸性最弱的是_____________。
(2)写出H2CO3电离方程式是?、?。
(3)写出反应的方程式:足量的氢氟酸与碳酸钠溶液混合:___________?______,
足量的CO2通入NaCN溶液中:_________?_____。
参考答案:(1)氢氟酸,? HCN?
(2)H2CO3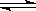 HCO3―+H+,? HCO3―
HCO3―+H+,? HCO3―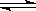 CO32―+H+
CO32―+H+
( 3)2HF+Na2CO3=2NaF+H2O+CO2↑,? NaCN+H2O+CO2= HCN+NaHCO3
本题解析:(1)电离常数越大,相应酸的酸性越强,所以根据电离常数可知,酸性最强的是氢氟酸,而最弱的是HCN。
(2)碳酸是二元弱酸,电离是分步进行的,所以电离方程式依次是
H2CO3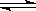 HCO3―+H+、HCO3―
HCO3―+H+、HCO3―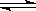 CO32―+H+。
CO32―+H+。
(3)由于氢氟酸的电离常数大于碳酸的电离常数,所以根据较强酸制取较弱的酸可知,反应的方程式是2HF+Na2CO3=2NaF+H2O+CO2↑;由于碳酸的第一步电离常数大于HCN的,但第二步小于HCN的,所以足量的CO2通入NaCN溶液中反应方程式是NaCN+H2O+CO2= HCN+NaHCO3。
本题难度:一般
4、选择题 下列化合物属于弱电解质的是(?)
A.HClO4
B.Ba(OH)2
C.CO2
D.HF
参考答案:D
本题解析:在水溶液中没有完全电离,存在电离平衡的是弱电解质,所以选项D正确,A和B是强电解质,CO2是非电解质,答案选D。
点评:强弱电解质并不能按物质的本质属性分类,主要的判断依据是,能否在水溶液中完全电离。从化学键和化合物的属类判别强弱电解质的依据如下:
(1)具有离子键的化合物是强电解质。
(2)具有极性共价键的化合物可能是强电解质,如HCl、HNO3等强酸;也可能是弱电解质,如CH3COOH、NH3・H2O等;还可能是非电解质,如CO2、SO2、NO、NO2、NH3等。
(3)部分盐类、强碱、强酸是强电解质。
(4)弱酸弱碱是弱电解质。
本题难度:一般
5、填空题 炼金废水中含有络离子[Au(CN)2]+,其电离出的CN―有毒,CN-与H+结合生成HCN时,其毒性更强。回答下列问题:
1)HCN的电离方程式为______________________NaCN溶液的pH_____7(填“< > =”)
2)与弱电解质的电离方程式相似,[Au(CN)2]+也存在着两步电离,其一级电离方程式为___________________________
3)处理这种废水是在碱性条件下,NaClO将CN―氧化为碳酸根和氮气,其离子方程式为:____________________________________
4)在酸性条件下,ClO―也能氧化CN--,但实际处理废水时却不在酸性条件下进行的原因是_______________________________网
参考答案:略
本题解析:略
本题难度:一般