��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��8�֣�ͼ��A��K������ѧ��ѧ�г������ʡ�A��һ���ᣬE��F��Iͨ��״���������壬����E�д̼�����ζ��X��Y�dz����Ľ������ʣ�JΪ���ɫ�������μӷ�Ӧ��ˮ�Լ����ɵ�ˮ��ͼ�о�����ȥ��
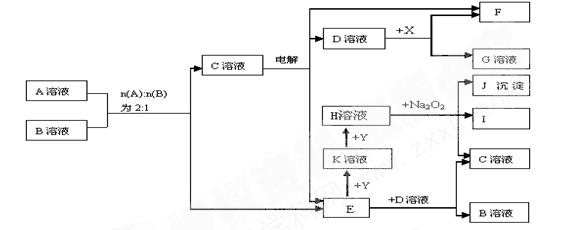
��ش��������⣺
��1��E�ĵ���ʽΪ? _____________��? J�Ļ�ѧʽΪ?��
��2��д������Һ��ٷ�Ӧ�����ӷ���ʽ����������������������������?��
��3��д��D��Һ��ط�Ӧ�����ӷ���ʽ ?__________��
��4��д��A��B �� C��E�Ļ�ѧ����ʽ? ______? __��
�ο��𰸣�����8�֣�
��1��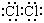 ����1�֣�Fe(OH)3����1�֣�?
����1�֣�Fe(OH)3����1�֣�?
��2��2Fe3+ + Fe = 3Fe2+��2�֣�
��3��2Al + 2H2O + 2OH- = 2AlO2- + 3H2����2�֣�
��4��2HCl + NaClO =" NaCl" + H2O + Cl2����2�֣�
�����������
�����Ѷȣ�һ��
2������� ��ͼ��ʾ�����У�ֻ��X�ǵ��ʣ�������A��B����̬����B�ǵ�������Ĵ�����Ⱦ�D�ǵ���ɫ���塣
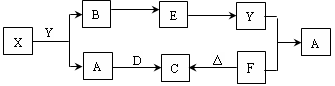
�ݴ˻ش��������⣺
��1��Ԫ��X��Ԫ�����ڱ���λ��?����?�塣
��2������D�ĵ���ʽΪ?�����������Ӹ�����Ϊ?��
��3���������F��������;��?��?��
��4��д��X��Y��Ӧ�Ļ�ѧ����ʽ?�������ɵ�B�ڱ�״���µ����Ϊ22.4L����Ӧ��ת�Ƶ�����ĿΪ?��
��5����д��Y��F��Ӧ�����ӷ���ʽ?��
�ο��𰸣���1������IVA
��2��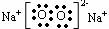 ��1�U2
��1�U2
��3���������ͷۡ�����θ�����ȣ�ֻҪ�������ɣ�
��4��C+2H2SO4��Ũ�� CO2��+2SO2��+2H2O��1.204��1024
CO2��+2SO2��+2H2O��1.204��1024
��5��H++HCO3-��CO2��+H2O
�������������ȫ����������ٿ����ڽ��ڸ���һģ�Ͷ�ģ�������У��������йص�����Խ��Խ�࣬�����ǽ��SO2�Դ�����Σ������Ҫ�Ļ�����Ӧ����ѧ��Ҫ��ѧ��Ӧ�����������ʵ�ʵ�һ�����ƶ��⡣�����֪ʶ��ȽϹ㣬�����ۺ���ǿ�����ϸ߿�����Ҫ����һ���ȼ���������⡣
��������������֪B��SO2����X�ǵ��ʣ�A�����壬����ȷ��X��A��Y�ֱ�ΪC��CO2��H2SO4�����D�ǵ���ɫ���壬����Ͽ�ͼ��ȷ��D��C��F�ֱ�ΪNa2O2��Na2CO3��NaHCO3���ݴ˿������𡣸���̼��ԭ�ӽṹΪ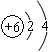 ����ȷ�����ڵڶ����ڵ�IVA�壻���Na2O2�ĵ���ʽ��ȷ���������Ӹ�����Ϊ1�U2������C��ŨH2SO4�ķ�Ӧ�����ϼ۱仯����ȷ������1mol SO2ʱת��2mol���ӡ�
����ȷ�����ڵڶ����ڵ�IVA�壻���Na2O2�ĵ���ʽ��ȷ���������Ӹ�����Ϊ1�U2������C��ŨH2SO4�ķ�Ӧ�����ϼ۱仯����ȷ������1mol SO2ʱת��2mol���ӡ�
�����Ѷȣ�һ��
3���ƶ��� ��ͼÿһ�����ʾ�йط�Ӧ��ijһ��Ӧ���������йز�������ȥ����֪AΪ���۵����ʣ������ͻ���ϣ�A��һ�������¿�����B��C��BΪ��ɫ���壬DΪһ����Ȼ�����Ŀ�ʯ����Ҫ�ɷ֣�����Ϊ���ϡ�
�Իش�
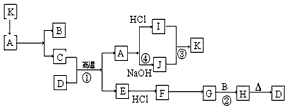
��1��д����ѧʽ��A___________��D____________��
��2��д����ѧ����ʽ��
��Ӧ��______________________����Ӧ��______________________��
��3��д�����ӷ���ʽ��
�ۣ�______________________���ܣ�______________________��
�ο��𰸣���1��A��Al2O3��D��Fe2O3
��2����2Al+Fe2O3 2Fe+Al2O3����4Fe(OH)2+O2+H2O=4Fe(OH)3
2Fe+Al2O3����4Fe(OH)2+O2+H2O=4Fe(OH)3
��3����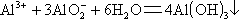 ����Al2O3+2OH-==2AlO2-+H2O
����Al2O3+2OH-==2AlO2-+H2O
���������
�����Ѷȣ�һ��
4������� ��6�֣���X��Y��Z��W���ֶ�����Ԫ�أ�ԭ����������������˵������Ϊ36��YԪ��ԭ������������ռ��������������3/4��WԪ��ԭ���������ӱ�ͬ����ZԪ�ض�5�����ӣ�W��Y����ͬһ���塣
��1��д��Ԫ�ط��ţ�X______Y_________Z________W___________.?
��2��Z��W��Ԫ�ص�����������Ӧˮ���ﷴӦ�����ӷ���ʽ��__________
�ο��𰸣���6�֣���1��д��Ԫ�ط��ţ�X__H__Y__O___Z__Na___W__S__.?
��2�����ӷ���ʽ��_��
�����������
�����Ѷȣ�һ��
5������� ��A��B��C��D������ɫ���壬
��A��ʹʪ��ĺ�ɫʯ����ֽ������
��һ�������£�A������B��Ӧ����C��C��������Ϊ����ɫ��
��D��A������ɰ��̣�
��D��Ũ��Һ�����̿���Ҫ�ɷ���MnO2���ڼ��������·�Ӧ����ȡ����ɫ����E����Ҫ��ش��������⣺
��1��д���ڻ�ѧ����ʽ______��
��2��д���ܵ����ӷ���ʽ______��
��3������E�ж���ʵ����һ����______���գ��÷�Ӧ�����ӷ���ʽ��______��
�ο��𰸣���A��ʹʪ��ĺ�ɫʯ����ֽ�������ǰ������������ʣ��ж�ΪNH3��
��һ�������£�A������B��Ӧ����C��C��������Ϊ����ɫ������ɫ����ΪNO2���ж�CΪNO��
��D��Ũ��Һ�����̿���Ҫ�ɷ���MnO2���ڼ��������·�Ӧ����ȡ����ɫ����E���ƶ�DΪŨ���ᣬ����ɫ����EΪCl2��
��D��A������ɰ��̣�˵��AΪNH3��BΪO2����
���������жϳ�������Ϊ��AΪNH3��BΪO2��CΪNO��DΪHCl��EΪCl2��
��1����Ӧ���ǰ����Ĵ���������һ��������ˮ��һ�������Ϳ�����������Ӧ���ɺ���ɫ���������������Ӧ�Ļ�ѧ����ʽΪ��4NH3+5O2����.��4NO+6H2O��2NO+O2=2NO2
�ʴ�Ϊ��4NH3+5O2����.��4NO+6H2O��2NO+O2=2NO2��
��2����Ӧ����ʵ�����Ʊ������ķ�Ӧ�����Ȼ�þ��������ˮ����Ӧ�����ӷ���ʽΪ��MnO2+4H+?��?.?Mn2++Cl2��+2H2O���ʴ�Ϊ��MnO2+2Cl-+4H+?��?.?Mn2++Cl2��+2H2O��
��3������EΪ�����ж������ŷŵ���������Ⱦ��������Ҫ������������Һ���գ���Ӧ�����ӷ���ʽΪ��Cl2+2OH-=Cl-+ClO-+H2O���ʴ�Ϊ��NaOH��Һ��Cl2+2OH-=Cl-+ClO-+H2O��
���������
�����Ѷȣ�һ��