��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��12�֣�T��X��Y��Z��Q��R��WΪ���ڱ�ǰ�����ڵ�Ԫ�أ�ԭ���������ε�������֪��
��W��ԭ������Ϊ29������Ԫ�ؾ�Ϊ����������Ԫ�أ�
��Tԭ�����������������������ֱ�����ԭ��������ȣ�
��X�Ļ�̬ԭ�ӵ���ռ������������ͬ�Ĺ������ÿ�ֹ���еĵ�������ͬ��
��Z�Ļ�̬ԭ�Ӽ۵����Ų�Ϊns2npn+2��
���ڸ�Ԫ�����ڵ������У�Q�Ļ�̬ԭ�ӵĵ�һ��������С��
��R�ĵ��ʳ��³�ѹ�������壬���̬ԭ�ӵ�M������1��δ�ɶԵ�p���ӣ�
��1��X��Y��Q����Ԫ�صĵ縺���ɴ�С��˳����?����Ԫ�ط��ű�ʾ����
��2����Wͬ���ڵ�Ԫ���У�ԭ��������������WԪ��ԭ����ͬ��Ԫ�ػ���?����Ԫ�ط��ţ�����W2+��ȡ[W(YT3)4]2+�����ӷ���ʽΪ?��
��3��T��X��Z����Ԫ����ɵ�һ�ֻ�����M�����Ϸ�������۷�ķ���Һ�к��е����ʣ��׳����ᣬ���ķ���ʽΪXT2Z2����÷��ӵ�Xԭ�Ӳ�ȡ?�ӻ���1mol M�����Цļ��ͦм��ĸ�����Ϊ?��
��4��X��Yԭ�ӽ���γɵ�X3Y4���壬�侧��ṹ����ʯ���ƣ���Ӳ�ȱȽ��ʯ����ԭ����?��
2������� ��ͼ��Ԫ�����ڱ��Ŀ��
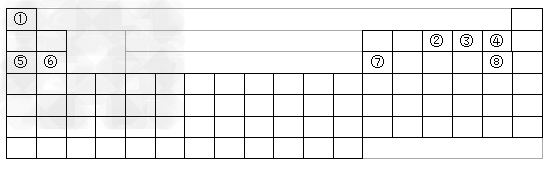
��1��������ͼ�л�������Ԫ�غͷǽ���Ԫ�صķֽ��ߣ������������ԣ���
��2����������Ԫ�����ڱ��Ŀ�����ṩ����Ϣ�ش��������⣨1��2��3�û�ѧʽ��ʾ����?
1���ݺ͢�����Ԫ�ص�����������ˮ�������ǿ��˳����? ��
2��д���ɢ١��ۡ�������Ԫ���γɵ��������ĵ���ʽ? ��
3��ijԪ�صĵ����ڳ����»�ѧ�����ȶ���ͨ������Ϊ��ѧ��Ӧ����������? ��
4��ȫ���ǽ���Ԫ�ص�������? ��ȫ���Ƿǽ���Ԫ�ص�������?��?
?a. ��A��?b. ��A��?c. ��A��? d. ��A��
��3��ijԪ���ǵ������ڵĽ���Ԫ�أ�����ԭ�Ӱ뾶��ͬ���ڵĽ�������С�ģ����Ԫ�صĵ�����NaOH��Һ��Ӧ�����ӷ���ʽ��?��
3��ѡ���� ���л������м������Ӽ����й��ۼ����ǣ�������
A��KBr
B��NH4Cl
C��HF
D��O3
4��ѡ���� ����˵������ȷ���ǣ�������
A����֪�����ۻ���Ϊ6.0kJ?mol-1�������������Ϊ20kJ?mol-1������ÿĦ��������2mol��������ۻ�����ȫ���ڴ��Ʊ�������������ֻ���ƻ�����15%�����
B����֪һ���¶��£�������Һ�����ʵ���Ũ��ΪC�������Ϊ����K��=��C����2/C��1-����������������CH3COONa���壬�����ƽ��CH3COOH�PCH3COO-+H+�����ƶ�������С��K����С
C��ʵ���û����飨l��������ϩ��l�����ͱ���l���ı�ȼ���ȷֱ�Ϊ-3916kJ?mol-1��-3747kJ?mol-1��-3265kJ?mol-1������֤���ڱ������в����ڶ�����̼̼˫��
D����֪��Fe2O3��s��+3C��ʯī��=2Fe��s��+3CO��g����H=489.0kJ?mol-1CO��g��+1/2O2��g��=CO2��g����H=-283.0kJ?mol-1
C��ʯī��+O2��g��=CO2��g����H=-393.5kJ?mol-1��4Fe��s��+3O2��g��=2Fe2O3��s����H=-1641.0kJ?mol-1
5��ѡ���� ������������ȷ����
A��CS2ΪV�εļ��Է���
B��ClO3-�Ŀռ乹��Ϊƽ��������
C��SF6�еĿռ乹��Ϊ����������
D��SiF4��SO32-������ԭ�Ӿ�Ϊsp3�ӻ�