微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 写出CO2气体与Na2O2反应的化学方程式。某学生欲通过实验来探索SO2和Na2O2反应的产物,请你协助完成下列假设与设计:
(1)从SO2和Na2O2双方的性质出发,推测彼此反应的产物,写出虚拟反应式。
(2)画出完成此项实验的装置图。
(3)说明装置各部分所起的作用或添置它的目的。
(4)如何确认二者反应的产物?
参考答案:2CO2+2Na2O2====2Na2CO3+O2? (1)SO2+Na2O2====Na2SO4
(2)见下图:
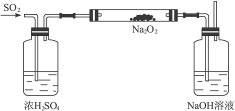
(3)前一洗气瓶中浓硫酸用于干燥SO2,以防水蒸气与Na2O2反应;中间玻璃管用于SO2与Na2O2反应;后一洗气瓶一是吸收未反应的SO2,二是检验有无O2生成。
(4)将Na2O2反应后的固体溶于水后,加盐酸酸化的BaCl2溶液,如有沉淀生成则说明生成的产物为Na2SO4。
本题解析:SO2有较强的还原性,Na2O2有较强的氧化性,二者发生氧化还原反应,产物只能为Na2SO4。
本题难度:简单
2、选择题 经检验,某酸雨的成分除含有少量H+和极少量OH-外,还有Na+、Cl-、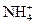 、
、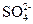 等离子,已知:c(Na+)=7×10-6 mol・ L-1,c(Cl-)=3.5×10-5 mol・ L-1,c(
等离子,已知:c(Na+)=7×10-6 mol・ L-1,c(Cl-)=3.5×10-5 mol・ L-1,c(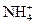 )=2.3×10-5 mol・ L-1,c(
)=2.3×10-5 mol・ L-1,c(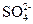 ) =2.5×10-6 mol・L-1,则该酸雨的pH为()
) =2.5×10-6 mol・L-1,则该酸雨的pH为()
A.3
B.4
C.5
D.6
参考答案:C
本题解析:根据溶液呈电中性列出方程式(忽略OH-提供的电荷):
c(Na+)+c(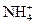 )+c(H+)=c(Cl-)+2c(
)+c(H+)=c(Cl-)+2c(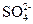 )
)
c(H+)=1.0×10-5 mol・L-1,pH=5。
本题难度:简单
3、选择题 银耳本身为淡黄色,有一种雪耳,颜色洁白如雪,其制作过程是:将银耳放在塑料棚内,在棚一端支个小锅,锅内放硫磺,加热使其熔化并燃烧,两天左右,雪耳就制成了,雪耳炖不烂,且对人有害,制作雪耳利用的是
A.S的还原性
B.S的漂白性
C.SO2的还原性
D.SO2的漂白性
参考答案:D
本题解析:SO2可和有色物质结合生成不稳定的物质而具有漂白性
本题难度:一般
4、选择题 右图是某硫酸试剂瓶的标签上的部分文字。据此,下列说法正确的是?(?)
 ?
?
A.向50mL该硫酸溶液中加入足量的铜片,加热充分反应后,被还原的硫酸的物质的量小于0.46mol
B.1mol Zn与足量的该硫酸反应生成2g氢气
C.该硫酸与等体积水混合所得溶液的物质的量浓度等于9.2mol・L-1
D.该试剂应保存在玻璃试剂瓶中,并用橡胶塞紧
参考答案:A
本题解析:略
本题难度:简单
5、计算题 两份不同浓度的NaOH溶液各500mL,分别吸收1120mL(标准状况下体积)SO2气体,反应后溶液中分别有5.75g和7.10g溶质。求两份NaOH溶液的物质的量浓度。
参考答案:0.150mol/L、0.240mol/L。
本题解析:解答本题时,一要挖掘隐含的两个反应;二要运用平均值规律通过对“5.75g”和“7.10g”的量的分析,判断溶质的组成。
SO2与NaOH作用可能的反应有:
SO2+2NaOH=Na2SO3+H2O;SO2+NaOH=NaHSO3。
1120mLSO2气体可生成0.0500molNa2SO3或NaHSO3,质量是6.30g或5.20g。依题意,两份溶液中,含溶质5.75g的一定含Na2SO3和NaHSO3;含溶质7.10g的一定含Na2SO3和NaOH。
设第一份溶液中含Na2SO3物质的量为x,NaHSO3物质的量为y,则:
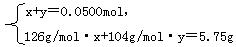
解得? x=0.0250mol,y=0.0250mol。
原溶液中含NaOH物质的量为:
2x+y=0.0750mol,
c(NaOH)=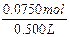 =0.150mol/L。
=0.150mol/L。
依上分析,第二份溶液中含Na2SO30.0500mol,质量是6.30g,则含NaOH的质量为:m(NaOH)=7.10g-6.30g=0.80g。
原溶液中含NaOH物质的量为:
2×0.0500mol+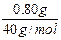 =0.120mol,
=0.120mol,
c(NaOH)=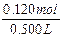 =0.240mol/L。
=0.240mol/L。
本题难度:简单