微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 某温度下,密闭容器中发生反应aX(g)
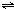
bY(g)+cZ(g),达到平衡后,保持温度不变,将容器的容积压缩到原来容积的一半,当达到新平衡时,物质Y和Z的浓度均是原来的1.8倍.则下列叙述正确的是( )
A.可逆反应的化学计量数数:a>b+c
B.压缩容器的容积时,v正增大,v逆减小
C.达到新平衡时,物质X的转化率减小
D.达到新平衡时,混合物中Z的质量分数增大
参考答案:A.将容器的容积压缩到原来容积的一半,当达到新平衡时,物质Y和Z的浓度均是原来的1.8倍,说明平衡向逆反应方向移动,则应由a<b+c,故A错误;
B.压缩容器的容积,压强增大,正逆反应速率都增大,故B错误;
C.平衡向逆反应方向移动,达到新平衡时,物质X的转化率减小,故C正确;
D.平衡向逆反应方向移动,混合物中Z的质量分数减小,故D错误.
故选C.
本题解析:
本题难度:简单
2、选择题 有一处平衡状态的反应X(s)+3Y(g)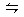 2Z(g)△H<0。为了使平衡向生成Z的方向移动,应采取的措施是(?)
2Z(g)△H<0。为了使平衡向生成Z的方向移动,应采取的措施是(?)
①升高温度;②降低温度;③增大压强;④减小压强;⑤加入催化剂;⑥及时分离出Z。
A.①③⑤
B.②③⑤
C.②③⑥
D.②④⑥
参考答案:C
本题解析:此题考查外界条件对平衡移动的影响。解这类题目,关键是分析反应的特点,依此进行判断。对于X(s)+3Y(g)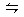 2Z(g)△H<0,正反应方向是体积减小,放热的反应。由此,要使平衡向生成Z的方向移动,可采取降低温度、增大压强和及时分离出Z等措施。
2Z(g)△H<0,正反应方向是体积减小,放热的反应。由此,要使平衡向生成Z的方向移动,可采取降低温度、增大压强和及时分离出Z等措施。
本题难度:一般
3、选择题 在温度相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下(已知CO(g)+2H2(g) CH3OH(g)? ΔH=-90.7 kJ/mol):
CH3OH(g)? ΔH=-90.7 kJ/mol):
容器
| 甲
| 乙
| 丙
|
反应物投入量
| 1 mol CO、2 mol H2
| 1 mol CH3OH
| 2 mol CH3OH
|
CH3OH的浓度(mol/L)
| c1
| c2
| c3
|
反应的能量变化
| 放出a kJ
| 吸收b kJ
| 吸收c kJ
|
平衡时压强(Pa)
| P1
| P2
| P3
|
反应物转化率
| α1
| α2
| α3
|
下列说法不正确的是
A.c1=c3?B.a+c/2<90.7? C.2P2>P3 ?D.α1+α3=1
参考答案:AD
本题解析:根据甲和乙的投入量可知,这两个平衡是等效的,因此平衡时c1=c2,α1+α2=1,a+c=90.7。丙相当于在乙的基础上将容器的体积缩小一半,平衡向生成甲醇的方向移动,所以c1=c2<2 c3,α1+α3<1,2P2>P3,a+c/2<90.7,A、D不正确,BC正确。答案选BC
本题难度:一般
4、填空题 (14分)(1)在一定温度下,向1L体积固定的密闭容器中加入1mol A(g),发生反应2A(g) B(g)+C(g),B的物质的量随时间的变化如图所示。 0―2min内的平均反应速率v(A)= ?. 相同温度下,若开始加入A(g)的物质的量是原来的2倍,则平衡时?是原来的2倍。
B(g)+C(g),B的物质的量随时间的变化如图所示。 0―2min内的平均反应速率v(A)= ?. 相同温度下,若开始加入A(g)的物质的量是原来的2倍,则平衡时?是原来的2倍。
a.平衡常数? b. A的平衡浓度?
c.平衡时混合气体的密度? d.平衡时B的体积分数
(2)实验室用Zn和稀硫酸制取H2,反应时溶液中水的电离平衡??移动(填“向左”“向右”或“不”);若加入少量下列试剂中的??,产生H2的速率将增大。
a.NaNO3? b.CuSO4 ?
c.Na2SO4?d.NaHSO3?
e.? CH3COOH?
(3)用惰性电极电解Cu(NO3)2溶液一段时间后,加入a mol 的Cu(OH)2可使溶液恢复原状,则电解过程中转移的电子数目为_____________
(4)已知:2Zn(s)+O2(g)=2ZnO(s)?△H=-701.0kJ・mol-1
2Hg(l)+O2(g)=2HgO(s)?△H=-181.6kJ・mol-1
则反应Zn(s)+ HgO(s)=ZnO(s)+ Hg(l)?△H=_____________
(5)已知25℃时,Ksp[Cu(OH)2]=2×10-20,要使0.2 mol・L-1 CuSO4溶液中Cu2+沉淀较为完全(使Cu2+浓度降至原来的千分之一),则应向溶液里加入NaOH溶液,使溶液的pH为 。
参考答案:(共14分)(1)0.1mol/(L・min) ; b c (2)向右?; b
(3)4a NA?(4)-259.7 kJ・mol-1?(5)6
本题解析:(1)在0―2min内B增加了0.1mol,则根据反应式A减少了0.2mol,所以起反应速率是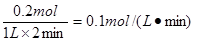 。由于反应前后体积不变,所以若开始加入A(g)的物质的量是原来的2倍,则平衡时A的平衡浓度和平衡时混合气体的密度都是原来的2倍,ac都是不变的,答案选bc。
。由于反应前后体积不变,所以若开始加入A(g)的物质的量是原来的2倍,则平衡时A的平衡浓度和平衡时混合气体的密度都是原来的2倍,ac都是不变的,答案选bc。
(2)锌和稀硫酸反应生成氢气,则溶液中氢离子的浓度降低,所以水的电离平衡向正反应方向移动,即向右移动。b可以构成铜锌原电池,加快反应速率。a中不再产生氢气,b不影响,d会消耗氢离子,近似反应速率。醋酸是弱酸,不能增大氢离子的浓度,答案选b。
(3)入a mol 的Cu(OH)2可使溶液恢复原状,说明在反应中阴极还产生氢气,但阳极始终是OH-放电产生氧气。a mol Cu(OH)2中含有2amol氧原子,所以反应中转移的电子是2amol×2=4amol。
(4)考查盖斯定律的应用,(①-②)÷2即得到Zn(s)+ HgO(s)=ZnO(s)+ Hg(l),所以反应热是(-701.0kJ・mol-1+181.6kJ・mol-1)÷2=-259.7 kJ・mol-1.
(5)根据溶度积常数的表达式可知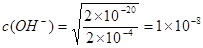 ,则氢离子浓度是
,则氢离子浓度是 ,所以pH=6.
,所以pH=6.
本题难度:一般
5、选择题 反应2A(g)  2B(g)+C(g);ΔH>0,达平衡时,要使V(正)降低、C(A)增大,应采取的措施是(?)
2B(g)+C(g);ΔH>0,达平衡时,要使V(正)降低、C(A)增大,应采取的措施是(?)
A.降温? B.加催化剂? C.升温? D.加压
参考答案:A
本题解析:A 对 降温,反应速率降低,平衡向右移动,C(A)增大,
B 错加催化剂,只改变反应速率,并不影响平衡移动,C(A)不变
C 错 升温,反应速率加快,平衡右移,C(A)减小
D 错 加压,反应速率加快,平衡左移,C(A)增大。
本题难度:简单