��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ԭ������С��36��X��Y��Z��W����Ԫ�أ�����X���γɻ�����������Ԫ�أ�Yԭ�ӻ�̬ʱ���������������ڲ��������2����Zԭ�ӻ�̬ʱ2pԭ�ӹ������3��δ�ɶԵĵ��ӣ�W��ԭ������Ϊ29��
�ش��������⣺
��1��Y2X2������Yԭ�ӹ�����ӻ�����Ϊ______��1mol?Y2X2���ЦҼ�����ĿΪ______��
��2��������ZX3�ķе�Ȼ�����YX4�ĸߣ�����Ҫԭ����______��
��3��Ԫ��Y��һ����������Ԫ��Z��һ�������ﻥΪ�ȵ����壬Ԫ��Z������������ķ���ʽ��______��
��4��Ԫ��W��һ���Ȼ��ᄃ��ľ����ṹ��ͼ��ʾ�����Ȼ���Ļ�ѧʽ��______��������Ũ���ᷢ����������ԭ��Ӧ�����������H2WCl3����Ӧ�Ļ�ѧ����ʽΪ______��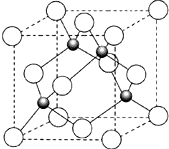
�ο��𰸣�ԭ������С��36��X��Y��Z��W����Ԫ�أ�����X���γɻ�������������Ԫ�أ���X��HԪ�أ�
Yԭ�ӻ�̬ʱ���������������ڲ��������2��������������������8�������ڲ������ֻ����2����Y��CԪ�أ�
Zԭ�ӻ�̬ʱ2pԭ�ӹ������3��δ�ɶԵĵ��ӣ���Z��NԪ�أ�W��ԭ������Ϊ29����W��CuԪ�أ�
��1��Y2X2����Ȳ������ʽΪC2H2��̼��ԭ��֮����ڦҼ���̼̼�����к���һ���Ҽ�������ÿ��̼ԭ�Ӻ���2���Ҽ�����ȡsp�ӻ���һ����Ȳ�����к���3���Ҽ�������1mol?Y2X2���ЦҼ�3mol��3��6.02��1023����
�ʴ�Ϊ��sp�ӻ���3mol��3��6.02��1023����
��2��Nԭ�ӵ縺�Խϴ�Cԭ�ӵ縺�Խ�С�������������д����������������в������������Ĵ��ڵ��°����ķе���ڼ��飬�ʴ�Ϊ��NH3���Ӵ��������
��3��CO2��N2O��ԭ�Ӹ�����ȡ��۵�������ȣ������ǵȵ����壬�ʴ�Ϊ��N2O��
��4�����þ�̯��֪���þ����к�ɫ�����=4����ɫ�����=18��8+12��6=4����ɫ��Ͱ�ɫ��ĸ���֮��=4��4=1��1�����Ը����ʵĻ�ѧʽ��CuCl��������Ũ���ᷢ����������ԭ��Ӧ�����������H2CuCl3������CuCl��H2CuCl3֪���� Ԫ�ء�ͭԪ�صĻ��ϼ۲��䣬���Ը÷�Ӧ����������ԭ��Ӧ���ǻ��Ϸ�Ӧ�������䷴Ӧ����ʽΪCuCl+2HCl�TH2CuCl3����CuCl+2HCl�TH2[CuCl3]��
�ʴ�Ϊ��CuCl��CuCl+2HCl�TH2CuCl3����CuCl+2HCl�TH2[CuCl3]��
���������
�����Ѷȣ�һ��
2������� ��ѡ���⣩���ǵؿ��к�����ߵĽ���Ԫ�أ������е�Ԫ����λ�ӵ���λ��
(1)?AlԪ�ص�ԭ�Ӻ����_______��ͬ�ܼ��ĵ��ӡ�
(2)?Mg��Al��Si����Ԫ�صĵ�һ��������ֵ��С�����˳��Ϊ____________
(3)?AlCl3��NH3��AlCl4�C�о�������λ������AlCl3��NH3�У�������________���ṩ�����ӶԵ�ԭ����_________��AlCl4�C?��Alԭ�Ӳ���________�ӻ���
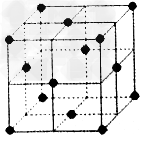
(4)������ľ����ṹ��ͼ��ʾ��һ����������ԭ�ӵ���Ŀ��_________��������һ����ԭ����Χ��֮�����������ȵ���ԭ����Ŀ��_______________
�ο��𰸣�(1)5?
(2)Al<Mg<Si?
(3)NH3��N��sp3?
(4)4��12
���������
�����Ѷȣ�һ��
3��ѡ���� ��������Ԫ���У���̬ԭ�ӹ����ʾʽ�д����ſչ����Ԫ���ж����֡�?
[? ]
A.?1?
B.?2?
C.?3?
D.?4
�ο��𰸣�D
���������
�����Ѷȣ���
4��ѡ���� ���й����ӻ�����������У���ȷ����
[? ]
A�������е�����ԭ��ͨ��sp3�ӻ�����ɼ�ʱ���÷���һ��Ϊ��������ṹ
B��CCl4���������ĸ���ȫ��ͬ��sp3-p�Ҽ�
C���ӻ����һ��ֻ�����γɦҼ�����������δ����ɼ��ŶԵ���
D���ӻ����������VSEPRģ�ͷ������ӵĿռ乹�ͽ�������ì��
�ο��𰸣�BC
���������
�����Ѷȣ�һ��
5������� ��A��B��C��D��E��F����Ԫ�أ�A����������ḻ��Ԫ�أ�B�����ڱ��е縺����ֵ����Ԫ�أ�C�Ļ�̬ԭ����2p���������δ�ɶԵĵ����ӣ�Fԭ�Ӻ����������B��C���������֮�ͣ�D������Ԫ������Eͬ���ڣ�E���γɺ�ɫ����ש��ɫ����E2O�ͺ�ɫ��EO���������D��B���γ����ӻ�����侧���ṹ��ͼ��ʾ����ش��������⡣

|
|
��1��EԪ��ԭ�ӻ�̬ʱ����Χ�����Ų�ʽΪ___________________��
��2��A2F������Fԭ�ӵ��ӻ�������____________��F����̬������FO3���ӵļ���Ϊ____________��
��3��CA3��������ˮ����ԭ����Ҫ��_________________�����ж�CA3����ˮ���γ�CA3��H2O��������ṹΪ_________������ĸ����

��4����ͼ�п��Կ�����D��B�γɵ����ӻ�����ĵ���ʽΪ________________�������ӻ����ᄃ����ܶ�Ϊag�� cm-3�����������_______________��ֻҪ���г���ʽ����
�ο��𰸣���1��3d104s1
��2��sp3��120��
��3����ˮ���Ӽ��γ������b
��4�� ��
��
���������
�����Ѷȣ�����