| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学知识点总结《反应速率与平衡的有关计算》试题强化练习(2017年最新版)(三)
 ①当合成氨反应达到平衡后,改变某一外界条件(不改变N2、H2和NH3的量),反应速率与时间的关系如下图所示。 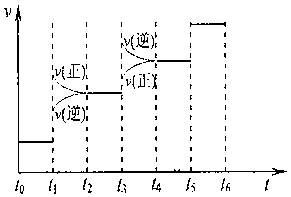 ? ?图t1时引起平衡移动的条件可能是?。 其中表示平衡混合物中NH3含量最高的一段时间是?。 ②温度为T°C时,将3amolH2和amolN2放入带有活塞的密闭容器中,如果活塞能自由移动,充分反应后测得N2的转化率为50%。如果在相同温度下将3amolH2、amolN2和2amolNH3气体放入该容器中,平衡时H2的转化率为?。 4、简答题 [15分]甲烷自热重整是先进的制氢方法,包含甲烷氧化和蒸汽重整。向反应系统同时通入甲烷、氧气和水蒸气,发生的主要化学反应有:
(1)反应CO(g)+H2O(g)  CO2(g)+H2(g)的△H=?kJ/mol。 CO2(g)+H2(g)的△H=?kJ/mol。(2)在初始阶段,甲烷蒸汽重整的反应速率?甲烷氧化的反应速率(填大于、小于或等于)。 (3)对于气相反应,用某组分(B)的平衡压强(PB)代替物质的量浓度(cB)也可以平衡常数(记作KP),则反应CH4(g)+H2O(g)  CO(g)+3H2(g)的KP=?; CO(g)+3H2(g)的KP=?;随着温度的升高,该平衡常数?(填“增大”、“减小”或“不变”)。 (4)从能量阶段分析,甲烷自热重整方法的先进之处在于?。 (5)在某一给定进料比的情况下,温度、压强对H2和CO物质的量分数的影响如下图: 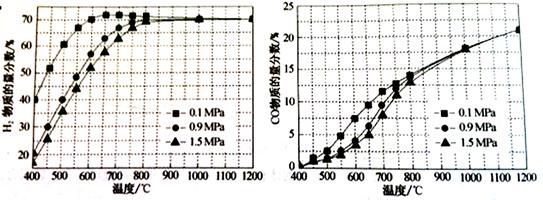 ①若要达到H2物质的量分数>65%、CO的物质的量分数<10%,以下条件中最合适的是?。 A.600℃,0.9Mpa? B.700℃,0.9MPa? C.800℃,1.5Mpa? D.1000℃,1.5MPa ②画出600℃,0.1Mpa条件下,系统中H2物质的量分数随反应时间(从常温进料开始即时) 的变化趋势示意图: 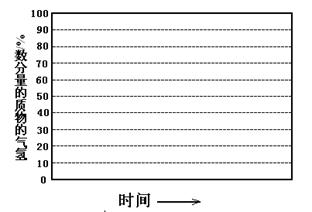 (6)如果进料中氧气量过大,最终导致H2物质的量分数降低,原因是?。 5、填空题 (10分)将6 mol H2和3 mol CO充入容积为0.5 L的密闭容器中,进行如下反应:2 H2(气) + CO(气) |
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高中化学知识点归纳《物质的量》.. | |