��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
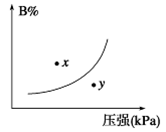
1��ѡ���� ��ӦmA(s)��nB(g) pC(g)����H��0����һ���¶��£�ƽ��ʱB���������(B%)��ѹǿ�仯�Ĺ�ϵ��ͼ��ʾ������������һ����ȷ����
pC(g)����H��0����һ���¶��£�ƽ��ʱB���������(B%)��ѹǿ�仯�Ĺ�ϵ��ͼ��ʾ������������һ����ȷ����
A��n��p
B��x���ʾ������Ӧ����С���淴Ӧ����
C��x���y��ʱ�ķ�Ӧ��������
D���������¶ȣ��÷�Ӧ��ƽ�ⳣ������
2��ѡ���� ��5 mL 0.1 mol��L��1��KI��Һ�еμ�5~6��0.1 mol��L��1��FeCl3��Һ���ٽ�������ʵ�飬���п�֤��FeCl3��Һ��KI��Һ�ķ�Ӧ�ǿ��淴Ӧ��ʵ����
A���ٵμ�AgNO3��Һ���۲��Ƿ���AgI��������
B������CCl4�۲��²�Һ����ɫ
C������CCl4��ȡ�ϲ���Һ���μ�AgNO3��Һ���۲��Ƿ���AgCl��������
D������CCl4��ȡ�ϲ���Һ���μ�KSCN��Һ���۲��Ƿ���Ѫ��ɫ
3��ѡ���� ������������ԭ�����͵��ǣ�?��?
A������ɫ��NO2����ѹ����ɫ�ȱ�����dz
B����ҵ�Ϻϳ�NH3��Ӧʹ�ô���
C��ʵ���ҿ��Բ����ű���ʳ��ˮ�ռ�Cl2
D����H2��I2(g)��HI(g)������ɵ�ƽ����ϵ��ѹ����ɫ����
4������� ��10�֣������ǹ�ҵ��������Ϊ��Ҫ�IJ�Ʒ֮һ���ڴ���Ӧ������еķ�ӦΪ��
2SO2(g)+O2(g) 2SO3(g)?��H=" �C196.6" kJ��mol-1
2SO3(g)?��H=" �C196.6" kJ��mol-1
��1���÷�Ӧ����������ͨ����400~500�桢?��?��
��2��SO3��?�����豸���ƣ�����?�����Լ����ƣ����ա�
��3���о�SO2 ��NO2��CO�ȴ�����Ⱦ����Ĵ���������Ҫ���塣
��֪�� 2NO(g)+O2(g) 2NO2(g)?��H=" �C113.0" kJ��mol-1
2NO2(g)?��H=" �C113.0" kJ��mol-1
��ӦNO2(g)+SO2(g) SO3(g)+NO(g)�Ħ�H=?kJ��mol-1��
SO3(g)+NO(g)�Ħ�H=?kJ��mol-1��
һ�������£���NO2��SO2�����ʵ���֮��1:2���ں����ܱ������з���������Ӧ��������˵����Ӧ�ﵽƽ��״̬����?��
a����ϵѹǿ���ֲ���?
b�����������ɫ���ֲ���
c��SO3��NO������ȱ��ֲ���?
d��ÿ����1 mol SO3��ͬʱ����1 mol NO2
���������Ӧƽ��ʱNO2��SO2�����ʵ���֮��Ϊ1:6����ƽ�ⳣ��K��?��
5��ѡ���� ��25��ʱ���ܱ�������X��Y��Z��������ij�ʼŨ�Ⱥ�ƽ��Ũ�����±���
����
| X
| Y
| Z
|
��ʼŨ��/mol��L-1
| 0.1
| 0.2
| 0
|
ƽ��Ũ��/mol��L-1
| 0.05
| 0.05
| 0.1
|

 ����˵����ȷ���ǣ�
����˵����ȷ���ǣ�
 A����Ӧ�ﵽƽ��ʱ��X��ת����Ϊ60��
A����Ӧ�ﵽƽ��ʱ��X��ת����Ϊ60��
 B����Ӧ�ɱ�ʾΪX+3Y
B����Ӧ�ɱ�ʾΪX+3Y 2Z����ƽ�ⳣ��Ϊ1600
2Z����ƽ�ⳣ��Ϊ1600
 C������ѹǿʹƽ��������Z�ķ����ƶ���ƽ�ⳣ������
C������ѹǿʹƽ��������Z�ķ����ƶ���ƽ�ⳣ������
 D���ı��¶ȿ��Ըı�˷�Ӧ��ƽ�ⳣ��
D���ı��¶ȿ��Ըı�˷�Ӧ��ƽ�ⳣ��