微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列各组元素中,属于同一周期的是
A.碳、氧、硫
B.硅、磷、氯
C.锂、钠、钾
D.氟、氯、溴
参考答案:B
本题解析:考查元素周期表的结构。元素的周期数就是元素原子的电子层数,硅、磷、氯原子核外均有3层,属于第三周期,所以答案选B。
本题难度:简单
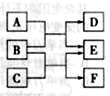
2、选择题 X 、Y、 Z、 W是原子序数依次增大的四种短周期元素,A、B、C、D、F有其中的两种或三种元素组成的化合物,E是由Z元素形成的单质,0.1mol・L-1D溶液的pH为13(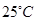 )。它们满足如图转化关系,则下列说法正确的是(?)
)。它们满足如图转化关系,则下列说法正确的是(?)
A.原子半径W>Z>Y>X
B.化合物F中含有共价键和离子键
C.在B和C的反应中,氧化剂是B,还原剂是C
D.Z元素的最高正价为+6
参考答案:B
本题解析:由题意可知D为一元强碱;根据B能与A、C反应生成同种物质且有一元强碱生成推断B是Na2O2,A是H2O,B是CO2,D是NaOH,E是O2,F是Na2CO3,则X、Y、 Z、 W分别是H、C、O、Na元素。A、根据元素周期律中原子半径的比较规律,原子半径W>Y>Z>X,错误;B、Na2CO3中含有共价键和离子键,正确;C、过氧化钠与二氧化碳的反应中,过氧化钠既是氧化剂又是还原剂,错误;D、O无最高正价,错误,答案选B。
本题难度:一般
3、填空题 A、B、C、D、E五种元素在周期表里的位置如下表所示:
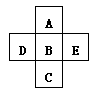
A、B、C为同主族元素,A为该族中原子半径最小的元素;D、B、E为同周期元素,E为该周期中原子半径最小的元素。
C元素名称是 ,D的最高价氧化物对应水化物的化学式 ,实验室制取单质E的化学方程式 ?。
参考答案:硒?磷酸? MnO2+4HCl(浓)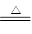 MnCl2+2H2O+Cl2↑
MnCl2+2H2O+Cl2↑
本题解析:根据周期表的结构可知,五种元素位于周期表的右侧,分别是第二、第三和第四周期。E为该周期中原子半径最小的元素,所以E是Cl,则B是S,D是P,A是O,C是Se。实验式制取氯气的化学方程式为MnO2+4HCl(浓)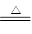 MnCl2+2H2O+Cl2↑。
MnCl2+2H2O+Cl2↑。
本题难度:简单
4、填空题 近期曝出的“毒大米”事件,引起了国人的震惊和忧虑,又一次把环境问题摆在了我们面前。“毒大米”是由镉污染引起的,会对人体健康造成严重危害。镉元素在元素周期表中的图示如图所示。

请回答下列问题:
(1)镉元素的原子序数为?,在元素周期表中的位置是?。
(2)有人说:“‘毒大米’中镉的含量很低,每人每天食用大米量也较少,所以,不会对人体健康造成严重危害。”你对这种说法有何评论??。
(3)你认为“毒大米”中镉的来源是什么??。
(4)镉也是生产电池的重要材料,镉镍二次电池(碱性)的放电和充电反应为:
Cd + 2NiO(OH) + 2H2O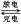 Cd(OH)2+ 2Ni(OH)2
Cd(OH)2+ 2Ni(OH)2
电池的负极是?。
负极的电极反应式为?。
若负极消耗a g反应物,产生N个电子的电量,则阿伏加德罗常数NA=?。
参考答案:(9分)?(1)48(1分)?第五周期第ⅡB族(1分)
(2)长期食用“毒大米”会使镉在人体内累积增多,最终仍然会对人体健康造成严重危害。(1分)
(3)工业生产造成了土壤的镉污染,富集在大米中(1分)
(4)Cd(镉)(1分)? Cd-2e―+2OH―=Cd(OH)2(2分)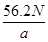 mol―1(2分)
mol―1(2分)
本题解析:(1)镉元素在元素周期表中的图示可知,镉元素的原子序数为48,在元素周期表中的位置是第五周期第ⅡB族。
(2)长期食用“毒大米”会使镉在人体内累积增多,最终仍然会对人体健康造成严重危害,所以这种说法是错误的。
(3)“毒大米”中镉的来源是工业生产造成了土壤的镉污染,富集在大米中。
(4)放电相当于是原电池,原电池中负极失去电子,化合价升高,发生氧化反应。所以根据化学方程式可知,该电池的负极是Cd,负极电极反应式是Cd-2e―+2OH―=Cd(OH)2。agCd的物质的量是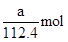 ,在反应中失去
,在反应中失去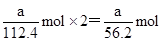 电子,所以阿伏加德罗常数NA=
电子,所以阿伏加德罗常数NA=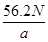 mol―1。
mol―1。
点评:该题以近期曝出的“毒大米”事件为载体,重点考查学生对元素周期表结构、原电池原理以及灵活运用基础知识解决实际问题的能力的培养,有利于调动学生的学习兴趣,激发学生的学习积极性。也有助于培养学生的环境保护意识,增强学生的社会责任感。
本题难度:一般
5、选择题 已知X、Y、Z、W、R是原子序数依次增大的短周期主族元素,X是原子半径最小的元素,Y的最高正价与最低负价的代数和为0,Z的二价阳离子与氖原子具有相同的核外电子排布,W原子最外层电子数是最内层电子数的3倍。下列说法正确的是
A.R的原子半径比Z的大
B.R的氢化物的热稳定性比W的强
C.X与Y形成的化合物只有一种
D.Y的最高价氧化物的水化物的酸性比W的
参考答案:B
本题解析:X、Y、Z、W、R是原子序数依次增大的短周期主族元素,X是原子半径最小的元素,则X为H元素;Z的二价阳离子与氖原子具有相同的核外电子排布,则Z为Mg,W原子最外层电子数是最内层电子数的3倍,最外层电子数为6,结合原子序数可知,W为S,故R为Cl,Y的最高正价与最低负价的代数和为0,处于ⅣA族,原子序数小于Mg,故Y为C元素,A、Z为Mg、R为Cl,二者同周期,原子序数依次增大,原子半径减小,故A错误;B、非金属性Cl>S,故氢化物稳定性HCl>H2S,故B正确;C、H与C元素形成烃类物质,化合物种类繁多,故C错误;D、Y、W的最高价氧化物的水化物分别为碳酸、硫酸,碳酸是弱酸,而硫酸是强酸,故D错误,故选B。
本题难度:一般