��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �����¶�ʱ����ѧ��Ӧ���ʼӿ죬��Ҫ�����ڣ�������
A�������˶����ʼӿ죬ʹ��Ӧ����Ӽ����ײ��������
B����Ӧ����ӵ��������ӣ�����Ӱٷ���������Ч��ײ�������࣬��ѧ��Ӧ���ʼӿ�
C���û�ѧ��Ӧ�Ĺ��������ȵ�
D���û�ѧ��Ӧ�Ĺ����Ƿ��ȵ�
�ο��𰸣������¶�ʱ����ѧ��Ӧ���ʼӿ죬���������¶ȣ���Ӧ����ӵ��������ӣ�����Ӱٷ���������Ч��ײ�������࣬��ѧ��Ӧ���ʼӿ죬����÷�ӦΪ���ȷ�Ӧ����ȷ�Ӧ�أ�
��ѡB��
���������
�����Ѷȣ���
2��ʵ���� �����ӡ�ʵ���У�3I-��S2O82-��I3-��2SO42-�ķ�Ӧ���ʿ�����I3-�����ĵ�����Һ����ɫ��ʱ��t��������tԽС����Ӧ����Խ��ij̽����ѧϰС����20�����ʵ�飬�õ����������±�
ʵ����
��
��
��
��
��
c(I-)/mol��L-1
0.040
0.080
0.080
0.160
0.120
c(SO42-)/mol��L-1
0.040
0.040
0.080
0.020
0.040
t /s
88.0
44.0
22.0
44.0
t2
�ش��������⣺
��1����ʵ���Ŀ����_______________________��
��2����ɫʱ��t2��_____________��
��3���¶ȶԸ÷�Ӧ�ķ�Ӧ���ʵ�Ӱ�����һ����ɣ�����40���½��б�Ţ۶�ӦŨ�ȵ�ʵ�飬��ɫʱ��t2�ķ�ΧΪ_____________������ĸ��
A <22��0s B 22��0��44��0s C ��44��0s D ���ݲ��㣬���ж�
��4��ͨ�������Ƚ��ϱ����ݣ��õ��Ľ�����__________________________
�ο��𰸣���1���о���Ӧ��I-��S2O82-��Ũ�ȶԷ�Ӧ���ʵ�Ӱ��
��2��29.3s
��3��A
��4����Ӧ�����뷴Ӧ����ʼŨ�ȳ˻������ȣ�����ɫʱ���뷴Ӧ����ʼŨ�ȳ˻��ɷ��ȣ�
���������
�����Ѷȣ�һ��
3��ѡ���� ����˵������ȷ����
[? ]
A��Ǧ�����ڷŵ�����У�����������С��������������
B�������£���ӦC(s) +CO2(g)=2CO(g)�����Է����У���÷�Ӧ�ġ�H >O
C�� һ�������£�ʹ�ô����ܼӿ췴Ӧ���ʲ���߷�Ӧ���ƽ��ת����
D����ͬ�����£���Һ��Fe3+��Cu2+��Zn2+�����������μ���
�ο��𰸣�AC
���������
�����Ѷȣ�һ��
4��ѡ���� ������Fe����һ���������ᷴӦ��Ϊ�˼�����Ӧ���ʣ����ֲ�Ӱ�����������������Ӧ�������������еģ�������
A��NaNO3��Һ
B��NaCl����
C��Na2SO4��Һ
D��CuSO4��ĩ
�ο��𰸣����ݷ����ķ�ӦΪFe+2H+�TFe2++H2�������С�����ӵ�Ũ�ȶ����ı������ӵ����ʵ����������������Ӧ���ʣ����ֲ�Ӱ�����������������
A������NaNO3��Һ��Fe����������ӡ������ӷ���������ԭ��Ӧ����NO������������������A����
B������NaCl���壬�Է�Ӧ��Ӱ�죬���������Ӧ���ʣ���B����
C������Na2SO4��Һ�������Ʋ����뷴Ӧ����Һ�������������ӵ�Ũ�ȼ�С���������ӵ����ʵ���û�б仯����Ӧ���ʼ��������ֲ�Ӱ�������������������C��ȷ��
D������CuSO4������Fe��Cu������ԭ��أ��ӿ췴Ӧ���ʣ���D����
��ѡC��
���������
�����Ѷȣ�һ��
5�������� ���淴Ӧ�ã����ȣ��ϣ��磩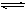 �ãϣ��磩���ȣ����磩����H=���ѡ��ﵽƽ��ı��¶�ʹƽ�ⷢ���ƶ��������ƽ����Է���������α仯?
�ãϣ��磩���ȣ����磩����H=���ѡ��ﵽƽ��ı��¶�ʹƽ�ⷢ���ƶ��������ƽ����Է���������α仯?
�ο��𰸣��𰸼�����
����������÷�Ӧ�е��¶ȸı�ʹƽ���ƶ�ʱ��ÿ���ӣ����С��1mol���������죩���壬��������������ӣ����С��12�磨��12���磩
������ԭƽ��ʱ�����������Ϊ��������12���������������ʵ���Ϊ��������
��������?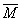 ���������
���������
�������¶����ߡ�ƽ�����ƺ�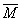 ��������12�������������?
��������12�������������?
�������¶Ƚ��͡�ƽ�����ƺ�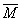 ��������12�������������
��������12�������������
������1���¶�����ƽ������ʱ��
����[������12�������������]�����������[����12�����]��[������]
�������ۣ�
������������12���12�����0?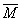 ����
����
������������12���12�����0?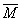 ���䣻
���䣻
������������12���12�����0?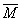 ����
����
������2���¶Ƚ���ƽ������ʱ��
�������ۣ�
������������12���12�����0?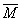 ����
����
������������12���12�����0?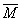 ���䣻
���䣻
��������12���12�����0?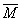 ����
����
�����Ѷȣ���