| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学知识点整理《原电池原理》在线测试(2017年最新版)(八)
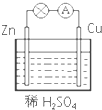 参考答案:该原电池中,锌易失电子而作负极,铜作正极,正极上氢离子得电子发生还原反应,电极反应式为:2H++2e-=H2↑,故选C. 本题解析: 本题难度:一般 2、选择题 关于下列各装置图的叙述中,正确的是( ) 参考答案:A、原电池中电流的方向是从正极流向负极,所以该电解池中a是阳极,b是阴极,电解精炼铜时,阳极材料是粗铜,阴极材料是纯铜,故A错误; 本题解析: 本题难度:简单 3、选择题 锂电池的构造如图所示,电池内部“→”表示放电时Li+的迁移方向,电池总反应可表示为:Li1-xCoO2+LixC6 |
参考答案:B
本题解析:A、放电时,负极上失电子化合价升高,发生氧化反应,所以LiCoO2为电池的负极,故A正确;B、干冰是固体二氧化碳,为非电解质,故B错误;C、充电时,阴极发生还原反应化合降低,所以电极反应式为Li1-xCoO2+xLi++xe-
本题难度:一般
4、选择题 铅蓄电池中的总反应为Pb+PbO2+2H2SO4 ?2PbSO4+2H2O,下列说法正确的是
?2PbSO4+2H2O,下列说法正确的是
A.在放电时,正极发生的反应是 Pb(s) +SO42-(aq)= PbSO4(s) +2e-
B.在放电时,电池的负极材料是铅板
C.在充电时,电池中硫酸的浓度不断变小
D.在充电时,阳极发生的反应是 PbSO4(s)+2e-=" Pb(s)+" SO42-(aq)
参考答案:B
本题解析:略
本题难度:一般
5、选择题 标况下,电解一定物质的量浓度的CuSO4溶液一段时间后,加入0.2molCu(OH)2固体使溶液完全恢复到初始状态,则此过程中共产生气体( )
A.6.72L
B.8.96L
C.11.2L
D.5.6L
参考答案:Cu(OH)2从组成上可看成CuO?H2O,加入0.2mol Cu(OH)2固体使溶液完全恢复到初始状态,根据“出什么加什么”的原则知,电解析出的物质是氧气、铜和氢气,根据原子守恒得:氧元素全部生成形成氧气,氢元素全部形成氢气,根据氢氧化铜中氢氧元素计算氢气和氧气的体积.
设生成氧气的体积为x,氢气的气体为y.
根据原子守恒,氢氧化铜和氧气、氢气的关系式为:
Cu(OH)2-----O2
1mol? 22.4L
0.2mol? x
x=4.48L
Cu(OH)2---H2
1mol? 22.4L
0.2mol? y
y=4.48L
所以共产生的气体体积=x+y=4.48L+4.48L=8.96L
故选B.
本题解析:
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高中化学必备知识点《化学反应速.. | |