��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ����˵����ȷ���ǣ�������
A��������ֻ�������ԣ�������ֻ�л�ԭ��
B��ʧ�����ѵ�ԭ�ӻ�õ��ӵ�����һ��ǿ
C���õ�����Խ������������������Ծ�Խǿ
D��Ҫʵ��Fe2+��Fe3+��ת�����������������
�ο��𰸣�A�������ӿ����л�ԭ�ԣ���Fe2+�������ӿ����������ԣ�������������MnO4-����A����
B��ʧ�����ѵ�ԭ�ӻ�õ��ӵ�������һ��ǿ����Ar����B����
C����������������ǿ���Ǹ��ݵõ������׳̶��жϵģ����Ǹ��ݵõ��Ӷ����жϵģ����Եõ�����Խ������������������Բ�һ��ǿ����C����
D��Ҫʵ��Fe2+��Fe3+��ת�����ڷ�Ӧ����������ʧ��������ԭ���������������������������������������ӣ���D��ȷ��
��ѡD��
���������
�����Ѷȣ�һ��
2������� ��1��������ԭ��Ӧ��ʵ����______����Ӧ����ijԪ�صĻ��ϼ۽��ͣ�������Ԫ�ص�ԭ��______���ӣ��ʧȥ�������õ�����������Ԫ�ص����ʷ���______��Ӧ���������Ӧ��������ԭ��Ӧ����
��2����˫���ŷ����ʵ������ȡCl2�Ļ�ѧ��Ӧ����ʽ�е���ת�Ƶķ������Ŀ
MnO2+4HCl��Ũ��
MnCl2+Cl2��+2H2O
����HCl��______�����������������ԭ���������Ȳ���������Ҳ���ǻ�ԭ����������������Ԫ��Ϊ______��
�ο��𰸣���1��������ԭ��Ӧ���������õ��ӻ�ԭ��ʧ���ӣ����Է�Ӧʵ���Ƿ�Ӧ���е��ӵ�ת�ƣ����Ӵ�����ɣ����Ԫ�صõ��ӣ����Ӹ���ɴ�������ɣ������Ӵ����磬�õ��ӵ���������������������ԭ��Ӧ��
�ʴ�Ϊ����Ӧ���е���ת�ƣ��õ�����ԭ��Ӧ��
��2���÷�Ӧ�ж������̵õ��������������Ȼ�������Ԫ��ʧ���ӻ��ϼ����ߣ�������Ԫ�ر����������Ȼ�������ԭ����1mol��������ʧȥ2mol���ӣ�1mol�μ�������Ӧ���Ȼ���ʧȥ1mol���ӣ�������ת�Ƶ��ӵ����ʵ�����2mol�����ԭ���غ���ƽ����ʽ��������˫���ű������ת�Ƶķ������ĿΪ
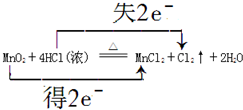
��
�ʴ�Ϊ��

����ԭ�����ȣ�Cl����
���������
�����Ѷȣ�һ��
3��ѡ���� ���з�Ӧ�У����ǻ��Ϸ�Ӧ������������ԭ��Ӧ���ǣ�������
��1������������Ӧ��2Fe+3Cl2�T2FeCl3
��2������ͨ���廯����Һ��Cl2+2NaBr�T2NaCl+Br2
��3���Ȼ�����Һ��Ũ�����ϼ��ȣ�2NaCl+H2SO4��Ũ���TNa2SO4+2HCl��
��4���������̸�Ũ�����ڼ��������·�Ӧ��MnO2+4HCl��Ũ���TMnCl2+Cl2��+2H2O
��5��������������ȼ�գ�H2+Cl2�T2HCl��
A����1����2��
B����1����3��
C����1����4��
D����1����5��
�ο��𰸣���1������������Ӧ��2Fe+3Cl2�T2FeCl3����Ԫ�ء���Ԫ�صĻ��ϼ۶������仯��������������ԭ��Ӧ��������������������һ�����ʣ�����Ҳ�ǻ��Ϸ�Ӧ��
��2������ͨ���廯����Һ��Cl2+2NaBr�T2NaCl+Br2����Ԫ�ء���Ԫ�صĻ��ϼ۶������仯��������������ԭ��Ӧ��ͬʱ�����û���Ӧ��
��3���Ȼ�����Һ��Ũ�����ϼ��ȣ�2NaCl+H2SO4��Ũ���TNa2SO4+2HCl���У���Ԫ�ػ��ϼ۶����䣬���Բ���������ԭ��Ӧ�����ڸ��ֽⷴӦ��
��4���������̸�Ũ�����ڼ��������·�Ӧ��MnO2+4HCl��Ũ���TMnCl2+Cl2��+2H2O����Ԫ�ء���Ԫ�ػ��ϼ۶������仯��������������ԭ��Ӧ�������ǻ��Ϸ�Ӧ��
��5��������������ȼ�գ�H2+Cl2�T2HCl����Ԫ�غ���Ԫ�ػ��ϼ۶������仯��������������ԭ��Ӧ�������ڻ��Ϸ�Ӧ��
��ѡD��
���������
�����Ѷȣ���
4��ѡ���� X��Y��Z��ԭ���������ε����Ķ�����Ԫ�أ�3��Ԫ�ص�ԭ�Ӻ��������֮����Ca2+�ĺ����������ȣ�X��Z�ֱ�õ�һ�����Ӻ���γ�ϡ������ԭ�ӵ��ȶ����Ӳ�ṹ������˵����ȷ���ǣ�������
A��ԭ�Ӱ뾶��Z��Y��X
B��Z��X�γɻ�����ķе����Z��ͬ��Ԫ����X�γɻ�����ķе�
C��CaY2��ˮ����������ԭ��Ӧʱ��CaY2ֻ��������
D��CaX2��CaY2��CaZ2��3�ֻ������У��������������Ӹ����Ⱦ�Ϊ1��2
�ο��𰸣�X��Y��Z��ԭ���������ε����Ķ�����Ԫ�أ�3��Ԫ�ص�ԭ�Ӻ��������֮����Ca2+�ĺ����������ȣ�3��Ԫ�صĺ��������֮��Ϊ18��Z�õ�1�����ӱ��8���ӽṹ����ZΪFԪ�أ���X��Yһ��������һ��λ�ڵ�2���ڣ�X�õ�һ�����Ӻ���γ�ϡ������ԭ�ӵ��ȶ����Ӳ�ṹ����XΪHԪ�أ�YԪ��ԭ�Ӻ��������Ϊ18-1-9=8����YΪOԪ�أ�
A��X��Y��Z�ֱ���H��O��F��ͬ�����������ԭ�Ӱ뾶�����Ӳ�Խ��ԭ�Ӱ뾶Խ��ԭ�Ӱ뾶O��F��H����A����
B��HF����֮�京��������е��������ͬ���⻯��ķе㣬��B��ȷ��
C������������ˮ��Ӧ���������Ƽ������������ǻ�ԭ������C����
D��CaO2��������ΪO22-�����������Ӹ�����Ϊ1��1����D����
��ѡB��
���������
�����Ѷȣ���
5��ѡ���� ʵ�����б仯��һ��Ҫ�����������������������ǣ�������
A��CaCO3��CO2
B��NaCl��NaNO3
C��Zn��ZnCl2
D��Cl2��HCl
�ο��𰸣�A����Ԫ�صĻ��ϼ۶�û�з����仯������������ԭ��Ӧ�����������ʵ�ַ�Ӧ����A����
B��ͨ�����ֽⷴӦ��ʵ��ת���������������������B����
C��ZnԪ�ػ��ϼ����ߣ����������������ʵ�֣���C��ȷ��
D��ClԪ�ػ��ϼ۽��ͣ�����뻹ԭ������ʵ�֣���D����
��ѡC��
���������
�����Ѷȣ���