微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 某元素的一个原子形成的离子可表示为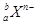 ,下列说法正确的是
,下列说法正确的是
A.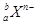 含有的中子数为a+b
含有的中子数为a+b
B.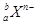 含有的电子数为a-n
含有的电子数为a-n
C.X原子的质量数为a+b+n
D.X原子的质量约为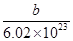 g
g
参考答案:D
本题解析:在表示原子组成时元素符号的左下角表示质子数,左上角表示质量数。因为质子数和中子数之和是质量数,所以A、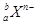 含有的中子数为b-a,A不正确;B、质子数=核外电子数,则该微粒的电子数=a+n,B不正确;C、X原子的质量数为b,C不正确;D、由于X原子的质量数为b,则1mol该原子的质量是bg。由于1mol该原子含有的原子个数是6.02×1023,所以X原子的质量约为
含有的中子数为b-a,A不正确;B、质子数=核外电子数,则该微粒的电子数=a+n,B不正确;C、X原子的质量数为b,C不正确;D、由于X原子的质量数为b,则1mol该原子的质量是bg。由于1mol该原子含有的原子个数是6.02×1023,所以X原子的质量约为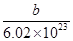 g,D正确,答案选D。
g,D正确,答案选D。
本题难度:一般
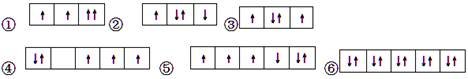
2、选择题 以下是一些原子的2p能级和3d能级中电子排布的情况。其中违反了洪特规则的是
A.①
B.①③
C.②④⑤
D.③④⑤
参考答案:C
本题解析:当电子排布在同一个能级的不同轨道时,基态原子中的电子总是单独优先占据一个轨道,而且自旋状态相同,称为洪特规则,据此可以判断。①同一轨道自旋方向相同,违反泡利不相容原理;②不同轨道的单电子自旋方向不同,违反了洪特规则;③符合洪特规则;④应优先占据不同的轨道,每个轨道有1个电子,违反了洪特规则;⑤不同轨道的单电子自旋方向不同,违反了洪特规则;⑥符合洪特规则,所以其中违反了洪特规则的是②④⑤,答案选C。
本题难度:一般
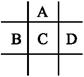
3、填空题 有A、B、C、D、E五种短周期元素,已知相邻的A、B、C、D四种元素原子核外共有56个电子,在周期表中的位置如图所示。E的单质可与酸反应,1 mol E单质与足量酸作用,在标准状况下能产生33.6 L H2;E的阳离子与A的阴离子核外电子层结构完全相同。
回答下列问题:
(1)A与E形成的化合物的化学式是 。?
(2)B的最高价氧化物化学式为 ,C的元素名称为 ,D的单质与水反应的方程式为 ____________________________
(3)向D与E形成的化合物的水溶液中滴入烧碱溶液直至过量,观察到的现象是
_____________________________________________________
有关反应的离子方程式为___________________________
参考答案:(1)Al2O3(1分)
(2)P2O5(1分) 硫(1分) Cl2+H2O HCl+HClO(2分)
HCl+HClO(2分)
(3)先有白色胶状沉淀产生并逐渐增多,随NaOH溶液的加入又逐渐溶解最终澄清(2分)
Al3++3OH-=Al(OH)3↓(2分),Al(OH)3+OH-=Al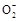 +2H2O(2分)
+2H2O(2分)
本题解析:设A、B、C、D四种元素原子的电子数分别为x-8、x-1、x、x+1,则(x-8)+(x-1)+x+(x+1)=56,x=16,A、B、C、D分别为O、P、S、Cl。根据1 mol E与足量酸反应生成的H2的体积为33.6 L,可知E为铝元素。
本题难度:一般
4、选择题 A、B为短周期元素,二者能形成A2B3型化合物。若A阳离子比B阴离子少一层电子层,且B的原子序数为n,则A的原子序数是
A. n-3? B. n+3? C. n+5? D. n-5
参考答案:A
本题解析:略
本题难度:简单
5、选择题 我国的“神州五号”载人飞船已发射成功,“嫦娥”探月工程已正式启动。据科学家预测,月球的土壤中吸附着数百万吨的32He,每百吨32He核聚变所释放出的能量相当于目前人类一年消耗的能量。在地球上,氦元素主要以42He的形式存在。下列说法不正确的是
A.42He原子核内含有2个质子
B.32He和42He互为同位素
C.32He原子核内含有1个中子
D.42He的最外层电子数为2,所以42He具有较强的金属性
参考答案:D
本题解析:在表示原子组成时元素符号的左下角表示质子数,左上角表示质量数,所以选项A、C都是正确;质子数相同而中子数不同的同一种元素的不同核素互为同位素,所以B正确;He是稀有气体元素,没有很强的金属性,选项D不正确,答案选D。
本题难度:一般