微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列关于合金的说法错误的是(? )
A.镁铝合金的熔点比镁和铝都髙
B.钠钾合金作为原子反应堆导热材料主要因为其液态范围宽和比热大
C.在合金中加入适量的稀土金属能大大改善其性能
D.青铜、硬铝、钢都是合金
参考答案:A
本题解析:合金的熔点一般低于其成分金属的熔点,A不正确,其余选项都是正确的,答案选A。
点评:该题是基础性试题的考查与训练,主要是考查学生对合金概念、组成、性能的了解掌握程度,有利于培养学生的逻辑思维能力和发散思维能力,通过学生的答题效率。
本题难度:简单
2、选择题 Na、Al、Fe、Cu是中学化学中重要的金属元素,它们的单质及其化合物之间有很多转化关系,如通常所说的“铁三角”、“铝三角”等。下表所列物质不能按如图(“→”表示一步完成)关系相互转化的是

选项
| A
| B
| C
| D
|
A
| Na
| Al
| Fe
| Cu
|
B
| NaOH
| Al2O3
| FeCl3
| CuSO4
|
C
| NaCl
| Al(OH)3
| FeCl2
| CuCl2
参考答案:B
本题解析:Na→NaOH,Na与水反应;NaOH→NaCl,NaOH与HCl反应;NaCl→Na,电解熔融状态下的NaCl,A正确;Fe→FeCl3,Fe与Cl2反应;FeCl3→FeCl2,FeCl3与Fe反应;FeCl2→Fe,FeCl2与Zn反应,C正确;Cu→CuSO4,Cu与Ag2 SO4反应;CuSO4→CuCl2,CuSO4与BaCl2反应;CuCl2→Cu,CuCl2与Fe反应,D正确;Al→Al2O3,Al与氧气反应;Al2O3→Al(OH)3,是无法实现的,因为Al2O3与少量或过量的NaOH反应,都是生成偏铝酸钠。答案选B
点评:金属及其化合物是重要的无机物,是历年高考的重点。考生在备考过程中应注意积累各物质的性质及重要的化学反应。
本题难度:一般
3、实验题 为证明Fe3+具有较强的氧化性,甲同学做了如下实验:将Cu片放入Fe(NO3)3溶液中,观察到Cu片逐渐溶解,溶液由黄色变为蓝绿色,由此甲同学得到Fe3+具有较强氧化性的结论。乙同学提出了不同的看法:“Fe(NO3)3溶液具有酸性,在此酸性条件下NO3-也能氧化Cu”,并设计实验进行探究。
已知:
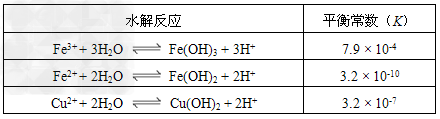
请回答:
(1)稀硝酸和Cu反应的化学方程式为________________。
(2)请利用所提供的试剂,帮助乙同学完成实验方案设计。 ?
试剂:0.5mol/L?Fe(NO3)3溶液、Cu片、精密pH试纸(0.5~5.0)、稀硝酸 ?
方案:__________________________________
(3)丙同学分别实施了甲、乙两位同学的实验方案,并在实验过程中用pH计监测溶液pH 的变化,实验记录如下。

①根据实验现象写出发生反应的离子方程式_____________________。
②导致实验过程中溶液pH略有上升的可能原因是______________________。
(4)请你设计更简便可行的实验方案,帮助甲同学达到实验目的:?_______________。
参考答案:(1)3Cu?+?8HNO3?==?3Cu(NO3)2?+?2NO↑?+?4H2O
(2)测定硝酸铁溶液的pH,再配制相同pH的硝酸,将铜片加入硝酸中,观察二者是否反应
(3)①?Cu?+?2Fe3+?==?Cu2+?+?2Fe2+?;②?Fe3+?变为Cu2+和Fe2+,水解能力下降
(4)将铜片放入氯化铁溶液中
本题解析:
本题难度:一般
4、选择题 取χg铜和镁的合金完全溶于浓硝酸,若反应中硝酸被还原只产生8960mL的NO2气体和672mL的N2O4气体(都已折算到标准状况),在反应后的溶液中,加入足量的氢氧化钠溶液,生成沉淀的质量为17.02g,则χ等于
A.8.64g
B.9.20g
C.9.00g
D.9.44g
参考答案:B
本题解析:略
本题难度:简单
5、选择题 元素X的单质及X与Y形成的化合物能按如下图所示的关系发生转化,则X为?

[? ]
A.Fe?
B.Cu?
C.S?
D.C?
参考答案:A
本题解析:
本题难度:一般
|