| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学必考知识点《水的电离平衡》试题特训(2017年最新版)(四)
参考答案:B 本题解析:A.水的电离是吸热过程。将纯水加热到90 ℃,可以促进水的电离,C(H+)增大,溶液的PH减小。小于7.错误。B. 向水中加少量Na2CO3溶液发生反应H2O+CO32- 本题难度:一般 5、选择题 在常温下,将pH=8的NaOH溶液与pH=10的NaOH溶液等体积混合后,溶液的pH最接近于: |
参考答案:D
本题解析: 将pH=8的NaOH与pH=10的NaOH溶液等体积混合后,溶液中OH-的浓度是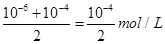 ,则根据水的离子积常数可知c(H+)=
,则根据水的离子积常数可知c(H+)=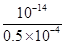 =2×10-10 mol/L,根据pH计算公式计算等pH为9.7.答案选D。
=2×10-10 mol/L,根据pH计算公式计算等pH为9.7.答案选D。
考点:考查强间混合时氢离子浓度的有关计算
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学知识点整理《醇》高频试.. | |