��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ʵ���� ij��ѧ��ѧ�о���ѧϰС����������װ����ȡ��̽������������
[A�з�����Ӧ�Ļ�ѧ����ʽ��2NH4Cl+Ca(OH)2 2NH3��+2H2O+CaCl2] ��
2NH3��+2H2O+CaCl2] ��

��ʵ��̽����
(1)A�еķ�Ӧ___����ǡ����ǡ���������ԭ��Ӧ��
(2)Aװ�û���������ȡ____���壨ֻ��һ�֣���
(3)����10.7 g NH4Cl���壬������ȡNH3����״�����������____L(NH4Cl ��Ħ������Ϊ53.5
g��mol-1)��
(4)ʵ�����ռ������ķ�����___��
(5)C��Dװ������ɫ�ᷢ���仯����___(�C����D��)��
(6)��ʵ�����һ��ʱ���ѹEװ���еĽ�ͷ�ιܣ�����1~2��Ũ���ᣬ�ɹ۲쵽��������___��
(7)Ϊ��ֹ����������ɿ�����Ⱦ����Ҫ������װ�õ�ĩ������һ��β������װ�ã����ʵ�װ����____���F����G������
��֪ʶ��չ��
(8)��ʯ����ˮ��Ӧ����Ca(OH)2���ų�����[��ѧ����ʽΪCaO+H2O==Ca(OH)2]��ʵ�������ô�ԭ��������ʯ���еμ�Ũ��ˮ�����Կ�����ȡ����������Ϊ��ʯ�ҿ������� ___���ʴ��棨����ţ���
A����ʯ��(NaOH��CaO�Ĺ�������)
B��NaOH����
C��������Һ
D��ʯ��ʯ(CaCO3)
��֪ʶӦ�á�
(9) 2010��11��9��������ʡ������һ�䶳����������й©�¼���500�������ҹ��ת�ơ����������ֳ���������ʲô�Ծȷ�����
�ο��𰸣�(1)����
(2) O2�������������������𰸼��ɣ�?
(3)4. 48
(4)�����ſ�����
(5)D
(6)�������
(7)F
(8)A B
(9)
����ʪë����ס�ڱǣ���Ѹ�ٳ��롣
�ڵ�ͷ���������ʹ��ܣ�Ѹ�ٳ��롣
����籼�ܣ�Ѹ�ٳ��롣
�ܴ��Ϸ�����ߣ�Ѹ�ٳ��롣
���������
�����Ѷȣ�һ��
2��ʵ���� ��14�֣�������һ������Ⱥ��ϲ���Ĵ�ͳʳƷ���ڰ����������һֱռ����Ҫλ�á�����������������������ʮ���ձ飬��Ӱ��Ⱥ�ڽ�����ʳƷ��ȫ��������2009��5����Ѯ��ʼ���㽭ʡ�������ӹ�ͣ�ú���ʳƷ�����Ӽ�����ת��Ϊ�������Ӽ��䷽���գ��Ӷ���֤���ճ��ϰ�ȫ�����ĵ����������������䷽��̼�����ƣ�С�մ�̼����泥����ۣ���ɡ�Ϊ�ⶨ������С�մ����������w��NaHCO3����ʵ��С��ͬѧ���������װ�ý���ʵ�顣
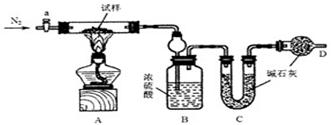

ʵ�����
�ٰ�ͼ��װ���������װ�õ������ԣ�
�ڽ�����m1g����Ӳ�ʲ������У�װ��B��C��D��ҩƷ��ͼ����֪��ҩƷ��װ��B������Ϊm2g��װ��C������Ϊm3g��
�۹رջ���a����ȼ�ƾ��Ƽ���������ֱ��Bװ����������ð������a��װ����ͨ��N2��һ��ʱ������ƾ��ƣ��رջ���a��
�ܳƵ�װ��B������Ϊm4g��װ��C������Ϊm5g��
��ش��������⣨װ����ԭ�п�����ʵ���Ӱ����Բ��� ����
����
��1��װ��A�з�����Ӧ�Ļ�ѧ����ʽΪ?��?��
��2��װ��B������Ϊ?��?��
װ��C������Ϊ?��?��
��3��ʵ�������ͨ��N2��Ŀ��Ϊ?��?��
��4�������и������ṩ�������ܼ����w��NaHCO3�����ǣ�?��?������ѡ����ĸ��
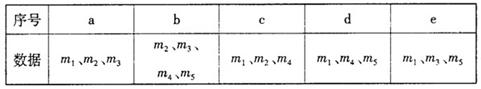
��5��ʵ���������װ��A��Ӳ�ʲ������Ҷ���ˮ�飬����Ϊ����ʵ�������ṩ�����ݻ��ܷ�õ�ȷ��w��NaHCO3��?��?����ܡ����ܡ��������ܣ���w��NaHCO3���ļ���ʽΪ��?��?�������ܣ����ʲ�����
�ο��𰸣�
��1��2NaHCO3 Na2CO3 + CO2 + H2O (2��)��NH4HCO3
Na2CO3 + CO2 + H2O (2��)��NH4HCO3 NH3+ CO2+H2O (2��)
NH3+ CO2+H2O (2��)
��2�����շ�Ӧ���ɵ�ˮ�����Ͱ���(1��) �����շ�Ӧ���ɵ�CO2 (1��)��
��3����װ���е�CO2��NH3��ˮ�����ų���ʹ�䱻װ��B��װ��C��ȫ����(2��)
��4��b��c ��e? (3�֣�ÿ��1�֣�ѡ��һ���һ�֣�������ͷ�0��)?��
��5���ܣ�1�֣���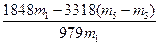 ��100%���ȼ۱���ʽ��(2��)
��100%���ȼ۱���ʽ��(2��)
�����������
�����Ѷȣ�һ��
3��ʵ���� I.ijУ��ѧѧϰС��Ϊ��̽������(H2C2O4)�Ļ�ѧ���ʣ����������ʵ��:
С���Ա����������Һ�����Ը��������Һ��Ӧʵ��ʱ���֣���Һ��ɫ������졣
��1������H2C2O4��Һ������KMnO4��Һ��Ӧ�����ӷ���Ϊ?��
��2��Ϊ��̽���˷�Ӧ������С����ԭ��ͬѧ��������ʵ�飨���С�һ����ʾδ������Լ�����
ʵ��
���
| ��Ӧ�¶�
(����ˮԡ����)
| ϡ����
��Һ
| MnSO4����
| 0.10 mol/L
KMnO4��Һ
| ��ɫ
ʱ��
|
1
| 750C
| һ
| һ
| 1mL
| 100s
|
2
| 750C
| 10��
| һ
| 1mL
| 40s
|
3
| 750C
| 10��
| ��������
| 1mL
| 3s
|
��ͬѧ�ɴ��ܹ��ó�����:??
II.��ͬѧ�����ϵ�֪�������и��������Բ����κ�̼���Ρ��� ������ʵ����֤��һ��ʵ���������κ�������һ���������ϵ�֪�����ᣨH2C2O4��������ǿ�ڴ���Ķ�Ԫ���ᣬ��Ӧ�ĸ��Σ�CaC2O4�������ڴ��ᣬ������ǿ�ᡣ
��1�� ��ȷ�ⶨ�����в����κ������ش��й����⣺
�ٲ�����ȡm g������Ʒ,�����в�����ת��Ϊ CaC2O4 �����������,�������ܽ��,��Һת��100mL����ƿ�м�ˮ���Ƴ�100mL��Һ��ÿ����ȡ25.00mL����Һ����0.0100mol��L��1 KMnO4����Һ�ζ����ζ�ʵ���ظ�����2 ��3�Ρ�ƽ�����ı���ҺV mL��
�ڼ��㣺�����в����Σ���C2O42���ƣ�����������Ϊ?����ֻ��ʽ�����㣬��֪��C2O42���ĵ�Ħ������Ϊ88 g?mol-1��
�����ۣ��ñ�KMnO4��Һֱ�ӵζ�������ĥ�����ݡ����˵õ�����Һ�������ƫ�ߣ�ԭ����??��
�ο��𰸣�I.��1��5H2C2O4+2MnO4?+6H+=2Mn2++10CO2��+8H2O
��2�����Ų�����Һ����������Һ��Ӧ�Ľ��У�������Mn2+��Mn2+��Ϊ�÷�Ӧ�Ĵ��������Լӿ컯ѧ��Ӧ���ʡ�
II����1����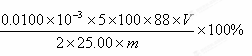
�۲����л�����������ԭ�����ʣ�����KMnO4��Ӧ
���������I����1�����������Һ���������ԣ�����������Ϊ������̼������ԭ���غ�͵���غ���ƽ��д���ӷ���ʽΪ��5H2C2O4+2MnO4-+6H+=2Mn2++10CO2��+8H2O
��2��ͼ���и��������Һ���ȣ���ɫʱ��ϳ�������������������������Ͽ죬��Ӧ��Ҫ��ʱ�����̣�Mn2+�����ã�����ϡ������ɫʱ�����̣�˵�����ɵ������ӶԷֽ����˴����á�
II����1�������ݷ�Ӧ�����ӷ���ʽ���㣬��������ʵ���Ϊx��
5H2C2O4+2MnO4-+6H+=2Mn2++10CO2��+8H2O
5? 2
x? 0.0100mol/L��v��10-3L
�ɵò����в����Σ���C2O42���ƣ�����������Ϊ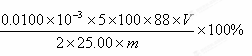
���ñ�KMnO4��Һֱ�ӵζ�������ĥ�����ݡ����˵õ�����Һ�п��ܺ���������ԭ�����ʻ����ĸ�����أ����½������ƫ�ߡ�
�����Ѷȣ�һ��
4��ѡ���� �����й�ʵ�����������ͽ��ͻ���۶���ȷ���� (? )
ѡ��
| ʵ�����
| ����
| ���ͻ����
|
A
| ������Fe���м���ϡHNO3����ַ�Ӧ����KSCN��Һ
| ��Һ�ʺ�ɫ
| ϡHNO3��Fe����ΪFe3��
|
B
| AgI�����е���ϡKCl��Һ
| �а�ɫ��������
| AgCl��AgI������
|
C
| �����£���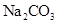 ��Һ�м����� ��Һ�м����� ��ĩ�����ˣ���ϴ���ij����м�ϡ���� ��ĩ�����ˣ���ϴ���ij����м�ϡ����
| �����ݲ���
| ����˵��������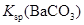
��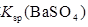 �Ĵ�С��ϵ �Ĵ�С��ϵ
|
D
| �ò�����պȡŨ��ˮ�㵽��ɫʯ����ֽ��
| ��ֽ����ɫ
| Ũ��ˮ�ʼ���
�ο��𰸣�CD
���������
��ȷ�𰸣�C��D
A��3Fe��8HNO3=3Fe(NO3)2��2NO��4H2O����Fe3��������KSCN��Һ�����ʺ�ɫ��
B��AgCl��I�D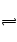 AgI��Cl�D�ǿ��淴Ӧ�� AgI��Cl�D�ǿ��淴Ӧ��
C��CO32�D��BaSO4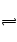 BaCO3��SO42�D,�ǿ��淴Ӧ�����Խ�����ȷ�� BaCO3��SO42�D,�ǿ��淴Ӧ�����Խ�����ȷ��
D������ͽ��۾���ȷ��
�����Ѷȣ���
5��ѡ���� ���н�����ȷ����?��?��
�ο��𰸣�D
�����������
�����Ѷȣ�һ��
|