微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 白铁皮(镀锌铁皮)常用于制造屋面、卷管和各种容器,利用废旧镀锌铁皮可制备磁性Fe3O4胶体粒子及副产物ZnO。制备流程如下:

已知:Zn及其化合物的性质与Al及其化合物的性质相似。请回答下列问题:
(1)用NaOH溶液处理废旧镀锌铁皮的作用是____________。
a.去除油污? b.溶解镀锌层? c.去除铁锈? d.钝化
(2)为获得Fe3O4胶体粒子,溶液B中必须含有一定量的Fe2+,可利用________检验其是否存在。
a.NaOH溶液? b.KSCN溶液? c.溶液KMnO4? d.氯水
(3)由溶液B制备Fe3O4胶体粒子的过程中,必须持续通入N2以保证产品的纯度,其原因是_____________ .
(4)在工业上常用水热法制造Fe3O4胶体粒子,有利于提高其纯度和磁性能,主要反应过程为:Fe2++S2O32-+O2+OH- Fe3O4(胶体)+S4O62-+H2O
Fe3O4(胶体)+S4O62-+H2O
①反应过程中起还原剂作用的微粒是________________;
②若反应过程中产生的Fe3O4(胶体)与S4O62-均为1mol,则参加反应的氧气在标准状况下的体积为____________L。
2、选择题 某酸性溶液中可能含有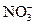 、I-、Cl-、Fe3+中的一种或几种离子,向其中加入溴水,溴水褪色,下列推测不正确的是
、I-、Cl-、Fe3+中的一种或几种离子,向其中加入溴水,溴水褪色,下列推测不正确的是
A.一定含I-
B.不含Fe3+
C.一定含Cl-
D.不含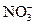
3、实验题 (9分)如图是某同学设计的放热反应的观察装置。
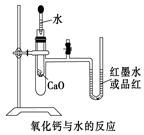
其实验顺序是:①按图所示将实验装置连接好。
②在U形管内加入少量红墨水(或品红)溶液。打开T型管?螺旋夹,使U形管内两边的液面处于同一水平面,再夹紧螺旋夹。③在中间的试管里盛1 g氧化钙,当滴入2 mL左右的蒸馏水后,同时打开螺旋夹即可观察。
试回答:(1)实验中观察到的现象是?
(2)该实验中必须进行的一步实验操作是?
(3)该实验的原理是
________________________________________________________________________
(4)实验中反应的化学反应方程式是?
(5)说明CaO、H2O的能量与Ca(OH)2的能量之间的关系?
(6)若该实验中CaO换成NaCl,实验还能否观察到相同现象?____。
4、实验题 已知某工业废水中含有大量CuSO4,少量的Ag+、Hg2+以及部分污泥,在实验室中通过下述过程可从该废水中回收硫酸铜晶体及其它物质。?
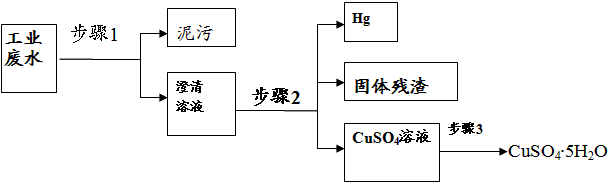
(1)步骤1的主要操作是________,需用到的玻璃仪器除烧杯外有___________。
(2)步骤2中需加入某种试剂后再将混合物分离,该试剂是(填化学式)___________,生成固体残渣的的离子方程式__________。
(3)步骤3中涉及的操作是:蒸发浓缩、________、过滤、烘干。
5、简答题 (10分)活性氧化锌用途非常广泛。以氧化锌粗品(含铁的氧化物、CuO和SiO2等杂质)为原料制备活性氧化锌并生产其它副产品的生产工艺流程如下:

已知:Zn(OH)2可溶于NaOH溶液。
请回答下列问题:
(1)“溶解”前将氧化锌粗品粉碎成细颗粒,其目的是?。
(2)操作A所得滤渣的主要成分是?。
(3)加入过量Fe时,滤液M中与Fe反应的离子有?。
(4) 操作C所得的滤渣P中含有Fe(OH)2和Fe(OH)3,请写出生成Fe(OH)3的化学反应方程式为?。
(5)“沉淀”的成分为ZnCO3・2Zn(OH)2・H2O,可用氧化物的形式把它改写为?。