��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ijѧ�����������ʵ�飺

�ش��������⣺
��1����ͬѧ��ʵ��Ŀ����______��
��2����ͼ�����ڵIJ��������Ϊ______��
��3������ʵ�鷽���õ���NaCl�����п϶�����______?���ѧʽ�����ʣ�Ϊ�˽����������������˵õ�����Һ�м���������______��
��4��д������B�����ӷ���ʽ______��
2��ʵ���� (15�֣�ͨ������һ��������Fe��Al�Ͻ���M����Һ��Ӧ����H2�ڱ�״���µ���������Լ�����Ͻ���Fe��Al������������������ͼװ������ȡH2,��������в�������ֱ������H2��
 ?
?
(1)C�����벣��˿���ţ�
(2) A�� ___________________________
(3) B��_____________________________
(4) ____________________________________
��5�� ____________________________________��
(6) �ڷ�Һ�¶��м���M����Һ��
(7) ______________________________________________________
3������� 1��2��3��4-���⻯���Ľṹ��ʽ��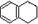 ������ʽ��C10H12��������Ϊ��ɫҺ�壬�д̼�����ζ���е�207�棬������ˮ����һ���������ܼ�������Һ�巢����Ӧ��C10H12+4Br2��C10H8Br4+4HBr�����ɵ����廯��������Ϊ��̬��������ˮ�����������⻯����Һ�塢����ˮ�ʹ�����Ϊԭ�ϣ��Ʊ�����������������Һ��ʵ�鲽�����£�
������ʽ��C10H12��������Ϊ��ɫҺ�壬�д̼�����ζ���е�207�棬������ˮ����һ���������ܼ�������Һ�巢����Ӧ��C10H12+4Br2��C10H8Br4+4HBr�����ɵ����廯��������Ϊ��̬��������ˮ�����������⻯����Һ�塢����ˮ�ʹ�����Ϊԭ�ϣ��Ʊ�����������������Һ��ʵ�鲽�����£�

�ٰ�һ�������Ȱ����⻯����ˮ�����ʵ��������У��������������ۣ�
����������Һ�壬���Ͻ��裬ֱ����Ӧ��ȫ��
��ȡ�·�Ӧ�����������������⻯����ֱ����Һ��ɫ��ʧ�����ˣ�����Һ�����Һ©�������ã�
�ܷ�Һ���õ��ġ�ˮ�㡱����������Һ���ش��������⣺
��1������ͼ��ʾ��װ�ã��ʺϲ���ٺ͢ڵIJ�������______��
��2��������в����������⻯����Ŀ����______��
��3��������й��˺�õ��Ĺ���������______��
��4���ڢܻ�õ�Ũ��Һ�м����Ҵ������ȣ��ɻ��һ�ֲ�����ˮ���л��д���÷�Ӧ�ķ���ʽ______��ʵ������ȡ��Ȳ������ͼ�е�װ��D����ʱ��Һ©���е�Һ��ͨ����______��
��5����Ȳ�ܱ����Ը��������Һ����������ƽ����Ӧ�ķ���ʽ��
______C2H2+______KMnO4+______H2SO4=______K2SO4+______MnSO4+______CO2+______H2O��
4��ʵ���� ��֪ij��ҵ��ˮ�к��д���CuSO4��������Ag+��Hg2+�Լ��������࣬��ʵ������ͨ���������̿ɴӸ÷�ˮ�л�������ͭ���弰�������ʡ�?
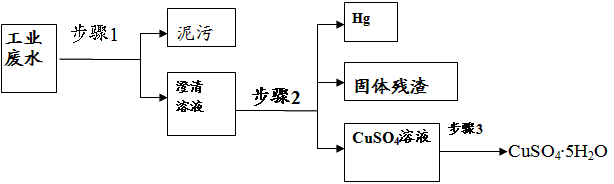
��1������1����Ҫ������________�����õ��IJ����������ձ�����___________��
��2������2�������ij���Լ����ٽ��������룬���Լ��ǣ��ѧʽ��___________�����ɹ�������ĵ����ӷ���ʽ__________��
��3������3���漰�IJ����ǣ�����Ũ����________�����ˡ���ɡ�
��4������2Ӧ����ͨ����н��У�ԭ����____________��
5��ʵ���� ij�о���ѧϰС�������һ��ʵ����̽��Ԫ�������ɡ���ͬѧ����Ԫ�طǽ��������Ӧ��ۺ�����֮��Ĺ�ϵ���������ͼװ����һ�������N��C��Si�ķǽ�����ǿ���Ƚϵ�ʵ���о�����ͬѧ�����û���Ӧ�Ĺ��ɣ�������ͼװ�������OԪ�صķǽ����Ա�Sǿ��ʵ���о����ش��������⣺

��1��ͼ��Dװ����ʵ���е�������________________��
��2������������������ѡ����ͬѧ��Ƶ�ʵ�����õ����ʣ�ͼ���Լ�AΪ_________���Լ�CΪ_________������ţ���
��ϡHNO3��Һ?��ϡ����?��̼���?��Na2SiO3��Һ?��SiO2?
��3��д����ƿ�з�����Ӧ�����ӷ���ʽ____________________��д���Թ�C�з�����Ӧ�����ӷ���ʽ___________________________���ɴ��жϣ�Ԫ��N��C��Si?�ǽ�����������ǿ��˳��Ϊ___________��
��4����ͬѧ��Ƶ�ʵ�����õ��Լ�AΪ________���Լ�BΪ________���Լ�CΪ________�� C��������Ϊdz��ɫ����������д��C�з�����Ӧ�Ļ�ѧ����ʽΪ______________��