微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 将等物质的量的A、B混合于2 L的密闭容器中,发生下列反应:
3A(g)+B(g) ?xC(g)+2D(g),经4min后测得D的浓度为0.5mol/L,c(A):c(B)=3:5,以C表示的平均速率v(C)=0.125mol・L-1・min-1,下列说法正确的是
?xC(g)+2D(g),经4min后测得D的浓度为0.5mol/L,c(A):c(B)=3:5,以C表示的平均速率v(C)=0.125mol・L-1・min-1,下列说法正确的是
A.反应速率v(B)=0.13 mol・L-1・min-1
B.该反应方程式中,x=1
C.4min时,A的物质的量为0.75mol
D.4min时,A的转化率为50%
参考答案:D
本题解析:根据题意得v(D)=0.5mol/L/4min=0.125 mol・L-1・min-1,以C表示的平均速率v(C)=0.125mol・L-1・min-1,根据化学反应速率之比等于方程式中化学计量数之比的x=2,B错误;同理可计算出v(B)=1/2v(D)=0.0625 mol・L-1・min-1,A错误;4min时,D的物质的量是0.5mol/L×2 L=1mol,所以消耗A、B的物质的量分别是1.5mol、0.5mol,设AB的起始物质的量均为ymol,则剩余A、B的物质的量分别是y-1.5mol、y-0.5mol,根据c(A):c(B)=3:5,得(y-1.5)/( y-0.5)=3:5,解得y=3mol。所以4min时,A的物质的量为3-1.5=1.5mol,C错误;A的转化率为1.5mol/3mol×100%=50%,D正确,答案选D。
本题难度:一般
2、选择题 X、Y、Z三种气体,当X和Y按1∶2的物质的量之比混合并通入密闭容器进行反应:X+2Y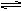 2Z,当达到化学平衡时,反应物总物质的量与生成物总物质的量相等,此时x的转化率是(? )
2Z,当达到化学平衡时,反应物总物质的量与生成物总物质的量相等,此时x的转化率是(? )
A.70%
B.60%
C.50%
D.40%
参考答案:B
本题解析:设X和Y的物质的量分别为1mol、2mol,X转化的物质的量为x,则
X?+? 2Y?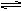 ?2Z
?2Z
初始物质的量/mol:? 1? 2? 0?
转化物质的量/mol:? x? 2x? 2x?
平衡物质的量/mol: 1―x? 2―2x? 2x?
依题意,可得:?(1―x)+(2―2x)= 2x
解之,得:x=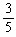 mol
mol
则x的转化率是 ×100%=60%。
×100%=60%。
本题难度:简单
3、选择题 中国首条“生态马路”在上海复兴路隧道建成,它运用了“光触媒”技术,在路面涂上一种光催化剂涂料,可将汽车尾气中45%的NO和CO转化成N2和CO2。下列对此反应的叙述中正确的是
A.使用光催化剂不改变反应速率
B.使用光催化剂能增大NO的转化率
C.升高温度能加快反应速率
D.改变压强对反应速率无影响
参考答案:C
本题解析:考查外界条件对反应速率和平衡的影响。催化剂只能改变反应速率,但不能改变平衡状态,选项A、D都不正确;升高温度移动加快反应速率,选项C正确;有气体参加或生成的反应,改变压强,可以改变反应速率,选项D不正确,答案选C。
本题难度:一般
4、选择题 可逆反应N2 + 3H2 2 NH3在一定条件下达到化学反应的限度时,下列判断正确的是
2 NH3在一定条件下达到化学反应的限度时,下列判断正确的是
A.N2完全转化为NH3
B.反应混合物中,NH3的质量分数不再改变
C.N2、H2与NH3的物质的量之比为1∶3∶2
D.消耗1 mol N2的同时消耗2 mol NH3
参考答案:BD
本题解析:略
本题难度:简单
5、选择题 反应N2O4(g) 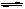 2NO2(g);△H=+57 kJ・mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如右图所示。下列说法正确的是(?)
2NO2(g);△H=+57 kJ・mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如右图所示。下列说法正确的是(?)

A.a、c两点的反应速率:a>c
B.a、c两点气体的颜色:a浅,c深
C.b、c两点的转化率:b>c
D.由b点到a点,可以用加热的方法
参考答案:D
本题解析:根据图像可知,a、c两点都在等温线上,a点压强小于c点压强,所以c点反应速率大于a点反应速率,A不正确;正方应是体积减小的可逆反应,则增大压强平衡向逆反应方向移动,NO2的浓度降低,颜色变浅,B不正确;b、c两点的NO2含量相同,转化率相同,C不正确。由b点到a点,NO2的含量增大,说明平衡向正反应方向移动。易于正方应是吸热反应,所以可以用加热的方法,D正确,答案选D。
点评:该题是中等难度的试题,主要是考查学生对可逆反应图像识别的掌握情况,意在培养学生的逻辑推理能力,提升的学生的学科素养。该题的关键是明确外界条件对化学平衡的影响及图象中纵横坐标的含义、“定一议二”“先拐先平”即可解答。
本题难度:一般