��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1�������
�������з�Ӧ��
A��2Mg+O2 2MgO B��CO2+H2O=H2CO3 C��Fe+CuSO4=Cu+FeSO4
2MgO B��CO2+H2O=H2CO3 C��Fe+CuSO4=Cu+FeSO4
D��Ba(OH)2+H2SO4=BaSO4��+2H2O E��NH4HCO3 NH3��+CO2��+H2O F��2HgO
NH3��+CO2��+H2O F��2HgO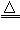 2Hg+O2��
2Hg+O2��
(1)����������ԭ��Ӧ����__________������ĸ����ͬ����
(2)�����ڻ��Ϸ�Ӧ������������ԭ��Ӧ����_____________��
(3)�����ڷֽⷴӦ������������ԭ��Ӧ����_____________��
�ο��𰸣�(1)A��C��F
(2)A
(3)F
���������
�����Ѷȣ�һ��
2�������� ����������������CN-�ķ�ˮ�����У�Һ���ڼ��������¿��Խ��軯�������������Σ��䶾�Խ�Ϊ�軯���ǧ��֮һ���������ν�һ��������Ϊ�����ʡ�
��1��ij����ˮ�к�KCN����Ũ��Ϊ650 mg��L-1?���������������������������·�Ӧ������N��Ϊ-3�ۣ���
KCN+2KOH+Cl2====KOCN+2KCl+H2O
��������Ԫ����__________��
��2��Ͷ�����Һ�ȣ��ɽ������ν�һ������Ϊ����������ƽ���л�ѧ����ʽ�����������ת�Ƶķ������Ŀ��
______KOCN+______KOH+______Cl2����______CO2+______N2+______KCl+______H2O
��3��������������ˮ20 L��ʹKCN��ȫת��Ϊ�����ʣ�������Һ��_________g��
�ο��𰸣���1��̼����C��
��2��2? 4? 3����2? 1? 6? 2?��3��35.5
�����������1���ڷ�ӦKCN+2KOH+Cl2====KOCN+2KCl+H2O�У�̼Ԫ�صĻ��ϼ۴�+2������+4��ʧ���ӱ�������
��2����KOCN+KOH+Cl2����CO2+N2+KCl+H2O��֪N��C��Ԫ�صĻ��ϼ۴�-3��+2�ֱ�����0��+4����ClԪ�صĻ��ϼ۴�0����-1������������ԭ��Ӧ��Ԫ�ػ��ϼ���������ȵĹ��ɣ�������ƽ��2KOCN+4KOH+3Cl2====2CO2+N2+6KCl+2H2O��
��3����KCN+2KOH+Cl2====KOCN+2KCl+H2O��2KOCN+4KOH+3Cl2====2CO2+N2+6KCl
+2H2O��֪2KCN+8KOH+5Cl2====2CO2+N2+10KCl+4H2O����2KCN��5Cl2����������20 L��ˮ��ʹKCN��ȫת��Ϊ�����ʣ�������Һ�ȣ�
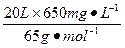 ��
��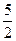 ��71 g��mol-1="35.5" g��
��71 g��mol-1="35.5" g��
�����Ѷȣ���
3��ѡ���� ����2NaBr+Cl2=2NaCl+Br2��Ӧ������˵������ȷ����
[? ]
A���÷�Ӧ�����û���Ӧ������������ԭ��Ӧ
B��Cl2����������������ԭ��Ӧ
C������1.6 g Br2���ɣ���Ӧ������ת����0.02 NA������
D����Ԫ���ڷ�Ӧ�м�̬���䣬����NaBr�Ȳ�����������Ҳ���ǻ�ԭ��
�ο��𰸣�D
���������
�����Ѷȣ���
4��ѡ���� �±��оٵĸ�������д��������ϵ����
���
| ��������I��ԭ��
| ������II�������
|
A
| O3������������
| �߿��е�O3�㱻��Ϊ����ı���ɡ
|
B
| ��100ml0.1mol/L��AlCl3��Һ�м���1.5g NaOH������Ӧ
| Al(OH)3����ȫ�ܽ�
|
C
| ��ԭ�Ӻ��������������
| �ƵĽ����Ա���ǿ
|
D
| HClO��SO2������Ư����
| ��Cl2��SO2ͬʱ ͨ��Ʒ����Һ��Ʒ����ɫ����� ͨ��Ʒ����Һ��Ʒ����ɫ�����
�ο��𰸣�A
�����������
�����Ѷȣ���
5������� ��5�֣���������(SeO2)��һ�����������䱻��ԭ��ĵ��������ܳ�Ϊ������Ⱦ�ͨ����ŨHNO3��ŨH2SO4��Ӧ����SeO2�Ի���Se�����������գ�
��1��Se��ŨHNO3��Ӧ�Ļ�ԭ����ΪNO��NO2����NO��NO2�����ʵ���֮��Ϊ1��1��д��Se��ŨHNO3�ķ�Ӧ����ʽ____?____��
��2����֪��Se+2H2SO4(Ũ)��2SO2��+SeO2+2H2O ��? 2SO2+SeO2+2H2O��Se+2SO42-+4H+
��SeO2��H2SO4(Ũ)��SO2����������ǿ������˳����____?__��
��3�����յõ���SeO2�ĺ���������ͨ������ķ����ⶨ���ⶨ��ԭ�����£���Ӧ�ٷ����������I2��I2�����ڷ�Ӧ���б��ζ�������Ϊָʾ������Na2S2O3��ҺΪ����Һ
��SeO2+KI+HNO3��Se+I2+KNO3+H2O
��I2+2Na2S2O3��Na2S4O6+2NaI
ʵ���У�ȷ����SeO2��Ʒ0.2500g��������0.2000 mol/L��Na2S2O3��Һ25.00 mL�����ⶨ����Ʒ��SeO2����������Ϊ_?__��
�ο��𰸣���5�֣���1��Se+2HNO3(Ũ)��H2SeO3+NO��+NO2��?��2�֣���
��2��H2SO4��Ũ����SeO2��SO2?��1�֣�
��3��0.555��2�֣�
�������������������ԭ��Ӧ���й��жϼ�����ȡ�
��1�����ݻ�ԭ����NO��NO2�����ʵ�����1�U1��֪���ڷ�Ӧ��Se��Ũ�����������ɣ�4�۵�H2SeO3�����Է�Ӧ�ķ���ʽ��Se+2HNO3(Ũ)��H2SeO3+NO��+NO2����
��2����������ԭ��Ӧ�У���������������ǿ����������ģ�����ԭ���Ļ�ԭ��ǿ�ڻ�ԭ����ġ����Ը��ݷ�Ӧ�ķ���ʽ��֪��SeO2��H2SO4(Ũ)��SO2����������ǿ������˳����H2SO4��Ũ����SeO2��SO2��
��3�����ݷ�Ӧ�ķ���ʽ��֪��SeO2��2I2��4Na2S2O3��������Ʒ��SeO2�����ʵ�����0.2000 mol/L��0.025L��4��0.00125mol����SeO2��������0.00125mol��111g/mol��0.13875g��������Ʒ��SeO2����������Ϊ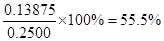 �� ��
�����Ѷȣ�һ��
|