微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 用氮化硅陶瓷代替金属制造发动机的耐热部件,能大幅度提高发动机的热效率。工业上用化学气相沉积法制备氮化硅,其反应如下:
3SiCl4 (g) + 2N2 (g) + 6H2 (g)  Si3N4(s) + 12HCl (g) ?H < 0
Si3N4(s) + 12HCl (g) ?H < 0
该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是 ( )
选项
| x
| y
|
A
| 温度
| 容器内混合气体的密度
|
B
| N2 的物质的量
| H2的转化率
|
C
| H2的浓度
| 平衡常数K
|
D
| 压强
| N2 的转化率
|
参考答案:D
本题解析: A.该反应的正反应是气体体积增大的放热反应。升高温度,平衡逆向移动,容器内混合气体的密度增大。错误。B.增加N2 的物质的量,使容器内的气体压强增大,化学平衡逆向移动,H2的转化率降低。错误。H2的浓度增大,但是由于化学平衡常数只与温度有关,而与压强、浓度等无关,所以平衡常数K不变。错误。D.增大压强,,化学平衡逆向移动,N2 的转化率降低。正确。
考点:考查温度、浓度、压强与气体的密度、物质的转化率、化学平衡常数的关系的知识。
本题难度:一般
2、选择题 实验室可利用反应“Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O”制取SO2,下列措施能降低该化学反应速率的是( )
A.适当降低反应温度
B.用铜粉代替铜片
C.加入MnO2作催化剂
D.将浓硫酸改为稀硫酸
参考答案:A、常温下铜与浓硫酸不反应,适当降低温度可以使化学反应速率减慢,故A正确;
B、用铜粉代替铜片,增大接触面积,加快反应速率,故B错误;
C、加入MnO2对该反应没有影响,故C错误;
D、铜与稀硫酸不反应,不能生成二氧化硫,故D错误.
故选A.
本题解析:
本题难度:一般
3、选择题 反应A+3B=2C+D在四种不同情况下的反应速率分别为:
①v(A) =0.15mol/(L・s)?②v(B)=0.6mol/(L・s)③v(C)=0.5mol/(L・s) ④v (D) =0.45mol/(L・s)
则反应进行由快到慢的顺序为:
A.④>③>①>②? B.②>④>③>①
C.②>③>④>①? D.④>③>②>①
参考答案:D
本题解析:同一化学反应方程式中,不同物质表示该反应的反应速率数值可能不同,但表示的意义完全相同,都是表示该反应的反应速率。并且,在同一化学反应方程式中,不同物质的速率之比等于化学计量数之比,所以,比较同一反应的反应速率快慢,需要将反应速率转化为同一种物质的反应速率才能比较;假设均将反应速率转化为v(B)的反应,则
①v(A)=3 v(B)=0.15mol/(L・s),得v(B)=0.05mol/(L・s);③v(C)=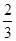 ?v(B)=0.5mol/(L・s),得
?v(B)=0.5mol/(L・s),得
v(B)=0.75mol/(L・s);④v (D) = ?v(B)=0.45mol/(L・s),得v(B)=1.35mol/(L・s);
?v(B)=0.45mol/(L・s),得v(B)=1.35mol/(L・s);
所以,正确的关系为:④>③>②>①
本题难度:一般
4、实验题 化学反应速率的变化和化学平衡移动的规律都可以通过实验得出结论,勒夏特列原理也是由实验总结出来的。
(1)将铜片投入到稀硝酸中,开始时产生气泡的速率很慢,随后反 应速率增大,根据你学到的知识分析,反应速率增大的原因是________________ __________________。当进行一段时间后,反应速率又减慢,这次速率减慢的原因是_______________________________。
应速率增大,根据你学到的知识分析,反应速率增大的原因是________________ __________________。当进行一段时间后,反应速率又减慢,这次速率减慢的原因是_______________________________。
(2)丙酮和碘在酸性溶液中发生下列反应:CH3COCH3+I2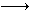 CH3COCH2I+H++I-。25℃时,该反应的速率由下列经验公式决定:
CH3COCH2I+H++I-。25℃时,该反应的速率由下列经验公式决定:
υ=k?c(CH3COCH3)?c(H+)[mol/(L?s)]
根据该经验公式,如果c(I2),c(CH3COCH3),c(H+)的起始浓度依次为0.01 mol/L,0.1 mol/L,0.01 mol/L,分析反应速率的变化趋势是_______________ ________________。
(3)在一支试管中先加入30 mL 0.01 mol/L FeCl3溶液,再滴加10 mL 0.01 mol/L KSCN溶液,摇匀。将制得的溶液平均分装于4支试管中,然后分别加入:①FeCl3固体;②KSCN固体;③KCl固体;④H2O。充分振荡后,溶液的颜色基本不变的是________(填序号)。
(4)在50 mL的注射器中吸入40 mL NO2和N2O4的混合气体,在另一同样规格的注射器中吸入40 mL Br2(g),对比两注射器中气体的颜色完全一致。然后都将注射器的活塞慢慢推至20 mL处,发现注射器内气体的颜色变化的现象是___________________________。推测平衡移动是通过观察装入NO2和N2O4的混合气体的注射器内气体的颜色比装入Br2(g)的注射器内气体的颜色_______。
(5)如果要鉴别密封于由两球连通的密闭容器中充满的红棕色气体是NO2和N2O4混合气还是Br2(g),可以____________________。
参考答案:(1)该反应是放热反应(1分)。随着反应的进行,硝酸的浓度减小(1分)。
(2)先逐渐增大后逐渐减小?(2分)。
(3)③?(2分)。
(4)前者先变深后变浅,但比原来深;后者只变深?(2分)。?浅?(2分)。
(5)通过加热(其他合理答案也可)?(2分)。
本题解析:略
本题难度:一般
5、简答题 学习了元素周期律后,同学们对第四周期过渡元素氧化物产生了浓厚的兴趣.是否只有二氧化锰能催化氯酸钾受热分解?氧化铁、氧化铜、氧化铬等对氯酸钾的受热分解有没有催化作用?对此他们进行了实验探究.请你根据要求完成下列部分实验报告.
Ⅰ课题名称:______
Ⅱ实验仪器及试剂:
实验仪器:带铁夹的铁架台、带橡皮塞的导管、量气装置、过滤装置、电子天平、药匙、大试管、酒精灯、计时器等.
实验试剂:二氧化锰、氧化铁、氧化铜、氧化铬和氯酸钾
Ⅲ实验步骤:略
Ⅳ实验数据:
实验
编号 | KClO3(g) | 氧化物 | 产生气体(mL)
(已折算到标况) | 耗时(s)
化学式
质量(g)
回收
1
0.60
-
-
-
10
480
2
0.60
MnO2
0.20
90%
67.2
36.5
3
0.60
CuO
0.20
90%
67.2
79.5
4
0.60
Fe2O3
0.20
90%
67.2
34.7
5
0.60
Cr2O3
0.20
异常
67.2
188.3
|
Ⅴ实验讨论:
(1)实验编号1的实验作用是______.
(2)实验编号3的实验中KClO3的分解率为______%(保留一位小数)
(3)在用Cr2O3?做研究实验时,发现有刺激性气味的气体产生,同时绿色的混合物变成了橘黄色.该刺激性气体可能是______(填分子式),可用______试纸检验.上述异常现象产生的原因是______.
Ⅵ实验结论:______.
参考答案:I?课题名称:因二氧化锰能催化氯酸钾受热分解,根据提供的试剂有氧化铁、氧化铜、氧化铬等,则含该实验来探究二氧化锰、氧化铁、氧化铜、氧化铬的氧化能力的比较,
故答案为:探究二氧化锰、氧化铁、氧化铜、氧化铬的氧化能力的比较;
V?实验讨论:
(1)因只有实验编号1不使用催化剂,则可以与使用催化剂的其它实验对照,故答案为:对照作用;
(2)实验编号3中生成氧气为67.2×10-3L22.4L/mol=0.003mol,由2KClO3催化剂.△2KCl+3O2↑可知,分解的氯酸钾为
0.002mol×122.5g/mol=0.245g,
则其分解率为0.245g0.60g×100%=40.8%,
故答案为:40.8;
(3)用Cr2O3做研究实验时,发现有刺激性气味的气体产生,同时绿色的混合物变成了橘黄色,则Cr元素的化合价升高,
Cl元素的化合价降低,氯酸钾与氧化铬发生了氧化还原反应,生成氯气,其化学式为Cl2,氯气能使湿润的淀粉碘化钾试纸变蓝,则可以使用湿润的淀粉碘化钾试纸检验氯气,
故答案为:Cl2;湿润的淀粉碘化钾;KClO3与Cr2O3发生了氧化还原反应;
VI?实验结论:因氧化铁和二氧化锰作催化剂时,时间少,相比较来说,其催化能力好,
故答案为:氧化铁和二氧化锰的催化能力较好.
本题解析:
本题难度:一般