微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 利用下图电解装置进行实验。
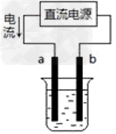
(1)若a、b是惰性电极,电解质溶液是氯化钠溶液,a极是_______极,总反应的离子方程式是_____________________。
(2)若a、b是惰性电极,电解质溶液是硝酸银溶液,b极上的现象是________________,总反应的离子方程式是___________________。
(3)若a、b是惰性电极,电解质溶液是硫酸钾溶液,a极上的电极反应是________,若两极附近分别加入石蕊试液,两极附近的现象是__________________。
参考答案:(1)阳;2Cl-+2H2O Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
(2)有银白色固体析出;4Ag++2H2O 4Ag+O2↑+4H+
4Ag+O2↑+4H+
(3)4OH--4e-=?2H2O+O2↑;a极附近溶液变红,b极附近溶液变蓝
本题解析:
本题难度:一般
2、选择题 新近研制的溴一锌蓄电池的基本构造是用碳棒作两极,用ZnBr2溶液作电解液,现有四个电极反应:①Zn-2e=Zn2+②Zn2++2e=Zn③Br2+2e=2Br-④2Br--2e=Br2充电时的阳极和放电时的负极反应分别为
A.④和①
B.②和③
C.③和①
D.②和④
参考答案:A
本题解析:充电时和电源正极相连的是阳极,发生反应为
2Br--2e=Br2
放电时,电子流出的是负极,反应为
Zn-2e=Zn2+
本题难度:一般
3、选择题 如图为阳离子交换膜法电解饱和食盐水原理示意图。下列说法不正确的是
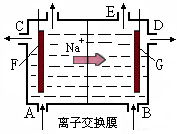
A.从E口逸出的气体是H2
B.从B口加入含少量NaOH的水溶液以增强导电性
C.标准状况下每生成22.4 LCl2,便产生2 mol NaOH
D.F电极材料为金属铁
参考答案:D
本题解析:根据装置图可知,在溶液中阳离子钠离子向右侧移动,所以G电极是阴极,F电极是阳极。所以氢离子在右侧生成,氯气在左侧生成。由于F是阳极,所以不能用活性电极铁作阳极。因此正确的答案是D。
本题难度:一般
4、选择题 (2014届浙江省金丽衢十二校高三第二次联考理综化学试卷)
早在1807年化学家戴维用电解熔融氢氧化钠制得钠,反应原理为:4NaOH(熔融) 4Na+2H2O+O2↑。后来盖・吕萨克用铁与熔融?氢氧化钠作用也制得钠,反应原理为:3Fe+4NaOH=Fe3O4+4Na↑+2H2↑。下列有关说法不正确的是
4Na+2H2O+O2↑。后来盖・吕萨克用铁与熔融?氢氧化钠作用也制得钠,反应原理为:3Fe+4NaOH=Fe3O4+4Na↑+2H2↑。下列有关说法不正确的是

A.电解熔融氢氧化钠制钠,阴极发生电极反应为:Na++e-=Na
B.盖・吕萨克法制钠原理是嫡的增加带动了反应的进行
C.若戴维法与盖・吕萨克法制得等量的钠,则两反应中转移的电子总数比为1:1
D.目前工业上常用电解熔融氯化钠法制钠(如图),电解槽中石墨极为阳极,铁为阴极
参考答案:C
本题解析:
A、电解池中阴极得到电子发生还原反应,则电解熔融氢氧化钠制钠,阴极发生电极反应为Na++e-=Na,A正确;B、根据反应式3Fe+4NaOH=Fe3O4+4Na↑+2H2↑可知,该反应是熵值增加的反应,因此盖・吕萨克法制钠原理是嫡的增加带动了反应的进行,B正确;C、根据反应方程式可知,若制得1mol钠,则戴维法与盖・吕萨克法中转移电子的物质的量是1mol、2mol,C不正确;D、电解池中阳极失去电子,阴极得到电子,因此用电解熔融氯化钠法制钠时,电解槽中石墨极为阳极,铁为阴极,则D正确,答案选C。
本题难度:一般
5、选择题 以石墨棒作电极,电解氯化铜溶液,若电解时转移的电子数是3.01×1023,则此时在阴极上析出铜的质量是( )
A.8g
B.16g
C.32g
D.64g
参考答案:电解氯化铜溶液时,阳极上氯离子失电子发生氧化反应生成氯气,阴极上铜离子得电子发生还原反应生成铜单质,所以阴极上的电极反应式为Cu2++2e-=Cu,设当有3.01×1023个电子转移时,在阴极上析出物质的质量为x.
? Cu2++2e-=Cu
2×6.02×1023 64g
?3.01×1023 x
所以x=16g,即析出铜的质量为16g,
故选B.
本题解析:
本题难度:简单