微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 化学反应可视为旧键断裂和新键形成的过程。共价键的键能是两种原子间形成1mol共价键(或其逆过程)时释放(或吸收)的能量。已知H-H键的键能为436kJ/mol. Cl-Cl键的键能为243kJ/mol,H-Cl键的键能为431kJ/mol,则 H2(g) +Cl2(g)=2HCl(g)的反应热(△H)等于
[? ]
A.- 183kJ/mol
B.+183kJ/mol
C.- 862kJ/mol
D.+862kJ/mol
参考答案:A
本题解析:
本题难度:一般
2、填空题 (5分)依据事实,写出下列反应的热化学方程式。
(1)在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为_________________________________________。
(2)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学方程式:
Fe2O3(s)+3CO(g)="=" 2Fe(s)+3CO2(g) △H=- A kJ/mol
3Fe2O3(s)+ CO(g)==2Fe3O4(s)+ CO2(g) △H=- B kJ/mol
Fe3O4(s)+CO(g)==3FeO(s)+CO2(g) △H= + C kJ/mol
写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学方程式:

参考答案:(共5分)
(1)CH3OH(l)+3/2 O2(g)=CO2(g) +2H2O(l) △H="-725.76kJ/mol " (2分)
△H="-725.76kJ/mol " (2分)
(2) CO (g)+ FeO (s)=CO2(g) +Fe (s) 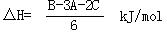 (3分)
(3分)
本题解析:略
本题难度:一般
3、选择题 下列离子方程式书写正确的是
A.向饱和NaHCO3溶液中通入过量SO2:SO2+HCO=CO2↑+HSO
B.含等物质的量溶质的亚硫酸氢铵溶液和氢氧化钠溶液的反应:NH+OH-=NH3?H2O
C.澄清石灰水与少量Ca(HCO3)2溶液混合:Ca2++2OH-+2HCO=CaCO3↓+CO+2H2O
D.NH4Al(SO4)2溶液中加入过量Ba(OH)2溶液:Al3++2SO+2Ba2++4OH-=AlO+2BaSO4↓+2H2O
参考答案:A
本题解析:分析:A.反应生成亚硫酸氢钠和二氧化碳;
B.等物质的量溶质的亚硫酸氢铵溶液和氢氧化钠溶液的反应,只发生亚硫酸氢根离子与碱的反应;
C.少量Ca(HCO3)2完全反应,反应生成碳酸钙和水;
D.NH4Al(SO4)2完全反应,反应生成硫酸钡、一水合氨、偏铝酸钡.
解答:向饱和NaHCO3溶液中通入过量SO2的离子反应为SO2+HCO3-=CO2↑+HSO3-,故A正确;
B.含等物质的量溶质的亚硫酸氢铵溶液和氢氧化钠溶液的反应的离子反应为HSO3-+OH-=NH3?H2O+SO42-,故B错误;
C.澄清石灰水与少量Ca(HCO3)2溶液混合的离子反应为Ca2++OH-+HCO3-=CaCO3↓+H2O,故C错误;
D.NH4Al(SO4)2溶液中加入过量Ba(OH)2溶液的离子反应为:NH4++Al3++2SO42-+2Ba2++5OH-=AlO2-+2BaSO4↓+2H2O+NH3?H2O,故D错误;
故选A.
点评:本题考查离子反应方程式的书写,明确发生的化学反应是解答的关键,注意与量有关的离子反应及反应的先后顺序为解答的难点,题目难度中等.
本题难度:简单
4、填空题 (4分)合成氨工业的核心反应是N2(g)+3H2(g)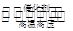 2NH3(g) ΔH=Q kJ・mol-1。反应过程中能量变化如图所示,回答下列问题。
2NH3(g) ΔH=Q kJ・mol-1。反应过程中能量变化如图所示,回答下列问题。
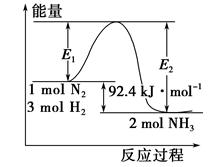
(1)在反应体系中加入催化剂,反应速率增大,E1和E2的变化:E1________,E2________(填“增大”、“减小”或“不变”)。
(2)在500 ℃、2×107 Pa和催化剂条件下向一密闭容器中充入0.5 mol N2和1.5 mol H2,充分反应后,放出的热量________(填“<”、“>”或“=”)46.2 kJ,理由是____________________________________________________________。
参考答案:(1) E1减小,E2减小。(2)< 因为该反应是可逆反应,反应不会进行到底
本题解析:(1)加入催化剂,降低了反应的活化能,即最高能量降低,所以E1和E2均减小;
(2)因为合成氨的反应是可逆反应,当0.5mol氮气与1.5mol氢气完全转化为氨气时才放出46.2kJ的热量,所以实际放出的热量要小于46.2kJ。
考点:考查催化剂的作用,对可逆反应的理解
本题难度:一般
5、选择题 下面有关离子化合物的说法正确是
A.离子化合物中一定含有金属元素,含金属元素的化合物一定是离子化合物。
B.离子键只存在于离子化合物中,离子化合物中一定含有离子键
C.离子化合物中不可能含有共价键
D.离子化合物受热融化破坏化学键,吸收能量,属于化学变化
参考答案:B
本题解析:离子化合物中不一定含有金属元素,例如氯化铵等。含金属元素的化合物也不一定是离子化合物,例如氯化铝等,A不正确;离子键只存在于离子化合物中,离子化合物中一定含有离子键,B正确;离子化合物中可能含有共价键,例如氢氧化钠等,C不正确;离子化合物受热融化破坏化学键,吸收能量,但并没有生成新物质,不属于化学变化,D不正确,答案选B。
点评:该题是中等难度的试题,主要是考查学生对化学键以及化学键与化合物关系、离子化合物熔融时变化的判断等基础知识的熟悉了解程度,以及灵活运用基础知识解决实际问题的能力的培养。注意学会举例排除筛选得出正确结论的解题方法。
本题难度:简单