微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 Ⅰ、恒温、恒压下,在一个可变容积的容器中发生如下反应: N2(g)+3H2(g)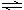 2NH3(g);△H<0
2NH3(g);△H<0
(1)工业生产中,该反应通常在高压下进行反应,做出此选择的理由是:
①?;
② ? 。
(2)开始时放入1mol N2和3mol H2,到达平衡后,生成amol NH3,若开始时放入χmol N2、3mol H2和y mol NH3,到达平衡后,NH3的物质的量为 3amol,则x= ? mol,y= ? mol。
Ⅱ、若该容器恒压、绝热(与外界不发生热交换),在一个与(2)反应前起始条件完全相同的容器中发生上述反应
(3)若开始时放入1mol N2和3mol H2,到达平衡后,生成b mol NH3,将b与(2)小题中的a进行比较?(选填一个编号)
(甲)a<b (乙)a>b (丙)a=b (丁)不能比较a和b的大小
作出此判断的理由是 。
Ⅲ、某研究性学习小组为探究利用电化学原理合成氨,设计如图所示的装置,
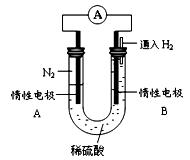
(4)电极B为?极
(5)电极A发生的电极反应式为?
(6)该电池工作一段时间后,电解质溶液pH?(填增大、减小或不变)
参考答案:
本题解析:略
本题难度:一般
2、选择题 某密闭容器中充入等物质的量的气体A和B,一定温度下发生反应A(g)+xB(g) 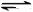 2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间的变化如下图所示。下列说法中正确是
2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间的变化如下图所示。下列说法中正确是
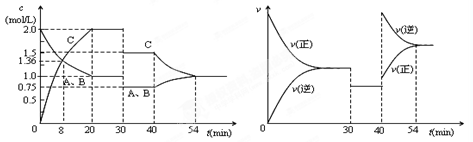
A.前8min A的平均反应速率为0.08mol/(L・s)
B.30min时扩大容器的体积,40min时升高温度
C.反应方程式中的x=1,正反应为吸热反应
D.30min和54min的反应的平衡常数相等
参考答案:B
本题解析:某密闭容器中充入等物质的量的气体A和B,一定温度下发生反应A(g)+xB(g) 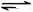 2C(g),达到平衡后,只改变反应的一个条件,30min时发现C和A.B的浓度都下降了;反应速率也是都减小,但是平衡不移动,说明反应方程式中的x=1;所以30min时扩大容器的体积。40min时C的浓度下降,AB的浓度上升;正逆反应速率都增大,逆反应的速率增大的快;说明40min时升高温度,正反应为放热热反应;30min和54min的反应的温度不同,所以平衡常数不同。前8min A的平均反应速率必须指明物质是谁。故选B。
2C(g),达到平衡后,只改变反应的一个条件,30min时发现C和A.B的浓度都下降了;反应速率也是都减小,但是平衡不移动,说明反应方程式中的x=1;所以30min时扩大容器的体积。40min时C的浓度下降,AB的浓度上升;正逆反应速率都增大,逆反应的速率增大的快;说明40min时升高温度,正反应为放热热反应;30min和54min的反应的温度不同,所以平衡常数不同。前8min A的平均反应速率必须指明物质是谁。故选B。
点评:.对于化学反应速率的有关图象问题,可按以下的方法进行分析:
(1)认清坐标系,搞清纵、横坐标所代表的意义,并与有关的原理挂钩。
(2)看清起点,分清反应物、生成物,浓度减小的是反应物,浓度增大的是生成物;一般生成物多数以原点为起点。
(3)抓住变化趋势,分清正、逆反应,吸、放热反应。升高温度时,v(吸)>v(放),在速率一时间图上,要注意看清曲线是连续的还是跳跃的,分清渐变和突变,大变和小变。例如,升高温度时,v(吸)大增,v(放)小增;增大反应物浓度时,v(正)突变,v(逆)渐变。
(4)注意终点。例如在浓度一时间图上,一定要看清终点时反应物的消耗量、生成物的增加量,并结合有关原理进行推理判断。
本题难度:一般
3、计算题 在一个容积为500mL的密闭容器中,充入5mol H2和2mol CO 在一定温度、压强下发生如下反应:
2H2(g)+CO(g) 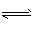 CH3OH(g),经5s后达到平衡状态。若此时测得CH3OH蒸气的浓度为2mol/L。
CH3OH(g),经5s后达到平衡状态。若此时测得CH3OH蒸气的浓度为2mol/L。
试求:
(1)以H2的浓度变化表示的该反应的速率。
(2)达到平衡时CO的转化率。
(3)该温度下的平衡常数K。
参考答案:开始时

2H2(g) + CO(g)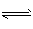 CH2OH(g)
CH2OH(g)
开始浓度10mol・L-1 4mol・L-1? 0
变化浓度4mol・L-1 2mol・L-1 2mol・L-1
平衡浓度6mol・L-1 2mol・L-1 2mol・L-1
(1)?
(2)CO的转化率为?
(3)
本题解析:
本题难度:一般
4、选择题 溴水中存在着如下的平衡:Br2+H2O HBr+HBrO,若要使溴水的颜色变浅,可采取的措施是
HBr+HBrO,若要使溴水的颜色变浅,可采取的措施是
A.加压
B.加入NaF晶体
C.通入SO2气体
D.加入NaI晶体
参考答案:BC
本题解析:A、加压对于没有气体参加的反应而言不会引起反应速率和化学平衡状态的改变,故A错误;B、加入氢氧化钠,能和酸反应生成盐和水,所以产物的浓度减小,平衡正向移动,能使溴水的颜色变浅,故B正确;C、通入SO2气体能和溴单质间发生氧化还原反应,使得溴单质的浓度减小,颜色变浅,故C正确;D、通入HCl气体,相当于增大了氢离子的浓度,所以化学平衡逆向移动,溴单质的量增多,颜色加深,故D错误.故选BC.
本题难度:简单
5、选择题 在一定条件下,将2molX和3molY 充入一密闭容器中,发生如下可逆反应: nX(g)+3Y(g)  2Z(g) 达到平衡时,X的转化率为a%,Y的转化率为b%,若a<b,则n的值为
2Z(g) 达到平衡时,X的转化率为a%,Y的转化率为b%,若a<b,则n的值为
[? ]
A.1
B.2
C.3
D.4
参考答案:A
本题解析:
本题难度:一般