|
高中化学知识点讲解《水的电离平衡》考点预测(2017年强化版)(六)
2017-08-22 17:12:48
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 常温下,将下列物质溶于水中分别配制成0.1 mol?L―1溶液,所得溶液pH大于7的是
A.NaCl
B.HCl
C.NaOH
D.CH3COOH
|
参考答案:C
本题解析:A、NaCl溶于水形成氯化钠溶液,氯化钠溶液显中性,pH等于7,故A错误;B、HCl溶于水形成盐酸,盐酸显酸性,pH小于7,故B错误;C、NaOH溶于水形成氢氧化钠溶液,氢氧化钠溶液显碱性,pH大于7,故C正确;D、醋酸溶于水得到醋酸溶液,显酸性,pH小于7,故D错误,故选:C。
考点:考查溶液酸碱性判断
本题难度:简单
2、选择题 常温下,关于溶液的稀释说法正确的是
A.将1 L 0.1mol・L-1的Ba(OH)2溶液加水稀释为2L
B.pH=13
C.pH=3的醋酸溶液加水稀释100倍,pH=5
D.pH=4的H2SO4加水稀释100倍,溶液中由水电离产生的[H+]=1×10-6mol・L-1
E.pH=8的NaOH溶液加水稀释100倍,其pH=6
参考答案:A
本题解析:试题分析:选项A、Ba(OH)2溶液中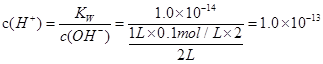
故其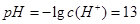 。故A正确。 。故A正确。
选项B、对于弱酸,稀释促进酸的电离,因此稀释100后,其pH<5.
选项C、水电离产生的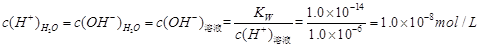
选项D、pH=8的NaOH溶液加水稀释100倍,其pH应接近7,但不会小于7.
考点:电解质溶液
点评:本题主要考查溶液pH的计算,以及溶液稀释后pH的变化。
①溶液中pH的计算,应掌握其基本的计算公式: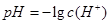 ; ;
②对于任意溶液中,均存在着公式: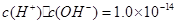 ; ;
③对于酸性溶液,水电离产生的
④对于溶液的稀释,无限稀释7为限。即酸性溶液稀释后,pH不会大于7;碱性溶液稀释后,pH不会小于7.
本题难度:简单
3、填空题 (10分)某化学实验小组从市场上买来一瓶某品牌食用白醋(主要是醋酸的水溶液),用实验室标准NaOH溶液对其进行滴定以测定它的准确浓度,完全反应时所得溶液pH大致为9 。下表是4种常见指示剂的变色范围:
指示剂
| 石蕊
| 甲基橙
| 甲基红
| 酚酞
| 变色范围(pH)
| 5.0~8.0
| 3.1~4.4
| 4.4~6.2
| 8.2~10.0
|
(1)该实验应选用 作指示剂。
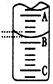
(2)右图表示50 mL滴定管中液面的位置,若A与C刻度间相差1mL,A处的刻度为25,滴定管中液面读数应为 mL;反应达滴定终点时的现象为 。
(3)为减小实验误差,该同学一共进行了三次实验,假设每次所取白醋体积均为V mL,NaOH标准液浓度为c mo1/L,三次实验结果记录如下:
实验次数
| 第一次
| 第二次
| 第三次
| 消耗NaOH溶液体积/mL
| 26.02
| 25.35
| 25.30
|
从上表可以看出,第一次实验中记录消耗NaOH溶液的体积明显多于后两次,其原因可能是 。
A.实验结束时,俯视刻度线读取滴定终点时NaOH溶液的体积;
B.滴定前滴定管尖嘴有气泡,滴定结束尖嘴部分充满溶液;
C.盛装白醋溶液的滴定管用蒸馏水洗过,未用白醋溶液润洗;
D.锥形瓶预先用食用白醋润洗过;
E.滴加NaOH溶液时,未充分振荡,刚看到溶液变色,立刻停止滴定。
(4)根据所给数据,写出计算该白醋中醋酸的物质的量浓度的表达式(不必化简):
c= mol/L。
参考答案:(共10分)
(1)酚酞(2分)
(2)25.40 (2分) 溶液从无色变为粉红色,且半分钟内不褪色(2分)
(3)BD(2分)
(4)〔(25.35+25.30)/2〕c/V(2分)
本题解析:(1)食醋中的醋酸是弱酸,氢氧化钠是强碱,所以滴定后的溶液呈碱性,所以选择酚酞作指示剂;
(2)A与C刻度间相差1mL,每一小格是0.1ml,滴定管的读数精确到0.01mL,所以正确读数是25.40mL;酚酞遇酸不变色,所以溶液开始无色,滴定终点时为弱碱性溶液,所以终点时的现象是溶液由无色变为浅红色或粉红色,且半分钟内不褪色;
(3)A、实验结束时,俯视刻度线读取滴定终点时NaOH溶液的体积,会使读数偏小,计算的体积也偏小,错误;B、滴定前有气泡,会使初读数偏小,滴定后消失,读数正确,则二者的差值偏大,正确;C、盛装白醋溶液的滴定管用蒸馏水洗过,未用白醋溶液润洗,对结果无影响,错误;D、锥形瓶用食醋润洗,使醋酸的物质的量增多,消耗氢氧化钠的体积增大,结果偏大,正确;E、滴加NaOH溶液时,未充分振荡,刚看到溶液变色,立刻停止滴定,滴定终点还未到达,使结果偏小,错误,答案选BD;
(4)第一次的数据与后两次的数据明显大,所以舍去第一次的数据,用后两次的数据进行计算,根据中和反应的实质,醋酸的浓度为〔(25.35+25.30)/2〕c/V。
考点:考查中和滴定实验,指示剂的判断,误差分析,浓度的计算
本题难度:一般
4、选择题 下列电离方程式中正确的是
[? ]
A、Na2HPO4溶于水:Na2HPO4 = 2Na+ + H+ + PO43-
B、NaHSO4熔化:NaHSO4 = Na+ + H+ +SO42-
C、HF溶于少量水中:HF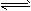 H+ + F- H+ + F-
D、(NH4)2SO4溶于水:(NH4)2SO4 2NH4+ + SO42- 2NH4+ + SO42-
参考答案:C
本题解析:
本题难度:简单
5、选择题 25℃时,BaCl2溶液呈中性,溶液中存在平衡:H2O?H++OH-;△H>0,下列叙述正确的是( )
A.向溶液中加入稀氨水,平衡逆向移动,c(OH-)降低,Kw不变
B.向溶液中加入少量固体CuSO4,c(H+)增大,Kw不变
C.向溶液中加入少量固体CH3COONa,平衡逆向移动,c(H+)降低,Kw不变
D.将溶液加热到90℃,Kw增大,溶液仍呈中性,pH不变
参考答案:B
本题解析:
本题难度:一般
| 